Beregning af normalitet i kemi:En praktisk vejledning
Af Kevin Beck
Opdateret 30. august 2022
Forståelse af koncentration i kemi
I kemi udtrykkes koncentration i form af mol snarere end masse eller volumen alene. En mol repræsenterer nøjagtigt 6,022×10²³ partikler af et stof, det samme antal atomer, som udgør 12g af den mest almindelige isotop af kulstof (C-12). At kende molmassen af hvert element gør det muligt for kemikere at konvertere mellem masse og mol med præcision.
Hvad er en muldvarp?
Et mol af ethvert stof indeholder 6,022×10²³ diskrete enheder. For eksempel vejer 1 mol vand (H₂O) 18,015 g, fordi den molære masse af oxygen (15,999 gmol⁻¹) plus to gange den molære masse af hydrogen (2×1,008 gmol⁻¹) er lig med 18,015 g.
Definition af molaritet
Molaritet (M) er antallet af mol opløst stof pr. liter opløsning. Det bruges almindeligvis til at beskrive koncentrationen af opløsninger i laboratoriemiljøer. For eksempel dissocieres en 1M opløsning af calciumchlorid (CaCl₂) ifølge:
CaCl₂(aq) ⇌ Ca²⁺(aq) + 2Cl⁻(aq)Denne reaktion producerer 1 mol Ca²⁺-ioner og 2mol Cl⁻-ioner pr. mol CaCl2.
Introduktion af normalitet
Normalitet (N) måler koncentrationen i gramækvivalenter pr. liter. Formlen er:
N = M × nhvor n er antallet af ækvivalenter pr. mol - i det væsentlige antallet af ladningsenheder en art kan donere eller acceptere i en reaktion. For CaCl2 er n=2 (én Ca²⁺ og to Cl⁻-ioner), så en 1M opløsning svarer til 2N.
Konvertering mellem molaritet og normalitet
For at konvertere normalitet til molaritet divideres med ækvivalensfaktoren:
M=N/n. Omvendt multiplicer molariteten med n for at opnå normalitet. For eksempel har 0,5N NaOH (en stærk base, der reagerer med en enkelt proton pr. molekyle) en molaritet på 0,5M, fordi n=1.
Praktisk anvendelse:Brug af online-beregnere
Til rutinemæssige beregninger, der involverer syrer og baser, kan online molaritets- og normalitetsberegnere strømline processen. Disse værktøjer giver dig mulighed for at indtaste molær masse, ønsket koncentration og ækvivalensfaktorer for at opnå nøjagtige resultater.
Se afsnittet Ressourcer for en praktisk lommeregner, der håndterer en lang række syre-base-kombinationer.
 Varme artikler
Varme artikler
-
 Nye hydrogeler viser lovende behandling af knogledefekterDer er vist et mikroskopisk billede af regenereret knogle i en kraniedefekt hos en mus. Kredit:University of California, Los Angeles Bioingeniører og tandlæger fra UCLA School of Dentistry har udv
Nye hydrogeler viser lovende behandling af knogledefekterDer er vist et mikroskopisk billede af regenereret knogle i en kraniedefekt hos en mus. Kredit:University of California, Los Angeles Bioingeniører og tandlæger fra UCLA School of Dentistry har udv -
 Forskere skaber en unik legering til luft, jernbanetransporterTorgom Akopyan, seniorforsker ved NUST MISIS Institut for Metalformning. Kredit:Sergey Gnuskov, SKAL IKKE MISIS Forskere fra National University of Science and Technology MISIS (NUST MISIS) i sama
Forskere skaber en unik legering til luft, jernbanetransporterTorgom Akopyan, seniorforsker ved NUST MISIS Institut for Metalformning. Kredit:Sergey Gnuskov, SKAL IKKE MISIS Forskere fra National University of Science and Technology MISIS (NUST MISIS) i sama -
 Tværfagligt samarbejde giver sværest, tyndeste belægninger endnu opdagetLehigh University-forskerne Nicholas Strandwitz (til venstre) og Brandon Krick (til højre) mener, at de har opdaget det sværeste, tyndeste, mest slidstærke belægninger endnu - plasma-forstærket atomla
Tværfagligt samarbejde giver sværest, tyndeste belægninger endnu opdagetLehigh University-forskerne Nicholas Strandwitz (til venstre) og Brandon Krick (til højre) mener, at de har opdaget det sværeste, tyndeste, mest slidstærke belægninger endnu - plasma-forstærket atomla -
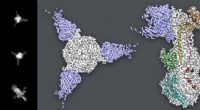 Cryo-EM-undersøgelse giver nye spor til skoldkopperinfektionBilleder ekstraheret fra cryo-EM-data (venstre og højre panel) viser varicella zoster-virusets gB-protein med tre antistoffer vedhæftet i enderne. Forskellige visninger af proteinet og antistoffer til
Cryo-EM-undersøgelse giver nye spor til skoldkopperinfektionBilleder ekstraheret fra cryo-EM-data (venstre og højre panel) viser varicella zoster-virusets gB-protein med tre antistoffer vedhæftet i enderne. Forskellige visninger af proteinet og antistoffer til
- Seniorprojektideer til elektronisk teknik
- Hvad er enzymet, der er ansvarlig for at fastgøre frie flydende nukleotider til en åben streng af …
- Kan et objekt have negativ kinetisk energi?
- Solen er direkte overhead ved 23,5 grader nordlig breddegrad i?
- Ny bog udforsker, hvordan mennesker bygger gode relationer på tværs af kulturelle grænser
- Ny forskning viser, hvordan klyngede partikler bestemmer elasticiteten af nogle geler


