Mestring af ækvivalente vægtberegninger:En omfattende vejledning
Af Kevin Beck Opdateret 30. august 2022
Ivan-balvan/iStock/GettyImages
Når kemikalier kombineres, gør de det i kendte, faste proportioner. Selvom du aldrig selv formelt har arbejdet med kemikalier, har du sikkert set din andel af kemiske reaktioner skrevet ud, og ved, at de optræder i et forudsigeligt format. Overvej for eksempel reaktionen mellem svovlsyre og hydroxidion for at producere vand og sulfation:
H2SO4 + 2OH- → 2H2O + SO42-
Tallene foran molekylerne, koefficienterne, viser antallet af hver reaktant og produktmolekyle i forhold til hinanden; underskrifterne i forbindelserne viser, hvor mange atomer af hver type der er i et givet molekyle. Disse tal er altid heltal, ikke brøktal som 4,24 eller 1,3. Men hvad repræsenterer de?
Begrebet ækvivalent vægt giver dig mulighed for at udforske det faktum, at atomer kombineres for at danne molekyler i faste talforhold, ikke masseforhold. Det vil sige, mens grundstofmasserne er forskellige, når det kommer til binding med andre atomer, er antallet af atomer , udtrykt i mol, er den afgørende faktor for, hvor meget af et givet grundstof eller en given forbindelse vil reagere med en given masse af et andet.
Hvad er muldvarpe?
Hvad er muldvarpe?
Et mol af et stof er defineret som 6,02 × 1023 individuelle partikler (atomer eller molekyler) af det pågældende stof. (Dette er tilfældigvis det nøjagtige antal atomer i 12 gram kulstof.) Når du bevæger dig fra venstre mod højre og nedad på det periodiske system, vil massen af et mol af et givet grundstof eller dets molekylvægt (MW ), er angivet i den tilsvarende boks for det pågældende element, normalt i midten.
Et eksempel hjælper med at give mening i denne definition. Hvis du har et molekyle vand, H2O, kan du se, at to H-atomer reagerer med et O-atom for at danne denne forbindelse. Men fordi MW af H er omkring 1,0 og end for O er 16,0, kan man se, at molekylet indeholder 2(1) =2 massedele H for hver (1)(16) =16 massedele O. Således består kun 2/18 =11/1 procent af massen af vand af H, mens 16/89 procent består af O.
Hvad er ækvivalent vægt?
Hvad er ækvivalent vægt?
Den ækvivalente vægt kan opfattes som vægten (eller massen, for at være præcis) af et stof, der vil indeholde en enkelt reaktiv proton (eller hydrogenion, H+) eller en enkelt reaktiv hydroxidion (−OH−). Førstnævnte tilfælde gælder for syrer , som er protondonorer, mens den anden gælder for baser , som er protonacceptorer.
Grunden til, at konceptet med ækvivalent vægt er nødvendigt, er, at nogle forbindelser kan donere eller acceptere mere end én proton, hvilket betyder, at for hver tilstedeværende muldvarp er stoffet i virkeligheden dobbelt reaktivt.
Formlen for det generelle antal ækvivalenter er
E =MW/ladningstal
Hvor MW er molekylvægten af forbindelsen, og ladningsnummer er antallet af proton- eller hydroxidækvivalenter, som forbindelsen indeholder. Eksempler med forskellige syrer og baser er med til at illustrere, hvordan dette fungerer i praksis.
Ækvivalenter af syrer og baser
Ækvivalenter af syrer og baser
Tag eksemplet med svovlsyre fra oven:
H2SO4 + 2OH- → 2H2O + SO42-
Du kan beregne MW af syren ved at henvise til et periodisk system for at få MW af hvert grundstof og tilføje 2(1) + (32) + 4(16) =98,0.
Bemærk, at denne syre kan donere to protoner, da sulfationen efterlades med en ladning på -2. Denne ækvivalente vægt er 98,0/2 =49,0.
For et grundlag er ræsonnementet det samme. Ammoniumhydroxid kan acceptere en proton i opløsning for at blive en ammoniumion:
NH4OH + H+ =H2O + NH4+
MW af ammoniumhydroxid er (14) + (4)(1) + (16) + 1 =35,0. Da kun én gang proton er forbrugt, er E for denne forbindelse 35,0/1 =35,0.
- En gramækvivalent (geq) er antallet af tilstedeværende gram stof divideret med dets ækvivalentvægt. Det kan også udtrykkes som antallet af ladningselementer indeholdt gange antallet af mol n.
Tilsvarende vægtberegner
Tilsvarende vægtberegner
Se ressourcerne for et websted, der giver dig mulighed for automatisk at beregne E for forskellige molekylvægte og ladningskombinationer, eller løse for en hvilken som helst værdi givet de to andre for enhver forbindelse, du kan finde på.
 Varme artikler
Varme artikler
-
 Ny forskning skaber en neutraliserende svamp til farlige kemikalierKredit:Pixabay/CC0 Public Domain Dr. Simon Holder, Læser i organisk kemi ved University of Kent (UK) og Dr. Barry Blight, lektor i kemi ved University of New Brunswick (Canada), har udviklet en ny
Ny forskning skaber en neutraliserende svamp til farlige kemikalierKredit:Pixabay/CC0 Public Domain Dr. Simon Holder, Læser i organisk kemi ved University of Kent (UK) og Dr. Barry Blight, lektor i kemi ved University of New Brunswick (Canada), har udviklet en ny -
 Van der Waals Forces:Den skjulte lim, der holder molekyler sammenkenzaza/iStock/GettyImages Van der Waals-kræfter danner elektrostatiske bindinger mellem molekyler. Disse intermolekylære interaktioner - dipol-dipol, dipol-induceret og London-dispersion - holder væ
Van der Waals Forces:Den skjulte lim, der holder molekyler sammenkenzaza/iStock/GettyImages Van der Waals-kræfter danner elektrostatiske bindinger mellem molekyler. Disse intermolekylære interaktioner - dipol-dipol, dipol-induceret og London-dispersion - holder væ -
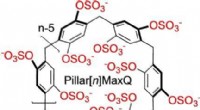 Molekylære beholdere til sekvestrering af neurotransmitterlægemidler i vandPillar[n]MaxQ:En ny værtsfamilie med høj affinitet til sekvestration i vand. Kredit:Angewandte Chemie International Edition Molekylære beholdere, der fjerner stoffer, toksiner, eller ildelugtende
Molekylære beholdere til sekvestrering af neurotransmitterlægemidler i vandPillar[n]MaxQ:En ny værtsfamilie med høj affinitet til sekvestration i vand. Kredit:Angewandte Chemie International Edition Molekylære beholdere, der fjerner stoffer, toksiner, eller ildelugtende -
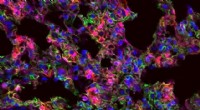 Nye materialer forbedrer leveringen af terapeutisk messenger-RNAMIT-forskere har designet nanopartikler, der kan levere messenger-RNA til specifikke organer. På dette billede, lungeceller, der udtrykker det syntetiske mRNA, viser sig som røde. Kredit:Piotr Kowalsk
Nye materialer forbedrer leveringen af terapeutisk messenger-RNAMIT-forskere har designet nanopartikler, der kan levere messenger-RNA til specifikke organer. På dette billede, lungeceller, der udtrykker det syntetiske mRNA, viser sig som røde. Kredit:Piotr Kowalsk
- Hvordan vil din julemiddag se ud i 2050?
- Forklar hvordan en frostlomme opstår i gartneri?
- Hvor mange sol kan passe ind i Sirius A?
- Når celler, der ligner struktur og funktion, går sammen, dannes de?
- Kan carboxylsyre reagere med Grignard-reagens?
- Fødevarer &ATP:Forståelse af cellulær energiproduktion


