Van der Waals Forces:Den skjulte lim, der holder molekyler sammen
kenzaza/iStock/GettyImages
Van der Waals-kræfter danner elektrostatiske bindinger mellem molekyler. Disse intermolekylære interaktioner - dipol-dipol, dipol-induceret og London-dispersion - holder væsker og faste stoffer sammen, hvilket påvirker egenskaber såsom overfladespænding og krystalstruktur. Selvom de er svagere end kovalente bindinger, former de afgørende adfærden af mange materialer.
TL;DR
Van der Waals-kræfter er svage elektrostatiske interaktioner, der binder molekyler. Fra stærkeste til svageste:dipol-dipol, dipol-induceret og London-dispersion. Hydrogenbindinger, en specialiseret dipol-dipol-interaktion, er særligt potente og styrer fysiske nøgletræk.
Typer af Van der Waals-styrker
1. Dipol-dipolkræfter – Polære molekyler med permanente positive og negative ender tiltrækker hinanden og skaber en stabil elektrostatisk binding.
2. Dipol-inducerede dipolkræfter – Et polært molekyle inducerer en midlertidig dipol i et tilstødende ikke-polært molekyle; den resulterende tiltrækning er svagere end ægte dipol-dipol-binding.
3. Londonske spredningskræfter – Selv ikke-polære molekyler oplever flygtige elektrontæthedsforskydninger, hvilket genererer midlertidige dipoler, der tiltrækker hinanden. Disse kræfter vokser sig stærkere i større molekyler med flere delokaliserede elektroner.
Når et brintatom er bundet til et stærkt elektronegativt grundstof (F, O, N), kaldes den resulterende stærke dipol-dipol-attraktion en hydrogenbinding , en hjørnesten i vands unikke egenskaber.
Hvordan Van der Waals Forces påvirker materialer
I gasser er molekyler langt fra hinanden og for energiske til, at Van der Waals kræfter kan betyde noget. I væsker forbliver molekyler mobile, gentagne gange danner og bryder svage bindinger, hvilket tillader dem at flyde, mens de stadig udviser overfladespænding og viskositet. I faste stoffer låser den reducerede kinetiske energi molekyler på plads, og den kumulative effekt af Van der Waals-interaktioner, sammen med ioniske eller metalliske bindinger, definerer krystalgitre, glasagtige strukturer og polymerfleksibilitet.
Mens kovalente bindinger dikterer kemisk identitet, styrer Van der Waals kræfter materialets fysiske karakter – tæthed, smeltepunkt, hårdhed.
 Varme artikler
Varme artikler
-
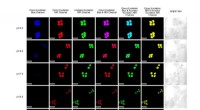 Gør en god ting bedre:En syretest, der ikke vil drukne i vandMichigan Tech kemikere dyrkede levende celler under forskellige pH-forhold, behandlede dem med et nyt fluorescerende cyaninfarvestof og fangede deres billeder under forskellige lysfrekvenser, både syn
Gør en god ting bedre:En syretest, der ikke vil drukne i vandMichigan Tech kemikere dyrkede levende celler under forskellige pH-forhold, behandlede dem med et nyt fluorescerende cyaninfarvestof og fangede deres billeder under forskellige lysfrekvenser, både syn -
 Hurtig påvisning af uranisotoper hjælper med at beskytte nukleare materialerAnalytiske kemikere fra ORNL koblede en mikroekstraktionsprobe til et massespektrometer til måling af uranisotopforhold fra miljøsvep. Kredit:Carlos Jones/ORNL, US Department of Energy Analytiske
Hurtig påvisning af uranisotoper hjælper med at beskytte nukleare materialerAnalytiske kemikere fra ORNL koblede en mikroekstraktionsprobe til et massespektrometer til måling af uranisotopforhold fra miljøsvep. Kredit:Carlos Jones/ORNL, US Department of Energy Analytiske -
 Forskere får kontrol over den interne struktur af selvsamlede kompositmaterialerEn model, der viser, hvordan et enkelt lagdelt materiale, afbildet i orange og blå, omdannes til et komplekst arkimedisk struktureret kompositmateriale, når det fryser rundt om en skabelon, afbildet i
Forskere får kontrol over den interne struktur af selvsamlede kompositmaterialerEn model, der viser, hvordan et enkelt lagdelt materiale, afbildet i orange og blå, omdannes til et komplekst arkimedisk struktureret kompositmateriale, når det fryser rundt om en skabelon, afbildet i -
 Akemikere låser op for hemmeligheder bag smeltede salteComputerkemiker Yu Shi fra University of Cincinnati. Kredit:Andrew Higley, University of Cincinnati En kemiker ved University of Cincinnati har fundet på en ny måde at studere de termodynamiske ege
Akemikere låser op for hemmeligheder bag smeltede salteComputerkemiker Yu Shi fra University of Cincinnati. Kredit:Andrew Higley, University of Cincinnati En kemiker ved University of Cincinnati har fundet på en ny måde at studere de termodynamiske ege
- Hvad er den nemmeste måde at tilføje energisoffer på?
- Hajer viser nye ændringer i deres immunkræftrelaterede gener
- Abell 1775:Chandra fanger slangebøsse under kollision
- Teamet skaber den første VX-neurotoksindetektor nogensinde
- IMERG viser ødelæggende nedbør over Østafrika
- Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialer


