Beregning af pH fra pKa:En praktisk vejledning
Sinhyu/iStock/GettyImages
Når du tænker på syrer - eddike, blegemiddel eller endda surheden af citronsyre - er du i gang med pH-skalaen, værktøjet, der kvantificerer surhedsgraden i vandige opløsninger. At forstå, hvordan man oversætter et stofs iboende surhedsgrad (dets syredissociationskonstant (Ka) ) til en målbar pH-værdi er afgørende for kemikere, undervisere og alle, der arbejder med syrer.
Syrer i opløsning
I vand donerer en syre en proton (H⁺) og bliver til en anion. Den frigjorte proton associerer med et vandmolekyle og danner hydroniumionen (H₃O⁺). Den oprindelige syre bliver dens konjugerede base. For eksempel dissocierer kulsyre (H₂CO₃) til H₃O⁺ og bicarbonat (HCO₃⁻).
Stærke syrer såsom saltsyre (HCl) frigiver protoner let selv i allerede sure medier, hvorimod svage syrer kun ioniseres mærkbart, når den omgivende protonkoncentration er lav (dvs. ved højere pH).
PH-skalaen
pH-skalaen er logaritmisk og spænder fra omkring 1 (meget sur) til 14 (meget basisk). Det er defineret af:
\(\tekst{pH} =-\log_{10}[\text{H}^+]\)
hvor \([\text{H}^+]\) er den molære koncentration af frie protoner. Hver ti gange stigning i protonkoncentrationen sænker pH-værdien med én enhed.
Eksempel: En 0,025M protonløsning har
\(\tekst{pH} =-\log_{10}(0,025) =1,602\)
Syreioniseringskonstanten (Ka)
Ka kvantificerer en syres tendens til at dissociere:
\(K_a =\dfrac{[A^-][\text{H}_3\text{O}^+]}{[HA]}\)
Højere Ka-værdier indikerer stærkere syrer, hvilket betyder mere fuldstændig dissociation ved ligevægt.
Fra Ka til pKa
Ved at tage den negative logaritme af Ka får vi syrens pKa:
\(\text{pKa} =-\log_{10}K_a\)
Beregning af pH ved hjælp af Henderson-Hasselbalch-ligningen
Henderson-Hasselbalch-ligningen forbinder pH, pKa og forholdet mellem konjugeret base og syre:
\(\text{pH} =\text{pKa} + \log_{10}\dfrac{[A^-]}{[HA]}\)
Dette forhold er især nyttigt for bufferopløsninger, hvor både syren og dens konjugatbase er til stede.
Eksempel: Eddikesyre (CH₃COOH) har \(K_a =1,77 \ gange 10^{-5}\). Hvis kun 10 % af syren er dissocieret, så er \([A^-]/[HA] =0,1\). Beregn først pKa:
\(\text{pKa} =-\log_{10}(1,77 \times 10^{-5}) =4,75\)
Anvend derefter Henderson–Hasselbalch:
\(\text{pH} =4,75 + \log_{10}(0,1) =4,75 - 1 =3,75\)
Ved en pH lig med pKa er koncentrationerne af syre og konjugatbase ens, hvilket betyder, at 50 % af syren er dissocieret.
Disse ligninger giver en ligetil metode til at forudsige pH-værdien af enhver opløsning, hvor syrens Ka og koncentration er kendt.
Vigtige ting
• pH-skalaen måler protonkoncentrationen på en logaritmisk skala.
• Ka udtrykker en syres dissociationstilbøjelighed; pKa er dens logaritmiske modstykke.
• Henderson-Hasselbalch-ligningen bygger bro mellem pH, pKa og syre/base-forholdet, hvilket muliggør nøjagtige pH-beregninger for buffere og svage syrer.
 Varme artikler
Varme artikler
-
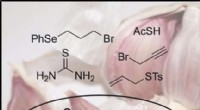 Kort total syntese af ajoene, en biologisk aktiv komponent i olieekstrakter af hvidløgKredit:Wiley Friske hvidløgsekstrakter indeholder en række sunde organiske svovlforbindelser, blandt hvilke ajoene udgør en vigtig olie-ekstraherbar ingrediens. Nu, kemikere i Det Forenede Kongeri
Kort total syntese af ajoene, en biologisk aktiv komponent i olieekstrakter af hvidløgKredit:Wiley Friske hvidløgsekstrakter indeholder en række sunde organiske svovlforbindelser, blandt hvilke ajoene udgør en vigtig olie-ekstraherbar ingrediens. Nu, kemikere i Det Forenede Kongeri -
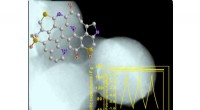 Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba
Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba -
 Høj effektivitet, billig katalysator til vandelektrolyseOxygenudvikling på overfladen af kerne-skal Co@NC elektrode i alkalisk vandelektrolyse. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Et forskerhold ledet af professor Sanga
Høj effektivitet, billig katalysator til vandelektrolyseOxygenudvikling på overfladen af kerne-skal Co@NC elektrode i alkalisk vandelektrolyse. Kredit:Daegu Gyeongbuk Institut for Videnskab og Teknologi (DGIST) Et forskerhold ledet af professor Sanga -
 Ædelmetalklynger kan forbedre ydeevnen af katalysatorer og spare ressourcerSkematisk fremstilling af en ædelmetalkatalysator med inaktive enkelte atomer (venstre) og aktive klynger (højre; ædelmetal:hvid; bæremetal:gul; oxygen:rød). Kredit:Florian Maurer, SÆT Milliarder
Ædelmetalklynger kan forbedre ydeevnen af katalysatorer og spare ressourcerSkematisk fremstilling af en ædelmetalkatalysator med inaktive enkelte atomer (venstre) og aktive klynger (højre; ædelmetal:hvid; bæremetal:gul; oxygen:rød). Kredit:Florian Maurer, SÆT Milliarder
- Set fra Pluto Ville solen forekomme mere end tusind gange svagere på jorden?
- Hvad er en ændring i hastighed over tid for et objekt?
- Besættelse af de sidste neandertalergrupper i den kantabriske region
- Hvilken mad giver dig energi?
- Hvad er et repræsentativt element? En klar definition
- Hvilken retning ser solen ud til at rejse over himlen hver dag?


