Forstå diffusion:Hvordan molekyler bevæger sig fra høj til lav koncentration
Af bidragyder | Opdateret 24. marts 2022
Diffusion forklaret
Diffusion er den spontane bevægelse af molekyler fra et område med højere koncentration til et område med lavere koncentration, drevet af deres iboende kinetiske energi. Over tid udligner denne proces koncentrationer uden behov for en katalysator, idet den udelukkende er afhængig af den indre energi i selve molekylerne.
Den indre energis rolle
Alle molekyler besidder indre energi, der viser sig som tilfældig, mikroskopisk bevægelse. Selv i et bad med vand, der stadig ser ud, bevæger molekylerne indeni sig med hundredvis af fod i sekundet. Den hastighed, hvormed diffusion sker, afhænger af denne indre energi og de specifikke egenskaber for hvert stof.
Illustrativt eksempel
Overvej en forseglet beholder adskilt af en aftagelig barriere. På den ene side er kulilte (CO) til stede; på den anden side oxygen (O2). Mens barrieren forbliver, er gasserne ubevægelige på makroskopisk niveau, men deres molekyler kolliderer konstant med barrieren. Når barrieren er fjernet, begynder molekylerne at blande sig og bevæger sig fra den CO-rige side mod den O₂-rige side. Til sidst bliver hele beholderen til en homogen blanding, der i dette tilfælde danner kuldioxid (CO₂), når gasserne reagerer.
Sidste artikelBeregning af pH fra pKa:En praktisk vejledning
Næste artikelMolar Mass Calculator:Nøjagtig molekylvægtberegning
 Varme artikler
Varme artikler
-
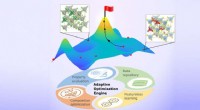 Ny tilgang bestemmer optimale materialedesign med minimale dataKredit:Northwestern University Northwestern University-forskere har udviklet en ny beregningsmæssig tilgang til at accelerere designet af materialer, der udviser metal-isolator overgange (MIT), en
Ny tilgang bestemmer optimale materialedesign med minimale dataKredit:Northwestern University Northwestern University-forskere har udviklet en ny beregningsmæssig tilgang til at accelerere designet af materialer, der udviser metal-isolator overgange (MIT), en -
 Videnskaben bag fugtighedsmålere:Sådan måler de fugtAf Josh Fredman, Opdateret 24. marts 2022 SEAN GLADWELL/Moment/GettyImages Hvad måler en fugtighedsmåler Fugtighed, mængden af vanddamp i luften, er en nøglevariabel i meteorologi. Selvom der findes
Videnskaben bag fugtighedsmålere:Sådan måler de fugtAf Josh Fredman, Opdateret 24. marts 2022 SEAN GLADWELL/Moment/GettyImages Hvad måler en fugtighedsmåler Fugtighed, mængden af vanddamp i luften, er en nøglevariabel i meteorologi. Selvom der findes -
 Fleksible faste elektrolytter til hel-solid-state lithium-batterierFotografier af ultratynd Li6.4La3Zr1.4Ta0.6O12-baseret film. Kredit:Qingya Guo, Ningbo Institute of Materials Technology and Engineering Faste elektrolytter af granattypen tiltrækker stor interesse
Fleksible faste elektrolytter til hel-solid-state lithium-batterierFotografier af ultratynd Li6.4La3Zr1.4Ta0.6O12-baseret film. Kredit:Qingya Guo, Ningbo Institute of Materials Technology and Engineering Faste elektrolytter af granattypen tiltrækker stor interesse -
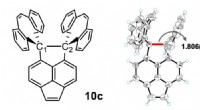 Ny rekord sat for carbon-carbon enkeltbindingslængdeDen kemiske struktur af forbindelsen, som viste den længste C-C-binding. Kredit:Ishigaki Y. et al., Chem , 8. marts, 2018. Forskere fra Hokkaido University har syntetiseret en organisk forbindel
Ny rekord sat for carbon-carbon enkeltbindingslængdeDen kemiske struktur af forbindelsen, som viste den længste C-C-binding. Kredit:Ishigaki Y. et al., Chem , 8. marts, 2018. Forskere fra Hokkaido University har syntetiseret en organisk forbindel
- Hvad reagerer kulbrinte med, når kulbrinte forbrændes?
- Lysbaseret produktion af lægemiddel-opdagelsesmolekyler
- Detektering af virus i et nålestik
- Plastprodukter kunne nemt blive elektroniske med de første formbare kredsløb i kulstof
- Geners samspil giver fingerpeg om, hvordan nye celletyper kunne udvikle sig
- Forudsiger en ny fase af superionisk is


