Ioner dannes, når sølvnitrat opløses i vand
Af Michael Judge
Opdateret 24. marts 2022
Ionisk dissociation af sølvnitrat
Sølvnitrat (AgNO₃) er et klassisk eksempel på en ionisk forbindelse, der let opløses i vand. Ved opløsning adskilles gitteret i dets bestanddele:sølvkationen (Ag⁺) og nitratanionen (NO₃⁻). Denne proces er drevet af den stærke elektrostatiske tiltrækning mellem de modsat ladede arter.
Sølvkation (Ag⁺)
Sølvionen bærer en enkelt positiv ladning efter at have mistet en elektron. Kationer såsom Ag⁺ er velkendte for deres antimikrobielle aktivitet; for eksempel viste en undersøgelse fra National Public Health Institute of Finland, at Ag⁺ effektivt kan hæmme væksten af Legionella bakterier. Disse egenskaber har ført til medicinske anvendelser, selvom sølvioner forbliver giftige for en lang række mikrober.
Nitratanion (NO₃⁻)
Nitrationen er en trivalent gruppe bestående af et nitrogenatom bundet til tre oxygenatomer, der bærer en netto negativ ladning. NO₃⁻ er naturligt til stede i fødevarer som spinat og er en nøglekomponent i mange gødninger. Selvom det er vigtigt i moderate mængder, kan overdreven nitratindtagelse udgøre sundhedsrisici, så dets koncentration er reguleret i fødevarer og vandforsyninger.
Yderligere ioner i opløsning
Selv i ultrarent vand opstår spormængder af ioner fra autoionisering af vandmolekyler:
- Hydroniumioner (H₃O⁺) dannes, når H⁺ associeres med vand.
- Hydroxidioner (OH⁻) produceret samtidigt.
 Varme artikler
Varme artikler
-
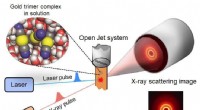 Hvert øjeblik med ultrahurtig kemisk binding fanget på filmBindingsdannelsesreaktionen i et guldtrimerkompleks initieres af en laserpuls, og en tredimensionel struktur efter en bestemt tidsforsinkelse detekteres af et røntgenstrålingsbillede. Kredit:IBS M
Hvert øjeblik med ultrahurtig kemisk binding fanget på filmBindingsdannelsesreaktionen i et guldtrimerkompleks initieres af en laserpuls, og en tredimensionel struktur efter en bestemt tidsforsinkelse detekteres af et røntgenstrålingsbillede. Kredit:IBS M -
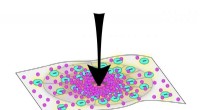 Under pres:Nyt bioinspireret materiale kan formskifte til eksterne kræfterTil JHU-teamets eksperiment, øget kraft (pilen peger nedad) påført materialet førte til flere elektriske ladninger, og dermed, mere mineralisering. Kredit:Pam Li/Johns Hopkins University Inspirere
Under pres:Nyt bioinspireret materiale kan formskifte til eksterne kræfterTil JHU-teamets eksperiment, øget kraft (pilen peger nedad) påført materialet førte til flere elektriske ladninger, og dermed, mere mineralisering. Kredit:Pam Li/Johns Hopkins University Inspirere -
 Silikoner opnået ved lave temperaturer ved hjælp af luftKredit:CC0 Public Domain Russiske forskere har udviklet en ny metode til syntetisering af para-carboxyplenylsiloxaner, en unik klasse af organosiliciumforbindelser. De resulterende forbindelser er
Silikoner opnået ved lave temperaturer ved hjælp af luftKredit:CC0 Public Domain Russiske forskere har udviklet en ny metode til syntetisering af para-carboxyplenylsiloxaner, en unik klasse af organosiliciumforbindelser. De resulterende forbindelser er -
 Grøn kemi og biobrændstof:Mekanismen for et centralt fotoenzym dekrypteretKunstnerindtryk af den enzymatiske katalyse foreslået i mekanisme af fedtsyrefotodecarboxylase. Kredit:Damien Sorigué Funktionen af enzymet FAP, nyttig til produktion af biobrændstoffer og til g
Grøn kemi og biobrændstof:Mekanismen for et centralt fotoenzym dekrypteretKunstnerindtryk af den enzymatiske katalyse foreslået i mekanisme af fedtsyrefotodecarboxylase. Kredit:Damien Sorigué Funktionen af enzymet FAP, nyttig til produktion af biobrændstoffer og til g
- I reaktionen MgCl2 plus 2KOH og 65532 Mg(OH)2 2KCl hvor mange mol KOH reagerer med 1 mol MgCl2?
- Videnskaben omkring planeten bruger billeder af Jorden fra rumstationen
- Billeddannelse af komplekse domænevægstrukturer i magnetiske nanostriber
- Magnetiske pindsvin kunne lagre store data på et lille rum
- Teknologien er bedre end nogensinde – men tusindvis af amerikanere dør stadig i bilulykker hvert å…
- Små myrer:Forskere bygger verdens mindste motor


