5 nøglefaktorer, der bestemmer reaktionsrater
Af Michael Judge
Opdateret 24. marts 2022
I kemi er hastigheden, hvormed en reaktion skrider frem, kritisk - især for industrielle processer. En reaktion, der er termodynamisk gunstig, men træg, såsom omdannelsen af diamant til grafit, kan være praktisk talt ubrugelig. Omvendt kan en for hurtig reaktion udgøre sikkerhedsrisici. Forståelse og styring af de faktorer, der påvirker reaktionshastigheder, gør det muligt for kemikere at designe sikrere og mere effektive processer.
Temperatur
En stigende temperatur fremskynder generelt reaktioner. Den underliggende årsag er aktiveringsenergibarrieren, der skal overvindes for at molekyler kan reagere. Højere termisk energi øger den kinetiske energi af molekyler, så flere kollisioner opnår den kritiske aktiveringsenergi. En nyttig tommelfingerregel er, at hastigheden for mange reaktioner groft fordobles for hver 10°C temperaturstigning (Arrhenius-adfærd).
Koncentration og tryk
For reaktioner i samme fase - f.eks. to opløste stoffer i vand - øger højere koncentrationer sandsynligheden for produktive kollisioner og fremskynder derved reaktionen. Effektens størrelse afhænger af reaktionens rækkefølge med hensyn til hver reaktant. I gasfasen øger et stigende tryk på samme måde kollisionsfrekvensen, hvilket ofte accelererer reaktionen i forhold til trykstigningen.
Mellem (opløsningsmiddel) effekter
Det omgivende medium kan ændre reaktionshastighederne væsentligt. Opløsningsmidler, der stabiliserer ladede eller polære overgangstilstande, såsom vand eller meget polære organiske opløsningsmidler, kan sænke aktiveringsenergien og fremskynde reaktioner, der involverer ioniske mellemprodukter. Omvendt kan et ikke-polært opløsningsmiddel bremse en reaktion, der kræver en polær overgangstilstand.
Katalysatorer
Katalysatorer sænker aktiveringsenergien af en reaktion ved at tilvejebringe en alternativ vej. Dette kan involvere adsorption af reaktanter på en katalytisk overflade, dannelse af mellemliggende komplekser eller tilvejebringelse af et organiseret miljø, der favoriserer overgangstilstanden. Fordi flere molekyler har den lavere energibarriere ved en given temperatur, stiger den samlede hastighed, uden at katalysatoren forbruges.
Overfladeareal af faste reaktanter
Når en reaktant er et fast stof, begrænser det eksponerede overfladeareal reaktionen til grænsefladen med den anden fase. Forøgelse af overfladearealet - ved for eksempel at knuse et fast stof til pulver - giver flere aktive steder og accelererer derved reaktionen. Klassiske eksempler inkluderer hurtigere rustning af findelt jern sammenlignet med en massiv blok.
Ved strategisk at manipulere disse faktorer kan kemikere finjustere reaktionshastighederne for at opfylde målene for sikkerhed, effektivitet og økonomi.
 Varme artikler
Varme artikler
-
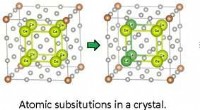 Udnyttelse af symmetrier:Fremskynder beregningsstudiet af solide løsningerGrafisk abstrakt. Kredit:Journal of Chemical Information and Modeling (2022). DOI:10.1021/acs.jcim.2c00389 Symmetri er et udbredt træk i naturen på alle skalaer. For eksempel kan vores blotte øjne
Udnyttelse af symmetrier:Fremskynder beregningsstudiet af solide løsningerGrafisk abstrakt. Kredit:Journal of Chemical Information and Modeling (2022). DOI:10.1021/acs.jcim.2c00389 Symmetri er et udbredt træk i naturen på alle skalaer. For eksempel kan vores blotte øjne -
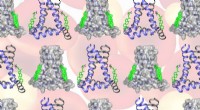 Kolesterol hjælper influenzavirus med at flygte gennem værtscellemembranenVed at bruge en teknik kaldet solid-state nuklear magnetisk resonans (NMR) spektroskopi, et MIT -team fandt ud af, at to kolesterolmolekyler binder til et influenzaprotein kaldet M2 for at skære viral
Kolesterol hjælper influenzavirus med at flygte gennem værtscellemembranenVed at bruge en teknik kaldet solid-state nuklear magnetisk resonans (NMR) spektroskopi, et MIT -team fandt ud af, at to kolesterolmolekyler binder til et influenzaprotein kaldet M2 for at skære viral -
 Ny indsigt kan fremme udviklingen af naturlige og sikrere fungiciderIsolering af svampeprøve fra en koloni. Kredit:Sylvain Dubey Landbrugsindustrien er stærkt afhængig af kemiske fungicider for at beskytte afgrøder. Mange af disse produkter har en skadelig effekt
Ny indsigt kan fremme udviklingen af naturlige og sikrere fungiciderIsolering af svampeprøve fra en koloni. Kredit:Sylvain Dubey Landbrugsindustrien er stærkt afhængig af kemiske fungicider for at beskytte afgrøder. Mange af disse produkter har en skadelig effekt -
 Hyperpolariseret proton -MR bruges til at observere metaboliske processer i realtidFantomet brugt til hyperpolariseret billeddannelse, med en illustration af billedskiver erhvervet ved hjælp af den nye teknik. Kredit:©:Laurynas Dagys, University of Southampton Magnetic resonance
Hyperpolariseret proton -MR bruges til at observere metaboliske processer i realtidFantomet brugt til hyperpolariseret billeddannelse, med en illustration af billedskiver erhvervet ved hjælp af den nye teknik. Kredit:©:Laurynas Dagys, University of Southampton Magnetic resonance
- Hvorfor er kaliumhydrogen phthalat en god primær standard?
- Hvad er den længste syd for Zodiac Constellation?
- Hvad betyder det at drømme om planter, der vokser på dig?
- EU til greenlight Bayer-Monsanto-overtagelse:kilde
- Bland og match:Blanding af nanopartikler for at lave multifunktionelle materialer
- Hvilken satellit er den største i forhold til størrelsen på sin planet?


