Atomer, elementer og isotoper:Forståelse af stoffets byggesten
jirkaejc/iStock/GettyImages
Atomer er de udelelige enheder, der udgør alt almindeligt stof. Deres navn stammer fra det græske ord for "kan ikke skæres." Hvert atom indeholder en kerne af protoner og neutroner omgivet af en sky af elektroner. Det enkleste atom, hydrogen, indeholder én proton og én elektron, men ingen neutroner.
Hvad er nogle eksempler på atomer?
Almindeligvis stødte atomer inkluderer brint, oxygen og kulstof. Vand, med formlen H2O, består af to hydrogenatomer bundet til et oxygenatom. Selvom vand er en kemisk forbindelse, er dets atomer ikke identiske, hvilket adskiller det fra et grundstof.
Atomstrukturen varierer på tværs af elementer. Brint har en proton og en elektron; alle andre atomer har mindst én proton, én neutron og én elektron. Protoner og neutroner har lignende masser (henholdsvis ≈1,6726×10⁻²⁷kg og 1,6749×10⁻²⁷kg), mens elektroner er langt lettere (≈9,1094×10⁻³¹kg) og ofte kan negligeres i masseberegninger.
I et neutralt atom er antallet af protoner lig med antallet af elektroner, hvilket balancerer de positive og negative ladninger. Når denne balance forstyrres, bliver atomet en ion, der bærer en nettoladning (f.eks. +3 eller –2).
Atomadfærd afspejler solsystemmodellen:kernen fungerer som solen, hvor elektroner kredser på grund af elektrostatisk tiltrækning. Kvantemekanik beskriver elektronpositioner sandsynligt, hvilket understøtter moderne teknologier såsom halvledere og kvanteberegning.
Hvad er navnene på atomer?
Det periodiske system er den endelige reference for atomnavne og nøgleegenskaber. Den viser 103 grundstoffer - 92 naturligt forekommende og 11 syntetisk fremstillede - hver identificeret ved et unikt atomnummer (antallet af protoner). Tabellens indtastning viser typisk elementets symbol, atomnummer og gennemsnitlige atommasse.
For eksempel har natrium (Na) atomnummer 11 og en gennemsnitlig masse på 22,99 amu. At trække atomnummeret fra massen (≈23) giver 12 neutroner. Denne beregning viser, hvordan neutrontal kan udledes ud fra atommasse.
Når du bevæger dig hen over det periodiske system fra venstre mod højre eller ned fra top til bund, bliver atomer generelt tungere på grund af tilføjelsen af protoner og neutroner.
Hvad er de forskellige typer atomer?
Atomer er kategoriseret efter deres neutronantal. Isotoper er atomer af samme grundstof (identisk atomnummer), der adskiller sig i neutrontal, hvilket fører til forskellige atommasser. For eksempel forekommer jern (Fe) naturligt som en blanding af fire isotoper:⁵⁴Fe (5,845%), ⁵⁶Fe (91,754%), ⁵⁷Fe (2,119%) og ⁵⁸Fe (0,282%). Hver isotop deler kemiske egenskaber, men adskiller sig i fysiske egenskaber såsom masse og smeltepunkt.
Andre klassificeringer omfatter ædelgasser (gruppe 18), metaller (alkali, jordalkali, overgang, post-transition, actinoider, lanthanoider), metalloider (bor, arsen, silicium, germanium, antimon, tellur, astatin) og ikke-metaller (svovl, nitrogen, osv.).
Hvad er forbindelser og molekyler?
En forbindelse består af to eller flere forskellige grundstoffer bundet sammen, såsom vand (H2O). Et molekyle er den mindste diskrete enhed af en forbindelse, der bevarer sin kemiske identitet. For eksempel er et enkelt natriumchloridmolekyle (NaCl) det mindste fragment af bordsalt, der stadig udviser saltets egenskaber.
Opløsninger opstår, når et eller flere stoffer (opløste stoffer) opløses i et andet (opløsningsmiddel) uden at danne kemiske bindinger – sukker opløst i vand er et klassisk eksempel.
Hvad er hovedelementerne?
Jordens bulksammensætning er domineret af ti elementer, der tegner sig for ~99% af dens masse. Ilt udgør 46,6%, silicium 27,7%, aluminium 8,1% og jern 5,0%. I den menneskelige krop er calcium (3,6 %), natrium (2,8 %), kalium (2,6 %) og magnesium (2,1 %) vigtige elektrolytter.
Selv et enkelt atom af et grundstof – såsom et guldatom – forbliver det samme grundstof, hvilket illustrerer begrebet elementær identitet på mikroskopisk niveau.
Hvorfor er det vigtigt at forstå isotoper
Selvom isotoper er kemisk identiske, udviser de unikke fysiske egenskaber. Denne forskel muliggør anvendelser lige fra medicinsk diagnostik (f.eks. ¹⁸F i PET-scanninger) til geologisk datering (f.eks. ²⁶Al). At anerkende isotopisk variation er afgørende for områder som miljøvidenskab, kernefysik og bioanalyse.
Samlet set udgør et klart greb om atomer, grundstoffer og isotoper grundlaget for kemi, fysik og de nye teknologier, der former vores verden.
 Varme artikler
Varme artikler
-
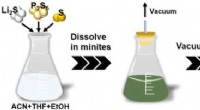 Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele
Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele -
 Magnetiske tænder afsløret ved hjælp af kvantebillederAcanthopleura hirtosa chiton radula. Den fulde radula består af 73 tænder med forskellige stadier af mineralisering. Billedet ovenfor viser tænderne før og efter starten af magnetitmineralisering. D
Magnetiske tænder afsløret ved hjælp af kvantebillederAcanthopleura hirtosa chiton radula. Den fulde radula består af 73 tænder med forskellige stadier af mineralisering. Billedet ovenfor viser tænderne før og efter starten af magnetitmineralisering. D -
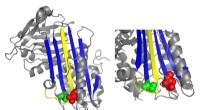 Hvad en sjælden blodsygdom kan lære os om blodpropperEt bånddiagram af antithrombin fremhæver placeringer af funktionelt vigtige mutationer. Kredit:Irene Martinez-Martinez Når en person kommer til skade, blodpropper er afgørende. Imidlertid, når far
Hvad en sjælden blodsygdom kan lære os om blodpropperEt bånddiagram af antithrombin fremhæver placeringer af funktionelt vigtige mutationer. Kredit:Irene Martinez-Martinez Når en person kommer til skade, blodpropper er afgørende. Imidlertid, når far -
 Supraballs tilbyder en ny måde at farve materialer påEt billede af en regnbuelignende blomster, malet med supraball blæk lavet af fem forskellige størrelser af kerne-skal syntetiske melanin nanopartikler. Kredit:Ming Xiao, Universitetet i Akron Et i
Supraballs tilbyder en ny måde at farve materialer påEt billede af en regnbuelignende blomster, malet med supraball blæk lavet af fem forskellige størrelser af kerne-skal syntetiske melanin nanopartikler. Kredit:Ming Xiao, Universitetet i Akron Et i
- Hvad ville der ske med en eukaryotisk celle, hvis den ikke havde kerne?
- Hvilke beviser overbeviste mange geologer om, at kontinenterne langsomt bevægede sig?
- Apple vil producere nye Mac Pro -computere i USA
- Europas Galileo -satellitter ramt af anomalier
- Forskere lærer at kontrollere elektronspin ved stuetemperatur for at gøre enheder mere effektive o…
- Hvad er biologiske aminer?


