Hvordan valenselektroner former et elements atomradius
Jupiterimages/Photos.com/Getty Images
Et grundstofs atomradius er afstanden fra kernen til de yderste (valens) elektroner. Denne radius skifter på forudsigelige måder hen over det periodiske system, drevet af samspillet mellem kernens positive ladning og de omgivende elektroner.
Energiniveauer og underskaller
Elektroner kredser om kernen i diskrete energiniveauer. Hvert niveau indeholder underskaller - s, p, d, f - der kan rumme et fast antal orbitaler og dermed et fast maksimalt antal elektroner. Når en underskal fyldes, skal yderligere elektroner optage orbitaler i det næste højere energiniveau. Jo højere energiniveauet er, jo længere sidder dens elektroner fra kernen.
Tendenser over en periode
Ved at bevæge sig fra venstre mod højre over en hovedgruppeperiode falder atomradius støt, mens antallet af valenselektroner stiger. Årsagen er en stigende nettokerneladning, der trækker de eksisterende valenselektroner tættere på, uden at tilføje et nyt energiniveau. Den lille afvigelse, der observeres i overgangsmetaller, stammer fra deres delvist fyldte d underskaller, som reducerer det effektive træk på ydre elektroner.
Afskærmning og effektiv nuklear ladning
Afskærmning opstår, når indre elektroner delvist neutraliserer kernens positive ladning. Den resterende "effektive" nukleare ladning er, hvad valenselektronerne føler. Over en periode forbliver antallet af indre elektroner konstant, mens kerneladningen stiger, så den effektive ladning vokser, strammer elektronskyen og krymper radius.
Trender ned i en gruppe
Nedstigende en gruppe optager valenselektronerne successivt højere energiniveauer. Selvom antallet af valens-elektroner forbliver det samme, skubber de ekstra skaller de ydre elektroner længere fra kernen. Det øgede antal protoner modsvares af den ekstra afskærmning fra indre elektroner, hvilket resulterer i en nettostigning i atomradius.
 Varme artikler
Varme artikler
-
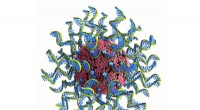 Ny maskinlæringsteknik analyserer hurtigt nanomedicin til kræftimmunterapiSNAer er kuglelignende former for DNA og RNA arrangeret på overfladen af en nanopartikel. Kredit:Chad Mirkin/Northwestern University Sfæriske nukleinsyrer er en klasse af personlig medicin til
Ny maskinlæringsteknik analyserer hurtigt nanomedicin til kræftimmunterapiSNAer er kuglelignende former for DNA og RNA arrangeret på overfladen af en nanopartikel. Kredit:Chad Mirkin/Northwestern University Sfæriske nukleinsyrer er en klasse af personlig medicin til -
 Billig, miljøvenlig katalysator åbner nye muligheder for organiske molekyler bygget af pyruvatPh.d.-studerende og førsteforfatter, Santanu Mondal, skitserer en reaktion af pyruvat ved at bruge en model af hans nydesignede organiske katalysatorsystem som reference. Kredit:OIST Kemikere ved O
Billig, miljøvenlig katalysator åbner nye muligheder for organiske molekyler bygget af pyruvatPh.d.-studerende og førsteforfatter, Santanu Mondal, skitserer en reaktion af pyruvat ved at bruge en model af hans nydesignede organiske katalysatorsystem som reference. Kredit:OIST Kemikere ved O -
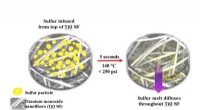 En stabiliserende påvirkning muliggør udvikling af lithium-svovlbatterierHot-press proceduren, udviklet hos Drexel, smelter svovl ind i nanofibermåtterne i et let tryksat, 140-graders celsius miljø - eliminerer behovet for tidskrævende behandling, der bruger en blanding af
En stabiliserende påvirkning muliggør udvikling af lithium-svovlbatterierHot-press proceduren, udviklet hos Drexel, smelter svovl ind i nanofibermåtterne i et let tryksat, 140-graders celsius miljø - eliminerer behovet for tidskrævende behandling, der bruger en blanding af -
 Forskere opdager, hvordan overflader kan have hjulpet tidligt liv på Jorden med at begyndeSpontant dannede protoceller, som ligner balloner forankret til en overflade af et netværk af reb, visualiseres ved 3D konfokal mikroskopi. Kredit:Irep Gözen På den tidlige jord, en række spontane
Forskere opdager, hvordan overflader kan have hjulpet tidligt liv på Jorden med at begyndeSpontant dannede protoceller, som ligner balloner forankret til en overflade af et netværk af reb, visualiseres ved 3D konfokal mikroskopi. Kredit:Irep Gözen På den tidlige jord, en række spontane
- Hvordan får du acceleration ved hjælp af et frit kropsdiagram?
- Hvad er nogle navne på naturlige indikatorer, og hvordan detekterer de syrebaser?
- Hvorfor er de fleste patogene mikroorganismer mesofiler?
- Hvis du skubber på en væg med kraft på 100 N, hvor hårdt gør du dig?
- Hvilke klasser af biologiske makromolekyler, som enzymer og stivelse tilhører?
- Hvad forskerne fandt efter at have sigtet gennem støv i solsystemet


