Sådan beregnes pH-værdien af en to-kemisk blanding nøjagtigt
Af Blake Flournoy | Opdateret 24. marts 2022
Billedkredit:StanislavSalamanov/iStock/GettyImages
pH er det logaritmiske mål for hydrogenionkoncentrationen i en opløsning, der spænder fra 0 til 14. For enkeltkomponentopløsninger er det ligetil at beregne pH. Når to syrer eller to baser kombineres, bliver beregningen lidt mere involveret, men den forbliver håndterbar med den rigtige tilgang.
TL;DR
Blanding af syrer eller baser producerer en neutraliseringsreaktion, der genererer salt (og nogle gange vand). Sådan finder du pH-værdien af en to-kemisk blanding:
- Bestem volumen og molariteten af hver komponent.
- Beregn det samlede antal mol H⁺ (for syrer) eller OH⁻ (for baser), der er indført i blandingen.
- Del den totale H⁺-koncentration med det samlede volumen af den blandede opløsning for at få [H⁺].
- Anvend pH=–log₁₀[H⁺].
Bær altid passende PPE, især ved håndtering af stærke syrer eller baser.
Forstå pH
pH kvantificerer koncentrationen af hydrogenioner i en opløsning. Mens udtrykket oftest er forbundet med væsker, er det lige så relevant for jord, geler og andre medier. Da pH er en logaritmisk skala, kan små ændringer i [H⁺] producere betydelige skift i surhedsgrad eller alkalinitet.
Komponentberegninger
Inden du kombinerer to syrer eller to baser, skal du indsamle følgende data for hver komponent:
- Volumen (i liter eller milliliter)
- Molaritet (molL⁻¹)
Brug disse oplysninger til at beregne antallet af mol hydrogenioner (for syrer) eller hydroxidioner (for baser), som hver opløsning bidrager med. Summen af disse mol repræsenterer det totale ionindhold i blandingen.
Blandede løsninger
Når det samlede antal mol H⁺ er kendt, er koncentrationen af hydrogenioner i den endelige blanding:
[H⁺]=(total molH⁺)/(samlet volumen i liter)
For eksempel, hvis to syrer giver henholdsvis 0,025 mol og 0,015 mol H⁺, og det kombinerede volumen er 200mL (0,200L), så:
[H⁺]=(0,025+0,015)mol/0,200L=0,0002molL⁻¹
Til sidst beregnes pH som:
pH=–log₁₀(0,0002)≈3,70
Gentag de analoge trin for base-base-blandinger ved at erstatte [OH⁻] og bruge relationen pH=14-pOH.
 Varme artikler
Varme artikler
-
 Ud af tyk luft:Omdannelse af kuldioxid til lysemitterende kulstofDette billede viser lysudsendelse, en proces kendt som fotoluminescens, danne fast kulstof, som er dannet på en sølv nanostruktur, oplyst af grønt lys. Kredit:University of Ottawa, OSA Optica Et t
Ud af tyk luft:Omdannelse af kuldioxid til lysemitterende kulstofDette billede viser lysudsendelse, en proces kendt som fotoluminescens, danne fast kulstof, som er dannet på en sølv nanostruktur, oplyst af grønt lys. Kredit:University of Ottawa, OSA Optica Et t -
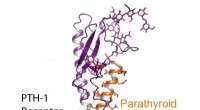 Fra receptorstruktur til nye osteoporoselægemidlerReceptoren er den vigtigste regulatoriske kontakt, der kontrollerer calciumfrigivelse fra knogler, og dermed et primært mål for udvikling af nye lægemidler til behandling af osteoporose. Receptoren be
Fra receptorstruktur til nye osteoporoselægemidlerReceptoren er den vigtigste regulatoriske kontakt, der kontrollerer calciumfrigivelse fra knogler, og dermed et primært mål for udvikling af nye lægemidler til behandling af osteoporose. Receptoren be -
 Ny undersøgelse hjælper med at karakterisere sammensmeltning af metallerEn prøve af Niob i mikroskopisk størrelse mellem to diamanter. Kredit:Asociación RUVID I de seneste år, en stor indsats er blevet afsat til undersøgelse af smeltningskurven for elementer ved højt
Ny undersøgelse hjælper med at karakterisere sammensmeltning af metallerEn prøve af Niob i mikroskopisk størrelse mellem to diamanter. Kredit:Asociación RUVID I de seneste år, en stor indsats er blevet afsat til undersøgelse af smeltningskurven for elementer ved højt -
 Datalagring ved hjælp af individuelle molekylerGrafisk animation af en mulig datahukommelse på atomskalaen:Et datalagringselement - bestående af kun 6 xenonatomer - flydende af en spændingspuls. Kredit:University of Basel, Institut for Fysik F
Datalagring ved hjælp af individuelle molekylerGrafisk animation af en mulig datahukommelse på atomskalaen:Et datalagringselement - bestående af kun 6 xenonatomer - flydende af en spændingspuls. Kredit:University of Basel, Institut for Fysik F


