Konvertering mellem mol, molaritet og volumen:en praktisk vejledning
Af William Hirsch
Opdateret 24. marts 2022
I kemi repræsenterer en muldvarp en bestemt mængde stof svarende til dens atommasse i gram. For eksempel indeholder et mol aluminium (atommasse ≈26,98g) 6,022×10²³ atomer, kendt som Avogadros tal. Molaritet (M) er koncentrationen af en opløsning udtrykt som mol opløst stof pr. liter opløsning.
Trin 1:Moles→Molaritet
For at finde molaritet skal du dividere antallet af mol med volumenet i liter.
Example: 10.0 mol in 5.0 L → 10.0 mol ÷ 5.0 L = 2.0 M
Trin 2:Molaritet→Moler
For at bestemme mol skal du gange molariteten med volumenet i liter.
Example: 3.0 M in 2.0 L → 3.0 mol/L × 2.0 L = 6.0 mol
Trin 3:Moles→Volume
For at beregne rumfanget af en opløsning skal du dividere molerne med molariteten.
Example: 6.0 mol at 3.0 M → 6.0 mol ÷ 3.0 mol/L = 2.0 L
Disse ligetil sammenhænge muliggør hurtige konverteringer i laboratorieberegninger og teoretisk arbejde.
 Varme artikler
Varme artikler
-
 Forskere optimerer additiv fremstilling på et molekylært niveauI en simulering, chromoxid-nanopartikler skaber bindinger med en vandbaseret diethylenglycolopløsning. Kredit:Adri van Duin Efterhånden som kompleksiteten og anvendelserne af additiv fremstilling
Forskere optimerer additiv fremstilling på et molekylært niveauI en simulering, chromoxid-nanopartikler skaber bindinger med en vandbaseret diethylenglycolopløsning. Kredit:Adri van Duin Efterhånden som kompleksiteten og anvendelserne af additiv fremstilling -
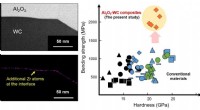 Brug af zirconium som tilsætningsstof i superstærke kompositmaterialerForskere ved Nagoya Universitet, arbejder i samarbejde med NGK Spark Plug Co., Ltd., har udviklet et sæt kompositmaterialer sammensat af lag af aluminiumoxid (Al2O3) og wolframcarbid (WC) med zirconiu
Brug af zirconium som tilsætningsstof i superstærke kompositmaterialerForskere ved Nagoya Universitet, arbejder i samarbejde med NGK Spark Plug Co., Ltd., har udviklet et sæt kompositmaterialer sammensat af lag af aluminiumoxid (Al2O3) og wolframcarbid (WC) med zirconiu -
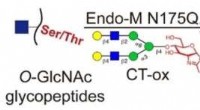 Reversibel kemoenzymatisk mærkningsstrategi muliggør dybdegående analyse af protein O-GlcNAcyleri…Kredit:Angewandte Chemie (2022). DOI:10.1002/ange.202117849 O-bundet β-N-acetylglucosamin (O-GlcNAcylation), en vigtig post-translationel modifikation (PTM) af proteiner, er involveret i forskellig
Reversibel kemoenzymatisk mærkningsstrategi muliggør dybdegående analyse af protein O-GlcNAcyleri…Kredit:Angewandte Chemie (2022). DOI:10.1002/ange.202117849 O-bundet β-N-acetylglucosamin (O-GlcNAcylation), en vigtig post-translationel modifikation (PTM) af proteiner, er involveret i forskellig -
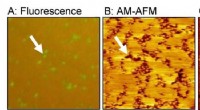 Samling af fluktuerende molekyler i kunstig cellemembranSe er lipiddobbeltlagsdomæner rige på polyethylenglycol (PEG)-modificeret lipid. (A) Fluorescensbillede, (B) amplitudemodulation (AM) AFM-topografi, og (C) frekvensmodulation (FM) AFM-topografi. Kredi
Samling af fluktuerende molekyler i kunstig cellemembranSe er lipiddobbeltlagsdomæner rige på polyethylenglycol (PEG)-modificeret lipid. (A) Fluorescensbillede, (B) amplitudemodulation (AM) AFM-topografi, og (C) frekvensmodulation (FM) AFM-topografi. Kredi


