Hvorfor visse stoffer modstår opløsning i vand:Nøgle videnskabelige principper
Af Claire Gillespie Opdateret 24. marts 2022
showcake/iStock/GettyImages
Vand kaldes ofte det "universelle opløsningsmiddel", fordi det kan opløse en lang række stoffer. Når et opløst stof helt opløses i et opløsningsmiddel, kaldes den resulterende homogene blanding en opløsning. På trods af vands bemærkelsesværdige solvens vil nogle materialer simpelthen ikke opløses i det.
TL;DR
Olie, paraffinvoks og sand er klassiske eksempler på stoffer, der forbliver uopløst i vand. Selv meget opløselige forbindelser når en mætningsgrænse, ud over hvilken yderligere opløst stof forbliver som fast rest.
Attraktive kræfter og opløselighed
Opløselighed afhænger af de relative styrker af tiltrækningskræfterne mellem opløste partikler, opløsningsmiddelpartikler og mellem opløst stof og opløsningsmiddel. Glucose opløses f.eks. let, fordi de hydrogen-bindingsinteraktioner med vand opvejer både glucose-glukose og vand-vand-interaktioner.
Blandbarhed vs. Ublandbarhed
Når to væsker blandes helt, er de blandbare; ellers er de ublandbare. Olie (kulbrinter) og vand er eksempler på ublandbarhed. Oliens lavere densitet får den til at flyde, og oliedråberne integreres aldrig i den vandige fase.
Polaritet betyder noget
Vands polaritet - delvis positiv ladning på brintatomer og delvis negativ ladning på ilt - gør det meget selektivt. Polære eller ioniske opløste stoffer tiltrækkes af vand, mens ikke-polære stoffer som paraffinvoks (lange kæder af C og H) afvises, idet de overholder reglen om "ligesom opløser ligesom".
Opløsning, erosion og suspension
Det er vigtigt at skelne opløsning fra erosion og suspension. Sand, for eksempel, opløses ikke, fordi vands indre attraktioner dominerer over vand-sand-interaktioner. Omrøring suspenderer sandet, hvilket giver en uklar blanding; når omrøringen stopper, sætter sandet sig, og vandet ovenover bliver klart. Langvarig vandkontakt kan erodere klippeoverflader og transportere fine partikler nedstrøms, men dette er en fysisk fjernelse snarere end kemisk opløsning.
Mætningsgrænser
Selv opløste stoffer, der er meget opløselige - såsom sukker eller natriumchlorid - udviser et mætningspunkt. Ved ligevægt er opløsningshastigheden lig med omkrystallisationshastigheden, så tilsætning af mere opløst stof øger ikke koncentrationen; i stedet forbliver overskud som uopløst fast stof.
Disse principper forklarer, hvorfor visse hverdagsmaterialer modstår opløsning i vand og understreger det nuancerede samspil mellem molekylære kræfter i vandig kemi.
 Varme artikler
Varme artikler
-
 Klæbende situation:Ny proces forvandler trærester til tapeIllustration, der repræsenterer transformationen af træer til tape. Ingeniører ved University of Delaware har udviklet en ny proces til at lave tape af en vigtig bestanddel af træer og planter kalde
Klæbende situation:Ny proces forvandler trærester til tapeIllustration, der repræsenterer transformationen af træer til tape. Ingeniører ved University of Delaware har udviklet en ny proces til at lave tape af en vigtig bestanddel af træer og planter kalde -
 Brug af vandmolekyler til at aflæse elektrisk aktivitet i lipidmembranerEPFL-forskere var i stand til i realtid at kortlægge, hvordan ladninger transporteres over og langs membraner, blot ved at observere adfærden af tilstødende vandmolekyler. Kredit:Jamani Caillet/EPFL
Brug af vandmolekyler til at aflæse elektrisk aktivitet i lipidmembranerEPFL-forskere var i stand til i realtid at kortlægge, hvordan ladninger transporteres over og langs membraner, blot ved at observere adfærden af tilstødende vandmolekyler. Kredit:Jamani Caillet/EPFL -
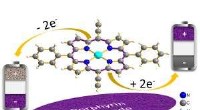 Naturligt molekyle til at øge ydeevnen af elektroder til genopladelige batterierPorphyrinmolekylet – brugt i elektroder – fremskynder opladningsprocessen af batterier i laboratoriet. Kredit:KIT/HIU Klorofyl, blod, og vitamin B12 er alle baseret på porfyrinmolekylet. Men por
Naturligt molekyle til at øge ydeevnen af elektroder til genopladelige batterierPorphyrinmolekylet – brugt i elektroder – fremskynder opladningsprocessen af batterier i laboratoriet. Kredit:KIT/HIU Klorofyl, blod, og vitamin B12 er alle baseret på porfyrinmolekylet. Men por -
 Sådan befris fangede radikaler fra carboxylFigur:Frie radikaler, Abekongen er bundet af carboxylgruppens store bjerg. De almindelige fotokatalytiske systemer er komplekse og dyre. Den nye katalysator bruger en ny mekanisme til at kombinere den
Sådan befris fangede radikaler fra carboxylFigur:Frie radikaler, Abekongen er bundet af carboxylgruppens store bjerg. De almindelige fotokatalytiske systemer er komplekse og dyre. Den nye katalysator bruger en ny mekanisme til at kombinere den
- Hvor meget varme producerer en pejs?
- Hvad er det videnskabelige navn eller taksonomiske klassificering af årlige blomster impatiens?
- Webb-teleskopet tager betagende billeder af Oriontågen
- Hvor sjældne er dobbelte regnbuer?
- Forskere identificerer molekylær motor, der transformerer kromosomer
- Hvad er formlen for carbontetrachlorid og det ionisk eller kovalent?


