Hvordan atomer kombineres:Fra ioniske gitter til kovalente molekyler
Af Chris Deziel Opdateret 24. marts 2022
Creativeye99/iStock/GettyImages
Det periodiske system katalogiserer alle kendte grundstoffer, hver defineret af et atoms kerne - sammensat af protoner og neutroner - og dets omgivende elektroner. Når atomer interagerer, omarrangerer de deres ydre skalelektroner for at opnå en mere stabil konfiguration. Denne omlejring giver anledning til ioniske strukturer eller kovalente molekyler - som begge danner byggestenene i forbindelser, der driver kemien i vores univers.
TL;DR
Atomer slutter sig til enten ioniske gitter eller kovalente bindinger og danner forbindelser, der spænder fra simple salte til komplekse organiske molekyler.
Hvordan atomer kombineres
Atomer søger en stabil "oktet" (otte elektroner) i deres yderste skal – bortset fra den første skal, som kun kan rumme to. Et atom, der har nogle få ledige pletter, vil forsøge at få eller dele elektroner for at fylde dem, mens et atom, der bærer et par ekstra elektroner, ofte vil miste dem. Ædelgasser (helium, neon, argon osv.) har allerede en fuld ydre skal, så de forbliver inerte og danner ikke forbindelser med hinanden eller med andre grundstoffer.
Ioniske forbindelser :Et atom, der har en enkelt valenselektron, vil donere det til en partner, der har brug for en. Donoren bliver en positivt ladet ion, modtageren en negativt ladet ion, og elektrostatisk tiltrækning trækker dem ind i et krystallinsk gitter. Dette er ikke et diskret molekyle, men en forbindelse, som eksemplificeret ved almindeligt bordsalt, natriumchlorid (NaCl). Få mere at vide om ionbinding .
Kovalent binding :Atomer med en til fire ekstra eller manglende valenselektroner deler elektronpar for at fuldende deres oktetter. Disse delte par danner stærke kovalente bindinger, og de resulterende strukturer er typisk molekyler. Vand (H2O), dannet når et oxygenatom deler et elektronpar med hver af to hydrogenatomer, er et klassisk eksempel. Kovalente molekyler udviser ofte lavere smelte- og kogepunkter end ioniske modstykker. Udforsk kovalente bindinger .
Metaller har en tendens til at miste elektroner og danner ioner, der samles i faste gitter, hvorimod ikke-metaller normalt danner kovalente molekyler, der er gasser eller væsker ved stuetemperatur.
Hvornår er et molekyle en forbindelse?
Alle uorganiske og organiske molekyler sammensat af mere end ét grundstof kvalificeres som forbindelser. Eksempler omfatter hydrogenchlorid (HCl), methan (CH4), carbondioxid (CO2) og det komplekse sukkersaccharose (C12H22011). Kulstof med fire valenselektroner balancerer unikt donerende og accepterende elektroner, hvilket gør det til rygraden i organisk kemi.
I modsætning hertil er molekyler, der udelukkende består af et grundstof – såsom nitrogengas (N₂), oxygengas (O₂) eller ozon (O₃) – ikke forbindelser, fordi de kun involverer et enkelt element. De er dog stadig distinkte molekylære enheder.
Se NIST Atomic Spectra Database for at få dybere indsigt i det periodiske system og elementinteraktioner. og Wikipedia-posten i det periodiske system .
Til visuel reference er her en skildring af, hvordan vandmolekyler bindes via kovalente interaktioner:Vandmolekyleillustration .
Sidste artikelBeregning af molbrøk:En trin-for-trin guide
Næste artikelHvilken gas giver den lilla glød i neonskilte?
 Varme artikler
Varme artikler
-
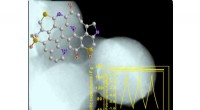 Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba
Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba -
 Lysfølsomt øverste lag af plastikfilm fremkalder bevægelseSkematisk af filmen (til venstre):Filmen er for det meste sammensat af en ikke-fotoresponsiv polymer (200 - 400 nm tyk), og et fotoresponsivt polymerlag eksisterer kun ved overfladen (nogle nm tykt).
Lysfølsomt øverste lag af plastikfilm fremkalder bevægelseSkematisk af filmen (til venstre):Filmen er for det meste sammensat af en ikke-fotoresponsiv polymer (200 - 400 nm tyk), og et fotoresponsivt polymerlag eksisterer kun ved overfladen (nogle nm tykt). -
 Video:Vampyrfolklore har mere kemi, end du trorKredit:The American Chemical Society Halloween -sæsonen ville ikke være den samme uden de udøde. Denne uge om reaktioner, vi pakker den kemi ud, der måske har inspireret en af vores favoritter:
Video:Vampyrfolklore har mere kemi, end du trorKredit:The American Chemical Society Halloween -sæsonen ville ikke være den samme uden de udøde. Denne uge om reaktioner, vi pakker den kemi ud, der måske har inspireret en af vores favoritter: -
 Brug af metaller til brændstofKredit:Pixabay/CC0 Public Domain Vidste du, at vi inden for mikrotyngdekraft forbereder et af de mest lovende brændstoffer til fremtiden? Mikrotyngdekraft hjælper med at finde svar og modeller ti
Brug af metaller til brændstofKredit:Pixabay/CC0 Public Domain Vidste du, at vi inden for mikrotyngdekraft forbereder et af de mest lovende brændstoffer til fremtiden? Mikrotyngdekraft hjælper med at finde svar og modeller ti
- Hvorfor begyndte astronomer at søge efter en planet X?
- Hvad hedder Compound Nano2 2H2O?
- EU skal øge udgifterne i rummet eller presses ud:eksperter
- Hvordan kønsnormer påvirker, hvad unge vælger at læse i skolen
- 3D-trykte vejrstationer kunne muliggøre mere videnskab for færre penge
- NASA forestiller sig et katastrofalt nedslag af asteroide for at studere, hvordan det forhindres


