Hvordan man beregner mol og bestemmer molaritet i løsninger
Af bidragyder Opdateret 24. marts 2022
I kemi tilsættes et opløst stof ofte til en opløsning. En af de mest almindelige opgaver er at bestemme koncentrationen af det opløste stof, udtrykt som opløsningens molaritet.
Trin 1
Lær kerneligningen:M =mol opløst stof ÷ liter opløsning . Symbolet "M" repræsenterer molariteten, dvs. antallet af mol opløst stof pr. liter opløsning.
Trin 2
Konverter massen af det opløste stof til mol. Brug et periodisk system til at finde den molære masse af forbindelsen. For eksempel har natriumchlorid (NaCl) en molær masse på 58,5 gmol-1 (23 g for Na + 35,5 g for Cl). Hvis du opløser 24 g NaCl, er antallet af mol 24 g ÷ 58,5 gmol⁻¹≈0,41mol.
Trin 3
Mål det samlede volumen af opløsningen. Volumenet skal udtrykkes i liter til molaritetsberegningen. I dette eksempel er 650mL opløsning lig med 0,65L.
Trin 4
Beregn molariteten:M =0,41mol ÷ 0,65L ≈ 0,63M (afrundet til to decimaler).
Væsentlige værktøjer
- Videnskabelig lommeregner
- Nøjagtigt periodisk system
TL;DR
Molaritet er mol opløst stof pr. liter opløsning. Konverter gram til mol ved hjælp af den korrekte molære masse, og divider derefter med opløsningsvolumenet i liter.
Vigtig bemærkning
Omregn altid milliliter til liter, før du udfører opdelingen.
 Varme artikler
Varme artikler
-
 Forskere gør ananasaffald til aerogeler af høj værdiFormosa ananas i Filippinerne. Næsten tre gange så meget ananasbladaffald genereres for hvert kilo produceret frugt. Kredit:Judgefloro Høst af ananas, en udbredt tropisk frugt, efterlader tonsvis
Forskere gør ananasaffald til aerogeler af høj værdiFormosa ananas i Filippinerne. Næsten tre gange så meget ananasbladaffald genereres for hvert kilo produceret frugt. Kredit:Judgefloro Høst af ananas, en udbredt tropisk frugt, efterlader tonsvis -
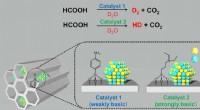 Nanokatalysator gør tungt arbejde af myresyreKontrolleret frigivelse af hydrogenisotopforbindelser fra dehydrogeneringen af myresyre i D 2 O af PdAg-legeringens nanopartikler understøttet på aminfunktionaliseret silica. Kredit:Osaka Universi
Nanokatalysator gør tungt arbejde af myresyreKontrolleret frigivelse af hydrogenisotopforbindelser fra dehydrogeneringen af myresyre i D 2 O af PdAg-legeringens nanopartikler understøttet på aminfunktionaliseret silica. Kredit:Osaka Universi -
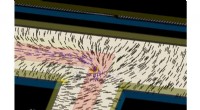 Aktive flydende krystalsystemer undersøgt i jagten på autonome materialesystemerSimuleringsøjebliksbillede af en selvkørende topologisk defekt i en aktiv flydende krystal styret af et lysmønster (skinnede i lyserødt område). Kredit:Prof. Zhang Rui, HKUST Liquid Crystals (LC)
Aktive flydende krystalsystemer undersøgt i jagten på autonome materialesystemerSimuleringsøjebliksbillede af en selvkørende topologisk defekt i en aktiv flydende krystal styret af et lysmønster (skinnede i lyserødt område). Kredit:Prof. Zhang Rui, HKUST Liquid Crystals (LC) -
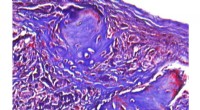 Nye hydrogeler viser lovende behandling af knogledefekterDer er vist et mikroskopisk billede af regenereret knogle i en kraniedefekt hos en mus. Kredit:University of California, Los Angeles Bioingeniører og tandlæger fra UCLA School of Dentistry har udv
Nye hydrogeler viser lovende behandling af knogledefekterDer er vist et mikroskopisk billede af regenereret knogle i en kraniedefekt hos en mus. Kredit:University of California, Los Angeles Bioingeniører og tandlæger fra UCLA School of Dentistry har udv


