Hvordan NaOH-koncentration i vand påvirker hydroxidioner, pH, neutralisering og buffering
Af John Brennan
Opdateret 24. marts 2022
Natriumhydroxid (NaOH), almindeligvis kendt som lud, er en stærk base, der er meget udbredt i laboratorier, industri og byggeri. Når dens koncentration i vand stiger, ændres flere vigtige kemiske egenskaber. De følgende afsnit forklarer disse effekter i detaljer.
Hydroxidioner
Ved opløsning dissocieres NaOH fuldstændigt til natriumioner (Na⁺) og hydroxidioner (OH⁻). Når NaOH-koncentrationen stiger, vokser tætheden af OH⁻ i opløsningen proportionalt, hvilket direkte øger opløsningens basicitet.
pH
Rent vand gennemgår autoprotolyse, og balancerer H₃O⁺- og OH⁻-koncentrationerne for at give en neutral pH-værdi på 7. Tilsætning af NaOH introducerer overskydende OH⁻, som accepterer protoner fra H₃O⁺, hvilket flytter ligevægten mod vanddannelse. Denne reduktion i H₃O⁺-koncentration driver pH opad, hvilket gør opløsningen mere basisk. Forholdet er logaritmisk, så trinvise stigninger i NaOH giver større pH-ændringer ved lavere koncentrationer.
Neutralisering
NaOH neutraliserer let syrer. Hydroxidionen accepterer en proton fra en syre og danner vand (H2O) og syrens konjugerede base. I praksis reducerer tilsætning af NaOH til en sur opløsning surhedsgraden, indtil reaktionen når støkiometrisk ækvivalens, hvor pH nærmer sig neutral eller let basisk, afhængigt af syrens styrke og mængde.
Buffering
Mens stærke baser ikke er klassiske buffere, kan koncentrerede NaOH-opløsninger absorbere små mængder tilsat syre uden dramatiske pH-skift. Fordi pH-skalaen er logaritmisk, betyder en høj OH⁻-koncentration, at hver trinvis protonneutralisering ændrer pH mindre mærkbart og effektivt fungerer som en basisk buffer.
At forstå disse sammenhænge er afgørende for præcis pH-kontrol i kemiske processer, sikkerhedsprotokoller og industrielle applikationer.
 Varme artikler
Varme artikler
-
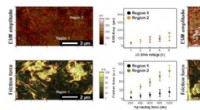 Visualisering af funktionelle komponenter for at karakterisere optimale kompositelektroderAFM -billeder af (a, c) prøver A og (b, d) B. (a, b) Topografiske højdebilleder og (c, d) friktionskraftbilleder, henholdsvis. Alle billeder blev optaget med en spidsbelastningskraft på 400 nN. Røde l
Visualisering af funktionelle komponenter for at karakterisere optimale kompositelektroderAFM -billeder af (a, c) prøver A og (b, d) B. (a, b) Topografiske højdebilleder og (c, d) friktionskraftbilleder, henholdsvis. Alle billeder blev optaget med en spidsbelastningskraft på 400 nN. Røde l -
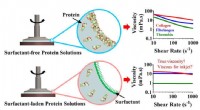 Fundning af fibrøst protein kan føre til forbedret bioprintning, vævsteknikKollagen og fibrinogen i vandige opløsninger danner et fast lag på overfladen af vand, ødelægger målinger af flowadfærd med rotationsreometere. Tilsætning af et ikke-ionisk overfladeaktivt stof i sm
Fundning af fibrøst protein kan føre til forbedret bioprintning, vævsteknikKollagen og fibrinogen i vandige opløsninger danner et fast lag på overfladen af vand, ødelægger målinger af flowadfærd med rotationsreometere. Tilsætning af et ikke-ionisk overfladeaktivt stof i sm -
 Smugler effektivt medicin ind i cellerFluorescerende bløde perler, der passerer gennem de indsnævrede kanaler i en biochip. Kredit:MPZPM, Salvatore Girardo En ny, patenteret metode kaldet Progressive Mechanoporation gør det muligt mek
Smugler effektivt medicin ind i cellerFluorescerende bløde perler, der passerer gennem de indsnævrede kanaler i en biochip. Kredit:MPZPM, Salvatore Girardo En ny, patenteret metode kaldet Progressive Mechanoporation gør det muligt mek -
 Teoretisk forudsigelse af omvendt intersystemkrydsning for organiske halvledereKredit:CC0 Public Domain Et fælles forskerhold ved RIKEN og Hokkaido University udviklede en metode til at forudsige hastighedskonstanter for reverse intersystem crossing (RISC) forbundet med lyse
Teoretisk forudsigelse af omvendt intersystemkrydsning for organiske halvledereKredit:CC0 Public Domain Et fælles forskerhold ved RIKEN og Hokkaido University udviklede en metode til at forudsige hastighedskonstanter for reverse intersystem crossing (RISC) forbundet med lyse
- Er Ubers bilservice virkelig 40 milliarder dollar værd?
- Fysikere demonstrerer ny måde at krænke lokal kausalitet
- Ny elektrokemisk biosensor til tidlig kræftpåvisning
- Hvor mange elektroner er der i det højeste besatte energiniveau atom barium?
- Ny tidsopløst ultraviolet fotodissociationsmassespektrometristrategi til målproteinstabilitetsanal…
- Hvad er laget af jord, der indeholder mest humus og mindre sten?


