Hvilke faktorer påvirker et stofs smeltepunkt
Af Claire Gillespie – Opdateret 24. marts 2022
Smeltepunkt er den temperatur, hvor et fast stof bliver til en væske. I en reversibel faseændring er smeltepunktet for et rent stof lig med dets frysepunkt - den temperatur, hvorved det størkner. For eksempel smelter is ved 0°C (32°F) og fryser ved samme temperatur og bliver tilbage til fast vand. At bestemme et stofs smeltepunkt er en pålidelig måde at bekræfte dets identitet på, fordi det er svært at opvarme faste stoffer langt ud over deres iboende smeltetærskler.
TL;DR
Tre nøglefaktorer former et smeltepunkt:molekylær sammensætning, styrken af intermolekylære kræfter og tilstedeværelsen af urenheder.
1. Molekylær sammensætning
Når molekyler pakker tæt og symmetrisk, modstår materialet smeltning. Symmetrisk neopentan har for eksempel et højere smeltepunkt end dets forgrenede isopentan-modstykke, fordi dets molekyler passer tættere sammen. Størrelsen betyder også noget:mindre molekyler kræver mindre termisk energi for at forstyrre deres arrangement. Ethanol (C₂H6O) smelter ved –114,1°C (–173,4°F), hvorimod den mere voluminøse polymer ethylcellulose smelter ved 151°C (303,8°F). Kæmpe kovalente netværk såsom diamant, grafit og silica indeholder hundredvis af stærke kovalente bindinger, der skal brydes før smeltning, hvilket giver dem usædvanligt høje smeltepunkter.
2. Intermolekylære kræfter
Stærke tiltrækninger mellem molekyler hæver smeltepunktet. Ioniske forbindelser udviser høje smeltepunkter på grund af kraftige elektrostatiske ion-ion-interaktioner. I organisk kemi hæver polaritet og hydrogenbinding smeltepunkter yderligere. For eksempel smelter det polære molekyle jodmonochlorid ved 27°C (80,6°F), mens det ikke-polære brom smelter ved –7,2°C (19,0°F). Jo større polaritet eller hydrogenbindingsevne er, jo mere energi er der brug for for at adskille molekylerne.
3. Urenheder og smeltepunktsdepression
Rene faste stoffer har et smalt, skarpt smelteområde - typisk 1-2°C - fordi deres molekyler er ensartet pakket. Enhver urenhed introducerer strukturelle defekter, der svækker intermolekylær kohæsion, hvilket fører til en lavere smeltetemperatur og et bredere smelteområde. Dette fænomen, kendt som smeltepunktsdepression, er en klassisk indikator for prøvens renhed. For eksempel vil en krystallinsk organisk forbindelse, der er et enkelt, velordnet molekyle, smelte ved en bestemt temperatur, hvorimod en blanding af to forskellige organiske molekyler vil smelte over et bredere område, fordi de ikke kan passe perfekt sammen.
 Varme artikler
Varme artikler
-
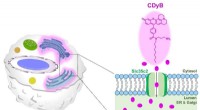 En enklere måde at differentiere B-celler og T-celler påDen foreslåede farvningsmekanisme af CDyB. Kredit:Institut for Grundvidenskab Vores immunsystem er afgørende for vores overlevelse, da vores kroppe konstant bliver udsat for bakterier, vira, parasi
En enklere måde at differentiere B-celler og T-celler påDen foreslåede farvningsmekanisme af CDyB. Kredit:Institut for Grundvidenskab Vores immunsystem er afgørende for vores overlevelse, da vores kroppe konstant bliver udsat for bakterier, vira, parasi -
 DNA -enzymer kunne udkonkurrere proteinenzymer til genteknologiKemiprofessor Yi Lu ledede et team, der udviklede en teknik, der tillader DNA-enzymer at skære dobbeltstrenget DNA, muliggøre en bred vifte af gentekniske applikationer. Kredit:L. Brian Stauffer F
DNA -enzymer kunne udkonkurrere proteinenzymer til genteknologiKemiprofessor Yi Lu ledede et team, der udviklede en teknik, der tillader DNA-enzymer at skære dobbeltstrenget DNA, muliggøre en bred vifte af gentekniske applikationer. Kredit:L. Brian Stauffer F -
 Mekanisme af Cl-initieret oxidation af methacrolein under NOx-frie forholdFig. 1. Fotoioniseringsmassespektre erhvervet (a) uden O2 og (b) tilføjelse af O2 ind i hurtigstrømsrøret. Kredit:Lin Xiaoxiao Kloratomer (Cl) er mere reaktive i atmosfæren end andre oxidanter. I d
Mekanisme af Cl-initieret oxidation af methacrolein under NOx-frie forholdFig. 1. Fotoioniseringsmassespektre erhvervet (a) uden O2 og (b) tilføjelse af O2 ind i hurtigstrømsrøret. Kredit:Lin Xiaoxiao Kloratomer (Cl) er mere reaktive i atmosfæren end andre oxidanter. I d -
 Nyt upcycling-system til kommercielle polyestereForskere har udviklet en one-shot-proces til at omdanne almindeligt tilgængelige polymere plastik, såsom polyestere, til meget funktionelle materialer kaldet vitrimerer, der let kan genanvendes til ny
Nyt upcycling-system til kommercielle polyestereForskere har udviklet en one-shot-proces til at omdanne almindeligt tilgængelige polymere plastik, såsom polyestere, til meget funktionelle materialer kaldet vitrimerer, der let kan genanvendes til ny


