Oxygen vs. Oxygen Gas:Nøgleforskelle og deres indvirkning
Af Doug Leenhouts
Opdateret 24. marts 2022
Ilt er et grundstof, der kan eksistere som et fast stof, væske eller gas afhængigt af temperatur og tryk. I atmosfæren findes det som en gas, specifikt et diatomisk molekyle (O₂). Både de elementære iltatomer og iltgas er reaktive stoffer, der er nødvendige for livet på Jorden.
Oxygengas (O₂)
Iltgas eller dioxygen er det næstmest udbredte grundstof i Jordens atmosfære og udgør 21 % af den luft, vi indånder, efter nitrogen på 78 %. Ren ilt har en vægtfylde på 1,105, hvilket betyder, at det ville synke i forhold til resten af atmosfæren, hvis det ikke var for vind eller konvektion. ligas.com
Reaktivitet
Iltgas reagerer med stort set alle grundstoffer undtagen ædelgasserne og danner oxider. For metaller som magnesium sker oxidation ved standard temperaturer og tryk, mens tungere grundstoffer kræver forhøjede temperaturer og tryk for at inducere oxidation. Ilt er afgørende for forbrændingen, selvom gassen i sig selv er ikke-brændbar. Mange industrielle varmebehandlingsprocesser er afhængige af ilt på flaske for at hæve forbrændingstemperaturerne.
Overflod
Vand er ca. 85% oxygen i massen, på trods af dets H2O-formel. Den menneskelige krop består af omkring 60 % ilt, hvilket er grunden til, at astronomer betragter atmosfærisk ilt som en potentiel biosignatur. Oxider tegner sig for omkring 46% af jordskorpen. I atmosfæren findes oxygen som diatomisk O₂ og som den allotrope ozon (O₃). Ozonlaget er kun ~3 mm tykt, og dets nedbrydning forværres af chlorfluorcarbon-emissioner.
Egenskaber
Iltgas er farveløs, lugtfri og smagløs; ozon og flydende ilt har en lyseblå nuance. Ozons kogepunkt er 161,3K versus O₂s 90,2K; dens smeltepunkt er 80,7 K sammenlignet med O₂'s 54,36 K. Ozon er tættere (2,144gL⁻1) end O₂ (1,429gL⁻1). Mens ilt er afgørende for respiration og stofskifte, er ozon en potent oxidator og giftig i høje koncentrationer.
 Varme artikler
Varme artikler
-
 Skaber ringe i naturlig antibiotikasynteseTværfaglige undersøgelser afslører, hvordan naturen skaber et globalt brugt antibiotikum. Kredit:University of Bristol Forskere ved University of Bristol har afsløret hemmelighederne bag nøglering
Skaber ringe i naturlig antibiotikasynteseTværfaglige undersøgelser afslører, hvordan naturen skaber et globalt brugt antibiotikum. Kredit:University of Bristol Forskere ved University of Bristol har afsløret hemmelighederne bag nøglering -
 Atomindstilling på kobolt muliggør en ottedobbelt stigning i hydrogenperoxidproduktionen3D-billede af enkelte koboltatomer på nitrogendoperet grafen. Det var afgørende for denne undersøgelse at kontrollere koordineringsmiljøet for et enkelt koboltatom, da denne koordineringsstruktur dire
Atomindstilling på kobolt muliggør en ottedobbelt stigning i hydrogenperoxidproduktionen3D-billede af enkelte koboltatomer på nitrogendoperet grafen. Det var afgørende for denne undersøgelse at kontrollere koordineringsmiljøet for et enkelt koboltatom, da denne koordineringsstruktur dire -
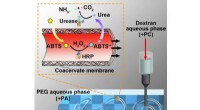 Materialeforskere bygger et syntetisk system med rum som rigtige cellerUMass Amherst materialeforsker Thomas Russell og andre beskriver i et nyt papir, hvordan de drager fordel af forskelle i elektrisk ladning til at skabe en alt vandig, vand-i-vand-konstruktion, der opn
Materialeforskere bygger et syntetisk system med rum som rigtige cellerUMass Amherst materialeforsker Thomas Russell og andre beskriver i et nyt papir, hvordan de drager fordel af forskelle i elektrisk ladning til at skabe en alt vandig, vand-i-vand-konstruktion, der opn -
 Prisbillig og mobil rensning af dialysevandI dag, Hæmodialyse er ofte centerbaseret og griber dybt ind i patienternes hverdag. Ved hjælp af mobile vandkilder, vi kunne tage et skridt mod højere mobilitet. Kredit:Fraunhofer IZI/Dr. Rainer Golda
Prisbillig og mobil rensning af dialysevandI dag, Hæmodialyse er ofte centerbaseret og griber dybt ind i patienternes hverdag. Ved hjælp af mobile vandkilder, vi kunne tage et skridt mod højere mobilitet. Kredit:Fraunhofer IZI/Dr. Rainer Golda
- Hvordan overføres energi fra solstråler til en autotrof og derefter en heterotrof?
- Undersøgelse viser atomlagsaflejringsvej til skalerbare, elektroniske van der Waals tellur tynde fi…
- Bioinspirerede materialer fra mælkebøtter
- Territorial forvaltning og styring af den colombianske Amazonas af oprindelige folk
- Strækbare grafentransistorer overvinder begrænsninger af andre materialer
- Kreative industrier kan være nøglen til økonomisk velstand i kyst- og landdistrikter


