Forstå pH-værdien af natriumcarbonatopløsninger i vand
Af Jack Brubaker
Opdateret 24. marts 2022
Vand
Vand (H2 O) gennemgår autodissociation, en selvioniseringsproces, der opdeler det i hydrogenioner (H + ) og hydroxidioner (OH - ):
H2 O → H + + OH -
pH
pH-skalaen kvantificerer koncentrationen af H + i en opløsning, der går fra 0 til 14. En pH>7 angiver en alkalisk (basisk) opløsning, <7 angiver surhedsgrad, og 7 repræsenterer neutralitet.
Natriumcarbonat
Natriumcarbonat (Na2 CO3 ), almindeligvis kendt som vaskesodavand, dissocieres i vand for at frigive natriumioner (Na + ) og carbonationer (CO3 2- ):
Na2 CO3 → 2 Na + + CO3 2-
Na + ioner er tilskuerioner og påvirker ikke pH. I modsætning hertil CO3 2- reagerer med vand, genererer hydroxidioner og hæver derved opløsningens pH:
CO3 2- + H2 O → HCO3 - + OH -
Koncentration og pH
pH er direkte proportional med koncentrationen af opløst natriumcarbonat. For eksempel ved at tilføje to spiseskefulde Na2 CO3 til et glas vand giver en højere pH end tilsætning af en spiseskefuld, fordi den større ionstyrke øger OH - koncentration.
Blandevejledning
Videnskabelige målinger bekræfter følgende pH-værdier for standardiserede opløsninger:
- 1 g (0,035 oz) Na2 CO3 opløst og fortyndet til 1L (≈1 quart) → pH=11,37
- 5 g (0,18 oz) Na2 CO3 opløst og fortyndet til 1L (≈1 quart) → pH=11,58
- 10 g (0,35 oz) Na2 CO3 opløst og fortyndet til 1L (≈1 quart) → pH=11,70
 Varme artikler
Varme artikler
-
 Gør trærester til smarte hydrogelerHvordan bio-hydrogeler reagerer på eksterne stimuli og i sidste ende kan nedbrydes i miljøet. Kredit:North Carolina State University NC -statens forskere gør træbiprodukter til sensoriske hydrogel
Gør trærester til smarte hydrogelerHvordan bio-hydrogeler reagerer på eksterne stimuli og i sidste ende kan nedbrydes i miljøet. Kredit:North Carolina State University NC -statens forskere gør træbiprodukter til sensoriske hydrogel -
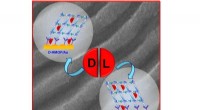 Forskere udvikler superfølsomme sensorer til spejlmolekyler i medicinKredit:Tomsk Polytechnic University (TPU) Forskere fra Tomsk Polytechnic University har sammen med kolleger fra Tjekkiet udviklet superfølsomme sensorer til påvisning af enantiomerer, kendt som sp
Forskere udvikler superfølsomme sensorer til spejlmolekyler i medicinKredit:Tomsk Polytechnic University (TPU) Forskere fra Tomsk Polytechnic University har sammen med kolleger fra Tjekkiet udviklet superfølsomme sensorer til påvisning af enantiomerer, kendt som sp -
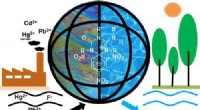 Let syntetiseret forbindelse fundet at være nyttig til at fjerne fluorid og metalioner fra drikkeva…Kredit:ACS (Phys.org) – Et par forskere ved Indian Institute of Science Education and Research Kolkata har fundet ud af, at en let syntetiseret forbindelse kan bruges til at fjerne fluorid og meta
Let syntetiseret forbindelse fundet at være nyttig til at fjerne fluorid og metalioner fra drikkeva…Kredit:ACS (Phys.org) – Et par forskere ved Indian Institute of Science Education and Research Kolkata har fundet ud af, at en let syntetiseret forbindelse kan bruges til at fjerne fluorid og meta -
 Selv efter håndvask, ny fngerprint test kan skelne mellem dem, der har taget eller håndteret heroi…Kredit:CC0 Public Domain En avanceret fingeraftryksdetektionsteknologi kan identificere spor af heroin på menneskelig hud, selv efter at nogen har vasket deres hænder – og det er også smart nok at
Selv efter håndvask, ny fngerprint test kan skelne mellem dem, der har taget eller håndteret heroi…Kredit:CC0 Public Domain En avanceret fingeraftryksdetektionsteknologi kan identificere spor af heroin på menneskelig hud, selv efter at nogen har vasket deres hænder – og det er også smart nok at
- Hvad skal kernekraftværker med energi?
- Hovedenergieniveau 1 af et atom indeholder elektron med den laveste hvorfor?
- Er det muligt for en krop at have en acceleration, når man bevæger sig med konstant hastighed?
- Hvad er komparativ genomik, der bruges til?
- NASA udvælger forslag til at demonstrere smallSat-teknologier til at studere interplanetarisk rum
- Hvad er den organisme, der ikke kan fremstille sin egen mad og skal fodre med andre organismer til e…


