Konverter atomer til gram med en lommeregner:en praktisk vejledning
Af Riti Gupta | Opdateret 24. marts 2022
At tælle individuelle atomer er umuligt med en balance, så kemikere bruger Avogadros tal til at forbinde den mikroskopiske verden med makroskopiske målinger.
conejota/iStock/GettyImages
Avogadros nummer:Broen mellem atomer og muldvarpe
Avogadros tal er 6,022×10²³, mængden af partikler i en mol (mol). Et mol kan være en samling af atomer, molekyler eller ioner, afhængigt af stoffet.
Hvad er massen af en muldvarp?
Massen af en muldvarp – dens molære masse — udtrykkes i gram pr. mol (gmol⁻¹). Du finder det direkte i det periodiske system (f.eks. klor:35,45 gmol⁻¹). For forbindelser summeres atommasserne af alle indgående atomer (vand:2×1,008+15,999=18,02gmol⁻¹).
Fra atomer til gram:konverteringsprocessen
Sådan konverteres et givet antal atomer til gram:
- Konverter atomer til mol:divider med Avogadros tal.
- Multipér de resulterende mol med molmassen.
Eksempel:3×10²⁴ atomer af klor
3×10²⁴atomerCl ÷ 6,022×10²³atomsmol⁻¹=4,98molCl
4,98 molCl × 35,45 gmol-¹=176,6 gCl
Således vejer 3×10²⁴ kloratomer 176,6 gram.
Håndtering af forbindelser:Atomer i et molekyle
Hvis du kun kender atomtallet for et grundstof, der forekommer i en forbindelse, skal du først bestemme, hvor mange molekyler af den forbindelse du har, ved at bruge forholdet atom til molekyle.
Eksempel:5,55×10²³ iltatomer i CO₂
5,55×10²³atomerO ÷ 2atomerOmol₂=2,78×10²³molekylerCO₂
2,78×10²³molekylerCO₂ ÷ 6,022×10²³molekylermol⁻¹=0,462molCO₂
0,462 molCO₂ × 44,01 gmol⁻1=20,3 gCO₂
Hold altid styr på dine enheder ved hvert trin for at undgå fejl.
Referencer: IUPAC Green Book, iupac.org ; Det periodiske system, PubChem .
 Varme artikler
Varme artikler
-
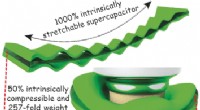 Super strækbar, superkomprimerbare superkondensatorerFleksibel, bærbar elektronik kræver lige så fleksibel, bærbare strømkilder. I journalen Angewandte Chemie , Kinesiske videnskabsmænd har introduceret en ekstraordinært strækbar og komprimerbar polye
Super strækbar, superkomprimerbare superkondensatorerFleksibel, bærbar elektronik kræver lige så fleksibel, bærbare strømkilder. I journalen Angewandte Chemie , Kinesiske videnskabsmænd har introduceret en ekstraordinært strækbar og komprimerbar polye -
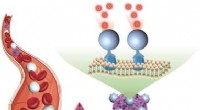 Direkte påvisning af cirkulerende tumorceller i blodprøverKredit:Wiley-VCH Tumorceller, der cirkulerer i blodet, er markører for tidlig opdagelse og prognose af kræft. Imidlertid, påvisning af disse celler er udfordrende på grund af deres knaphed. I jour
Direkte påvisning af cirkulerende tumorceller i blodprøverKredit:Wiley-VCH Tumorceller, der cirkulerer i blodet, er markører for tidlig opdagelse og prognose af kræft. Imidlertid, påvisning af disse celler er udfordrende på grund af deres knaphed. I jour -
 Svamp producerer yderst effektivt overfladeaktivt stofDr. Markus Greßler (l.) Og Florian Baldeweg undersøger en kultur af svampen Mortierella alpina. Jena -forskerne var i stand til at bevise, at svampen producerer store mængder af et overfladeaktivt sto
Svamp producerer yderst effektivt overfladeaktivt stofDr. Markus Greßler (l.) Og Florian Baldeweg undersøger en kultur af svampen Mortierella alpina. Jena -forskerne var i stand til at bevise, at svampen producerer store mængder af et overfladeaktivt sto -
 Forskere udvikler mikrobobler til at ødelægge farlige biofilmProfessor i kemisk og biomolekylær ingeniørvidenskab Simon Rogers, venstre, postdoktorale forskere Jun Pong Park og Yongbeom Seo og professor i kemisk og biomolekylær teknik Hyunjoon Kong ledede et in
Forskere udvikler mikrobobler til at ødelægge farlige biofilmProfessor i kemisk og biomolekylær ingeniørvidenskab Simon Rogers, venstre, postdoktorale forskere Jun Pong Park og Yongbeom Seo og professor i kemisk og biomolekylær teknik Hyunjoon Kong ledede et in
- Kan Nemo finde vej hjem?
- Forskere ser på olie og vand interaktion for at forhindre vandforurening
- Hvordan sammenlignes størrelsen på Saturn med jorden og solen?
- Hvad er modstanden for luft til et bevægende objekt?
- Hvordan ved du, at et objekt har energi?
- Hvilke fossile brændstoffer bruger Australien til at producere elektricitet?


