Forståelse af kovalent binding:Hvordan atomer deler elektroner for at danne stabile molekyler
Af Timothy Burns
Opdateret 24. marts 2022
Kovalente bindinger dannes, når to eller flere atomer deler et eller flere elektronpar, hvilket gør det muligt for hvert atom at opnå en stabil ydre elektronkonfiguration. Tænk på dette som en afbalanceret skammel:hvert ben (elektronpar) er afgørende for stabiliteten.
Bi-atomiske molekyler
De enkleste kovalente forbindelser er diatomiske molekyler, såsom O₂, H₂ og Cl2, som naturligt eksisterer som par af identiske atomer. Deres delte elektroner opfylder oktetreglen for hvert konstituerende atom.
Enkelt kovalente bindinger
En enkelt kovalent binding involverer to atomer, der deler et elektronpar. Klassiske eksempler omfatter hydrogenchlorid (HCl) og methan (CH4). I CH4 deler hvert brintatom en elektron med det centrale kulstof, hvilket giver kulstof otte elektroner og hver brint to, og derved opfylder oktetreglen.
Dobbelt kovalente bindinger
Når to atomer deler to elektronpar, dannes en dobbeltbinding, som er markant stærkere end en enkeltbinding. O₂-molekylet har en dobbeltbinding med en bindingsenergi på ca. 498 kJmol⁻1, hvilket bidrager til dets høje stabilitet. Denne styrke betyder, at brydning af O=O-bindingen – såsom ved elektrolyse af vand – kræver betydelig energitilførsel.
Gasformig ved stuetemperatur
Kovalent bundne molekyler forbliver ofte gasser ved stuetemperatur, fordi kræfterne mellem individuelle molekyler er svage. Deres stærke intramolekylære bindinger efterlader intet incitament for molekylerne til at interagere tæt, hvilket resulterer i lave smeltepunkter og vedvarende gasformige tilstande.
Elektrisk ledningsevne
I modsætning til ioniske forbindelser dissocierer kovalente stoffer ikke til frie ioner, når de opløses i vand. Som følge heraf er vandige opløsninger af kovalente molekyler typisk ikke-ledende, da elektronerne forbliver bundet i molekylerne i stedet for at bevæge sig frit.
Sidste artikelByg en 3D-model af et natriumatom:Trin-for-trin-vejledning
Næste artikelHvorfor bomuld er det ultimative absorberende stof
 Varme artikler
Varme artikler
-
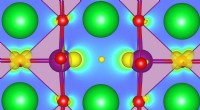 Forskere forbedrer beskrivelsen af defekte oxider med beregning af første principperAt forstå, hvordan defekter kan påvirke grundtilstandsegenskaber, fremme faseovergange, eller muliggøre helt nye funktionaliteter i nogle stærkt korrelerede oxider er blevet et emne af stor interesse
Forskere forbedrer beskrivelsen af defekte oxider med beregning af første principperAt forstå, hvordan defekter kan påvirke grundtilstandsegenskaber, fremme faseovergange, eller muliggøre helt nye funktionaliteter i nogle stærkt korrelerede oxider er blevet et emne af stor interesse -
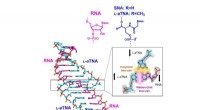 Livets helix:Ny undersøgelse viser, hvordan RNA stabilt binder sig til kunstige nukleinsyrerFigur 1:SNA og L-aTNA, omfattende en serinol- og L-threoninol-rygrad, henholdsvis, kan hybridisere med RNA. Denne undersøgelse bestemte krystallstrukturer af dimerer af hetero duplex af L-aTNA/RNA og
Livets helix:Ny undersøgelse viser, hvordan RNA stabilt binder sig til kunstige nukleinsyrerFigur 1:SNA og L-aTNA, omfattende en serinol- og L-threoninol-rygrad, henholdsvis, kan hybridisere med RNA. Denne undersøgelse bestemte krystallstrukturer af dimerer af hetero duplex af L-aTNA/RNA og -
 Aktiv maskinlæring til opdagelse og krystallisering af gigantiske polyoxometalatmolekylerKredit:Wiley Hvem er den bedre eksperimenterende, et menneske eller en robot? Når det kommer til at udforske syntetiske og krystallisationsbetingelser for uorganiske gigantiske molekyler, aktivt l
Aktiv maskinlæring til opdagelse og krystallisering af gigantiske polyoxometalatmolekylerKredit:Wiley Hvem er den bedre eksperimenterende, et menneske eller en robot? Når det kommer til at udforske syntetiske og krystallisationsbetingelser for uorganiske gigantiske molekyler, aktivt l -
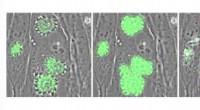 Parasitforskning varmer opIntracellulære Toxoplasma -parasitter, der udtrykker den genetisk kodede calciumindikator GCaMP. Parasitter blev behandlet med A23187, en forbindelse, der forårsager tilstrømning af calcium og stimule
Parasitforskning varmer opIntracellulære Toxoplasma -parasitter, der udtrykker den genetisk kodede calciumindikator GCaMP. Parasitter blev behandlet med A23187, en forbindelse, der forårsager tilstrømning af calcium og stimule


