Sådan får du sikkert og bruger rødt fosfor
Af Chris Deziel – Opdateret 24. marts 2022
Rødt fosfor er et alsidigt materiale med en lang historie inden for industrielle og rekreative anvendelser. Fra fyrværkeri og tændstikhoveder til gødningsproduktion og fremstilling af halvledere, dets unikke egenskaber gør det uundværligt på mange områder. Mens stoffet har et mørkt ry på grund af dets tilknytning til ulovlig metamfetaminproduktion, er dets legitime anvendelser omfattende og velregulerede.
Hvad er rødt fosfor?
Rød phosphor er en af de tre stabile allotroper af elementært phosphor (P4 ). Det produceres ved at opvarme hvidt fosfor til omkring 250°C (482°F) i en længere periode. Sammenlignet med det hvide modstykke er rødt fosfor mindre reaktivt, har et højere smeltepunkt og er mere stabilt, hvilket gør det mere sikkert at håndtere under kontrollerede forhold.
Industriel efterspørgsel og regulering
Det Europæiske Kemikalieagentur anslår, at der årligt produceres 1.000-10.000 tons fosfor til industriel brug. I USA regulerer Drug Enforcement Administration (DEA) salg og import af rød phosphor, hvid phosphor og hypophosphorsyre (H3 PO2 ) på grund af deres potentiale for ulovlig brug. Enhver, der køber eller importerer materialet, skal overholde DEA-reglerne og skal muligvis fremlægge dokumentation for lovlig brug.
Historisk baggrund
Grundstoffet blev først isoleret af alkymisten Hennig Brand i 1669, da han raffinerede fosfor fra urin under sin søgen efter de vises sten. Brands opdagelse gav hvidt fosfor, som er meget reaktivt og skal opbevares under vandet for at forhindre spontan antændelse. Den mere stabile røde allotrop blev senere opdaget af den østrigske kemiker Anton von Schrötter i 1845.
Nøgleallotroper af fosfor
- Hvidt fosfor: Meget reaktiv, lyser i mørke, skal holdes nedsænket.
- Rød fosfor: Sikrere, brugt i tændstikhoveder og flammehæmmere.
- Sort fosfor: Endnu mere stabil, dukker op i elektroniske applikationer.
Kommercielle produktionsruter
Industriel produktion involverer typisk udvinding af fosfor fra fosfatsten eller benaske. Materialet behandles med svovlsyre for at producere phosphorsyre, som derefter destilleres i nærvær af trækul og en kontrolleret flamme for at give hvidt fosfor. Det hvide fosfor opvarmes efterfølgende for at producere rødt fosfor.
Hvorfor er rødt fosfor vigtigt i hverdagsprodukter
- Fyrværkeri og fakkelproduktion.
- Tændstikhoveder, der slås overalt, og slagplader til sikkerhedsmatch.
- Brandhæmmende additiv i plast og harpiks.
- Gødningskomponent, især i knogleaske-baserede formuleringer.
- Dopingmiddel til silicium i halvlederfremstilling.
Sikker håndtering og opbevaring
Mens rødt fosfor er mindre farligt end hvidt fosfor, er det stadig et brændbart materiale. Det skal opbevares på et køligt, tørt sted og håndteres med passende personlige værnemidler. I tilfælde af spild kan materialet neutraliseres med en fortyndet syreopløsning.
Humane diætkilder til fosfor
Fosfor er afgørende for knogle- og tanddannelse, proteinsyntese og energiproduktion via ATP. Kostindtag kommer primært fra:
- Animalske produkter:mælk, kylling, svinekød, orgelkød og fisk og skaldyr.
- Plantekilder:bønner, linser, ærter, fuldkornsbrød, korn, nødder, frø, chokolade, quinoa og amaranth.
- Gødning:Knogleaske og flagermusguano er rige på fosfor og understøtter plantevækst.
Konklusion
Rødt fosfor er en kritisk komponent i mange sikre og regulerede industrier. At forstå dets egenskaber, produktionsmetoder og legitime anvendelser hjælper med at sikre ansvarlig håndtering og overholdelse af lovkrav.
 Varme artikler
Varme artikler
-
 Jernbaserede solceller på vej til at blive mere effektiveKredit:CC0 Public Domain En international undersøgelse ledet fra Lunds Universitet i Sverige viser, at 30 procent af energien i en bestemt type lysabsorberende jernmolekyle forsvinder på en hidtil
Jernbaserede solceller på vej til at blive mere effektiveKredit:CC0 Public Domain En international undersøgelse ledet fra Lunds Universitet i Sverige viser, at 30 procent af energien i en bestemt type lysabsorberende jernmolekyle forsvinder på en hidtil -
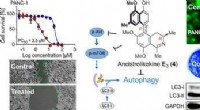 Rainforest vinforbindelse udsulter bugspytkirtelkræftcellerKredit:American Chemical Society Bugspytkirtelkræftceller er kendt for deres evne til at trives under ekstreme forhold med lave næringsstoffer og ilt, en egenskab kendt på kræftområdet som nøjsomh
Rainforest vinforbindelse udsulter bugspytkirtelkræftcellerKredit:American Chemical Society Bugspytkirtelkræftceller er kendt for deres evne til at trives under ekstreme forhold med lave næringsstoffer og ilt, en egenskab kendt på kræftområdet som nøjsomh -
 Ny måde at støde flåter af:Tør deres spyt opKredit:CC0 Public Domain Spyt fra en skovflåts bid kan overføre patogener, der forårsager alvorlige sygdomme, såsom Lyme sygdom, og betydelige landbrugstab. Nuværende insekticider har ulemper, så
Ny måde at støde flåter af:Tør deres spyt opKredit:CC0 Public Domain Spyt fra en skovflåts bid kan overføre patogener, der forårsager alvorlige sygdomme, såsom Lyme sygdom, og betydelige landbrugstab. Nuværende insekticider har ulemper, så -
 Dyb læring for nye legeringerDer vises en datadrevet arbejdsgang til at kortlægge de elastiske egenskaber af højentropi-legeringsrummet. Kredit:Chen et al. Hvornår er noget mere end blot summen af dets dele? Legeringer viser
Dyb læring for nye legeringerDer vises en datadrevet arbejdsgang til at kortlægge de elastiske egenskaber af højentropi-legeringsrummet. Kredit:Chen et al. Hvornår er noget mere end blot summen af dets dele? Legeringer viser
- Hvad hedder molekyler, der udgør slim?
- Hvad var den første menneskelige opfindelse, der bryder lydhastigheden?
- Hvad er den frie energiændring af hydrolyse ATP til ADP?
- Hvordan vil klimapolitikken påvirke målene for energiadgang?
- Hvad forårsager den top? Besvarelse af et langvarigt spørgsmål om kovalente væsker
- Hvilken enhed måler massen af et enkelt atom?


