Overgangsmetaller vs. indre overgangsmetaller:Nøgleforskelle forklaret
Af Angie Chipera Opdateret 24. marts 2022
Mens både overgangsmetaller og indre overgangsmetaller optager tilstødende blokke i det periodiske system, divergerer deres elektroniske konfigurationer og reaktivitet markant. Inden for den indre overgangsserie udviser lanthanider og aktinider distinkt adfærd på trods af at de begge er klassificeret som sjældne jordarters grundstoffer.
Atomnummer
Et grundstofs atomnummer - dets protonantal - definerer dets position i det periodiske system. Overgangsmetaller spænder over atomnumrene 21 til 118 og omfatter også de indre overgangsmetaller.
Atomstruktur
Begge grupper deler en d-blok-ramme, men deres elektronbelægningsmønstre er forskellige. Indre overgangsmetaller, med f-elektron involvering, er mere tilbøjelige til elektrontab og danner typisk +3 oxidationstilstande sammenlignet med de +2 tilstande, der er almindelige i overgangsmetaller.
Lanthanider
Lanthanider, med nummer 57 (La) til 71 (Lu), deler ensartede reaktivitetsprofiler. Disse bløde, formbare metaller er meget reaktive, oxiderer let i luften og tjener afgørende roller på tværs af elektronik, katalyse og avancerede materialer.
Actinider
Aktinider spænder over atomnumrene 89 (Ac) til 103 (Lr) og er universelt radioaktive. Uran og plutonium, de to naturligt forekommende aktinider, understøtter atomkraft og våben, mens alle tungere aktinider er syntetiske.
Referencer
- \"Kemi\"; Karen Timberlake; 2009
- \"Kemi\"; John C. Kotz, et al.; 1999
 Varme artikler
Varme artikler
-
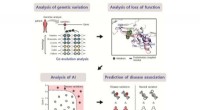 Evolutionær koblingsanalyse identificerer virkningen af sygdomsassocierede varianterSkematisk af den udviklede metode til at identificere virkningen af sygdomsassocierede varianter. Kredit:POSTECH Forudsigelse af virkningen af DNA-sekvensvarianter er vigtig for sortering af s
Evolutionær koblingsanalyse identificerer virkningen af sygdomsassocierede varianterSkematisk af den udviklede metode til at identificere virkningen af sygdomsassocierede varianter. Kredit:POSTECH Forudsigelse af virkningen af DNA-sekvensvarianter er vigtig for sortering af s -
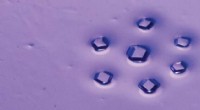 Låste MOF'er er nøglen til høj porøsitetMetal organiske rammer (MOFer) er krystallinske materialer fremstillet af metalioner forbundet med organiske linkere. De er ideelle til at være vært for forskellige molekyler og har fundet anvendelser
Låste MOF'er er nøglen til høj porøsitetMetal organiske rammer (MOFer) er krystallinske materialer fremstillet af metalioner forbundet med organiske linkere. De er ideelle til at være vært for forskellige molekyler og har fundet anvendelser -
 Omdannelse af spildevandsbiprodukter til bæredygtige grønne brændstofferKredit:Jonutis, Shutterstock En enorm mængde organisk affald fra forskellige sektorer ender enten på lossepladser eller bliver forbrændt, yderligere stigende drivhusgasemissioner (GHG) og jord- og
Omdannelse af spildevandsbiprodukter til bæredygtige grønne brændstofferKredit:Jonutis, Shutterstock En enorm mængde organisk affald fra forskellige sektorer ender enten på lossepladser eller bliver forbrændt, yderligere stigende drivhusgasemissioner (GHG) og jord- og -
 Forskere laver bæredygtig polymer af sukkerarter i træDen nye polymer er fremstillet ved hjælp af xylose, et sukker, der findes i træ. Kredit:Leszek Kobusinski Forskere fra University of Bath har lavet en bæredygtig polymer ved at bruge det næstmest
Forskere laver bæredygtig polymer af sukkerarter i træDen nye polymer er fremstillet ved hjælp af xylose, et sukker, der findes i træ. Kredit:Leszek Kobusinski Forskere fra University of Bath har lavet en bæredygtig polymer ved at bruge det næstmest
- Hvad er en lille gruppe stjerner, der danner mønster inden for konstellation?
- Forskning viser, hvordan parklignende tsunamiforsvar kan give et bæredygtigt alternativ til tårnhø…
- Mineraler findes kun i naturen?
- Hvem var den første person, der gik i Space Project Gemini?
- Hvad kalder du en permanent stigning i kropsstørrelse og tør masse af en organisme fra celletal?
- Hvordan kan islation føre til dannelse af nye arter?


