Mestring af ækvivalenspunktet i titreringseksperimenter
Af Claire Gillespie, Opdateret 24. marts 2022
I analytisk kemi er en titrering en kvantitativ teknik, hvor en opløsning af kendt koncentration (titranten) tilsættes til et målt volumen af en anden opløsning af ukendt koncentration (analytten). Processen fortsætter, indtil reaktionen mellem de to opløsninger er afsluttet. I dette øjeblik kaldet ækvivalenspunktet , er antallet af mol titrant lig med antallet af mol analyt, hvilket giver dig mulighed for at beregne analyttens koncentration med præcision.
TL;DR
Ækvivalenspunktet nås, når de reagerende arter er støkiometrisk afbalancerede. Det detekteres af en tydelig ændring i en indikator eller et plateau på et pH-meter, hvilket indikerer ingen yderligere reaktion.
Titreringstyper
- Syre-base titreringer – neutralisering af en syre med en base eller omvendt, almindeligvis overvåget med en farveindikator eller pH-meter.
- Redox-titreringer – overførsel af elektroner mellem arter, ofte ved hjælp af et oxidations- eller reduktionsmiddel som titrant.
- Kompleksometriske titreringer – dannelse af et stabilt kompleks mellem analytten og en ligand, nyttigt til metalionanalyse.
- Titrering af nedbør – et bundfald dannes ved ækvivalenspunktet, såsom ved titrering af en chloridion med sølvnitrat.
Væsentligt udstyr
- Erlenmeyer-kolbe eller bægerglas (helst 250 ml)
- Præcis burette (0,01 ml opløsning) og stativ
- Analytisk balance til måling af faste stoffer
- Destilleret vand og pipette til fortynding
- Indikatoropløsning (f.eks. phenolphtalein, methylorange) eller et kalibreret pH-meter
- Glas til skylning af faste stoffer i opløsning
Trin-for-trin-procedure
- Væg eller mål analytten nøjagtigt, og overfør den til kolben. Hvis analytten er fast, skyl den i kolben med destilleret vand.
- Tilsæt destilleret vand, indtil analytten er helt opløst, og optag derefter det endelige volumen.
- Hvis du bruger en farveindikator, tilsæt et par dråber og rotér forsigtigt for at blande.
- Fyld buretten med titranten, og sørg for, at der ikke er luftbobler, og noter det indledende volumen.
- Placer kolben under buretten, luk for hanen, og begynd at tilsætte titranten dråbevis.
- Efter hver tilsætning drejes kolben rundt for at sikre fuldstændig blanding.
- Fortsæt med at tilføje titranten, indtil indikatoren skifter farve og forbliver sådan, eller indtil pH-meteret viser et plateau, der angiver ækvivalenspunktet.
- Optag den sidste burettelæsning. Forskellen mellem start- og slutvolumener, ganget med titrantkoncentrationen, er lig med mol analyt.
- Brug mol analyt og det kendte volumen af analytopløsningen til at beregne dens koncentration.
For større nøjagtighed skal du udføre mindst to titreringer og gennemsnit af resultaterne. Kalibrer altid din burette før hvert løb, og hold burettespidsen ren og fri for dryp.
Ved at følge disse bedste praksisser kan du trygt lokalisere ækvivalenspunktet og bestemme koncentrationer med den præcision, der kræves til streng kemisk analyse.
 Varme artikler
Varme artikler
-
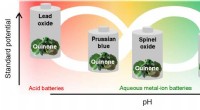 Billig organisk materiale giver sikre batterier en længere levetidUH-forskere har opdaget et nyt materiale, der har vist sig at være en effektiv anode til syre- og alkalibatterier, inklusive nye vandige metal-ion-batterier, giver løftet om sikker, langtidsholdbare b
Billig organisk materiale giver sikre batterier en længere levetidUH-forskere har opdaget et nyt materiale, der har vist sig at være en effektiv anode til syre- og alkalibatterier, inklusive nye vandige metal-ion-batterier, giver løftet om sikker, langtidsholdbare b -
 Døden muliggør kompleksitet i kemisk evolutionLivscyklussen for komplekse og mere simple replikatorer. De komplekse replikatorer produceres i en langsommere hastighed end de simple replikatorer, men da de er mere modstandsdygtige over for sammenb
Døden muliggør kompleksitet i kemisk evolutionLivscyklussen for komplekse og mere simple replikatorer. De komplekse replikatorer produceres i en langsommere hastighed end de simple replikatorer, men da de er mere modstandsdygtige over for sammenb -
 Forskere bruger maskinlæringsteknik til hurtigt at evaluere nye overgangsmetalforbindelserResultater fra en analyse af kunstigt neuralt netværk (ANN) er muligvis ikke pålidelige for molekyler, der er for forskellige fra dem, som ANN blev trænet på. De sorte skyer, der er vist her, dækker o
Forskere bruger maskinlæringsteknik til hurtigt at evaluere nye overgangsmetalforbindelserResultater fra en analyse af kunstigt neuralt netværk (ANN) er muligvis ikke pålidelige for molekyler, der er for forskellige fra dem, som ANN blev trænet på. De sorte skyer, der er vist her, dækker o -
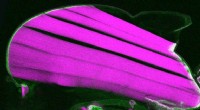 Hvordan holder muskel- og seneforbindelser hele livet?Skær i længderetningen gennem thoraxen på en frugtflue med en indsat kraftsensor i talinproteinet. Kraftsensoren på muskel-seneforbindelserne er grøn, og flyvemusklerne er magenta. Kredit:S. Lemke et
Hvordan holder muskel- og seneforbindelser hele livet?Skær i længderetningen gennem thoraxen på en frugtflue med en indsat kraftsensor i talinproteinet. Kraftsensoren på muskel-seneforbindelserne er grøn, og flyvemusklerne er magenta. Kredit:S. Lemke et


