Hvad er en monoatomisk ion? Forståelse af enkeltatom-ioner i kemi
Atomer er de grundlæggende enheder af stof. Hvert atom består af en positivt ladet kerne af protoner omgivet af en sky af negativt ladede elektroner. Når antallet af protoner er lig med antallet af elektroner, er atomet elektrisk neutralt, men alligevel søger det ofte en mere stabil elektronkonfiguration ved at danne bindinger med andre atomer.
Når et atom udveksler en eller flere elektroner med en anden, bliver det ladet og omtales som en ion. Hvis ionen er sammensat af et enkelt atom, kaldes den en monoatomisk ion. Omvendt er ioner, der indeholder to eller flere atomer, kendt som polyatomiske ioner.
Eksempler på monoatomiske ioner
Bordsalt (natriumchlorid) illustrerer monoatomiske ioners adfærd i hverdagen. I fast NaCl er hvert natriumatom (Na⁺) omgivet af chloridioner (Cl⁻), hvilket skaber et krystallinsk gitter. Når det opløses i vand, dissocieres gitteret til individuelle Na⁺- og Cl⁻-ioner, hvilket gør opløsningen til en elektrolyt, der leder elektricitet.
Andre almindelige monoatomiske ioner omfatter:
- Oxygenanioner (O²⁻) – dannet under ionisering af luft ved lyn.
- Tredobbelt ioniseret nitrogen (N³⁺) – også produceret i atmosfæriske begivenheder med høj energi.
Ioner, der bærer en positiv ladning, såsom Na⁺, kaldes kationer, mens dem med en negativ ladning, som Cl⁻, er anioner.
Eksempler på polyatomiske ioner
Polyatomiske ioner opstår, når to eller flere atomer kombinerer og deler elektroner og danner en ladet enhed. Bemærkelsesværdige eksempler omfatter:
- Hydronium (H₃O⁺) – den protonerede form af vand, der driver syre-base-kemien.
- Ammonium (NH₄⁺) – en nøglekation i gødning og biologiske systemer.
- Hydroxid (OH⁻) – den grundlæggende base, der neutraliserer hydronium til dannelse af vand.
- Nitrat (NO₃⁻) – en meget brugt anion i sprængstoffer og gødning.
- Carbonat (CO₃²⁻), Sulfat (SO₄²⁻) og fosfat (PO₄³⁻) – essentielle anioner i geologi, biologi og industri.
Sidste artikelKlordioxid:egenskaber, anvendelser og sikkerhed
Næste artikelMestring af ækvivalenspunktet i titreringseksperimenter
 Varme artikler
Varme artikler
-
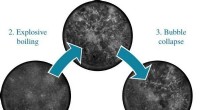 Køler rødglødende stål med varmt vandHøjhastighedsbilleder af køleprocessen. Kredit:Camila Gomez Ph.D. studerende Camila Gomez efterlignede afkølingsprocessen af Tata Steels højovne i laboratoriet og fandt ud af, at det er bedre at
Køler rødglødende stål med varmt vandHøjhastighedsbilleder af køleprocessen. Kredit:Camila Gomez Ph.D. studerende Camila Gomez efterlignede afkølingsprocessen af Tata Steels højovne i laboratoriet og fandt ud af, at det er bedre at -
 Tranebær kan reducere tarmsundhedsproblemer for kødspisereKredit:Julia Metkalova, Shutterstock Tranebær kaldes en superfood af en grund. Efter sigende fyldt med fibre og flere antioxidanter end nogen anden frugt og bær, tranebær er rost for deres mange s
Tranebær kan reducere tarmsundhedsproblemer for kødspisereKredit:Julia Metkalova, Shutterstock Tranebær kaldes en superfood af en grund. Efter sigende fyldt med fibre og flere antioxidanter end nogen anden frugt og bær, tranebær er rost for deres mange s -
 Forskere foreslår at bruge maskinlæring til at forudsige materialers egenskaberForskere foreslog at bruge maskinlæringsmetoder til at forudsige egenskaberne af kunstige safirkrystaller. Det er et unikt materiale, der er meget udbredt i mikroelektronik, optik og elektronik. Kredi
Forskere foreslår at bruge maskinlæring til at forudsige materialers egenskaberForskere foreslog at bruge maskinlæringsmetoder til at forudsige egenskaberne af kunstige safirkrystaller. Det er et unikt materiale, der er meget udbredt i mikroelektronik, optik og elektronik. Kredi -
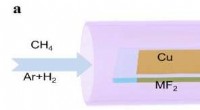 Fluor fremskynder todimensionel materialevækstSkematiske diagrammer over det eksperimentelle design til lokalt at introducere fluor til grafenvækst. Kredit:IBS Tilbage i 2004, fysikfællesskabet var lige begyndt at erkende eksistensen af vir
Fluor fremskynder todimensionel materialevækstSkematiske diagrammer over det eksperimentelle design til lokalt at introducere fluor til grafenvækst. Kredit:IBS Tilbage i 2004, fysikfællesskabet var lige begyndt at erkende eksistensen af vir
- Hvis et objekt bevæger sig i en cirkel med konstant hastighed, hvad er dens acceleration?
- Hvorfor betragtes sommerfuglen Bush betragtet som invasiv i sydlige stater?
- Ny forskning dokumenterer sværhedsgraden af LGBTQA+-konverteringspraksis – og hvorfor tro betyder…
- Hvilket organ reabsorberer vand ind i kroppen?
- Hvorfor bruger du ammoniumchlorid snarere end kun vand i Grignard -reaktionen?
- Hvad er den måde, lys sprænger fra en overflade, der er beskrevet af


