Atomer, ioner, molekyler og forbindelser:Forståelse af deres forskelle
Af Kevin Lee | Opdateret 24. marts 2022
Billedkredit:Creativeye99/iStock/GettyImages
Et enkelt sandkorn indeholder ca. 2,3×10 19 siliciumdioxid (SiO2) molekyler. Selvom det tal er svimlende, rummer kornet endnu flere atomer, da hvert SiO₂-molekyle er sammensat af tre atomer.
Atomer:Materiens byggesten
Atomer er de grundlæggende enheder af alle fysiske stoffer. Inde i et atom finder du en kerne - lavet af protoner og neutroner - omgivet af en sky af elektroner. Protoner har en positiv ladning, elektroner en negativ, og neutroner er neutrale. Når et atom har lige mange protoner og elektroner, er det elektrisk neutralt. Hver proton eller neutron er selv lavet af tre endnu mindre partikler kaldet kvarker.
Når atomer vinder eller taber elektroner:Ionernes fødsel
Når et atom mister en eller flere elektroner, bliver det positivt ladet; når den får elektroner, bliver den negativt ladet. Disse ladede atomer kaldes ioner. Fordi ioner bærer ladning, opfører de sig anderledes end neutrale atomer i kemiske reaktioner. For eksempel demonstrerer ionhalen på en komet – synlig når sollys ioniserer gasserne i dens koma – ioniske arters dynamiske natur.
Molekyler og forbindelser:kendetegn
Et molekyle er en gruppe af to eller flere atomer, der er kemisk bundet. Grundstoffer - såsom guld eller brint - er kun sammensat af én type atom, mens forbindelser består af mindst to forskellige grundstoffer. Kemiske formler afslører den nøjagtige sammensætning af et molekyle:vand (H2O) indeholder to hydrogenatomer og et oxygenatom. Sænkningen efter et elements symbol angiver antallet af atomer i det element; hvis der ikke er et underskrift til stede, antages der kun ét atom.
Fascinerende atomfakta
På trods af, at forskere kun har katalogiseret 109 grundstoffer (tallet er for nylig steget til 118 ifølge IUPAC), er mere end 13 millioner forskellige forbindelser blevet identificeret, hvilket illustrerer de enorme kombinatoriske muligheder for atombinding.
En isotop er en variant af et grundstof, der adskiller sig i neutrontal. For eksempel har brints mest almindelige isotop (protium) en proton og ingen neutroner, men dens tungere former - deuterium (en proton, en neutron) og tritium (en proton, to neutroner) - introducerer forskellige nukleare egenskaber. Når en kerne søger stabilitet, kan den udsende ioniserende stråling, et fænomen, der er centralt for nuklear kemi og fysik.
 Varme artikler
Varme artikler
-
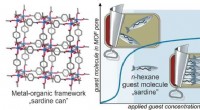 Gæstejustering og defektdannelse under porefyldning i metal-organiske rammefilmDen metalorganiske ramme danner et stillads med nanometerstore porer, som holder molekyler (til venstre). Så længe n-hexangas-molekyler tilsættes til porerne under tryk, justeres molekylerne i en sard
Gæstejustering og defektdannelse under porefyldning i metal-organiske rammefilmDen metalorganiske ramme danner et stillads med nanometerstore porer, som holder molekyler (til venstre). Så længe n-hexangas-molekyler tilsættes til porerne under tryk, justeres molekylerne i en sard -
 Forskere udfolder hemmelig stabilitet af bøjede sugerørUMass Amherst materialeforskere, med kolleger hos Virginia Tech, mener, at deres er den første undersøgelse, der undersøger, hvordan og hvorfor strukturer som bøjelige sugerør og sammenklappelige hund
Forskere udfolder hemmelig stabilitet af bøjede sugerørUMass Amherst materialeforskere, med kolleger hos Virginia Tech, mener, at deres er den første undersøgelse, der undersøger, hvordan og hvorfor strukturer som bøjelige sugerør og sammenklappelige hund -
 Forståelse af methylendiphenylisocyanat (MDI):Produktion, anvendelser og sikkerhedMethylendiphenylisocyanat (MDI) er en vigtig isocyanatforbindelse, der hovedsageligt anvendes til fremstilling af polyurethanskum, der finder anvendelse i isolering, polstring og kompositmaterialer. D
Forståelse af methylendiphenylisocyanat (MDI):Produktion, anvendelser og sikkerhedMethylendiphenylisocyanat (MDI) er en vigtig isocyanatforbindelse, der hovedsageligt anvendes til fremstilling af polyurethanskum, der finder anvendelse i isolering, polstring og kompositmaterialer. D -
 Algoritmer og lasere tæmmer kemisk reaktivitetKredit:CC0 Public Domain Forskere har udviklet en algoritme til fotokemi, bringer det spirende felt et skridt nærmere målet om at bruge forskellige lysfarver som en kontakt til at aktivere en rækk
Algoritmer og lasere tæmmer kemisk reaktivitetKredit:CC0 Public Domain Forskere har udviklet en algoritme til fotokemi, bringer det spirende felt et skridt nærmere målet om at bruge forskellige lysfarver som en kontakt til at aktivere en rækk
- Hvordan differentierer du salt og sukker?
- Byg digitalt, lever digitalt
- Hvilken slags energi afgiver, når et barn falder ud træ?
- Lovhåndhævelse står over for dilemmaer i vurderingen af online trusler
- Akemikere udnytter solen til at genbruge plastikaffald
- Hvilket volumen indeholder 2,4 mol klor, og hvordan regner du det ud?


