Sådan får du salt til at krystallisere derhjemme:Trin-for-trin-vejledning
Sådan får du salt til at krystallisere derhjemme
Af Sean Lancaster, Opdateret 24. marts 2022
Salt (natriumchlorid) opløses let i vand. Den klassiske metode til at udvinde salt fra havvand er afhængig af at fordampe vandet, indtil der kommer krystaller. I denne guide guider vi dig gennem processen i kontrollerede laboratoriemiljøer og fremhæver nøgleprincipperne for opløselighed og krystallisation.
Trin 1 – Opret en mættet løsning
Fyld et rent bægerglas med stuetemperatur vand. Tilsæt gradvist bordsalt under omrøring med en glasstang. Fortsæt med at tilføje indtil ikke mere salt er opløst; opløsningen er nu mættet, hvilket betyder, at den indeholder den maksimale mængde salt, som vand kan holde ved den temperatur.
Trin 2 – Opvarm opløsningen
Stil bægerglasset på en varmeplade og hæv forsigtigt temperaturen med et par grader celsius. Varmt vand kan indeholde mere salt, så dette øger opløselighedsgrænsen.
Trin 3 – Overmætning af blandingen
Mens opløsningen stadig er varm, bliv ved med at tilføje salt, indtil den ikke længere er opløst. Blandingen er nu overmættet - mere salt, end der normalt kan forblive opløst ved den temperatur.
Trin 4 – Køl ned
Sluk for varmepladen, og lad opløsningen afkøle naturligt. Efterhånden som temperaturen falder, falder vandets evne til at holde salt, og det overskydende salt begynder at udfældes.
Trin 5 – Start krystallisation
For at udløse krystalvækst skal du enten ridse den indvendige væg af bægeret under opløsningsniveauet med stangen eller indsætte et lille stykke præ-formet saltkrystal. Ridsen eller frøet giver et kernedannelsessted, hvor saltioner kan begynde at arrangere sig i et krystalgitter.
Materialer du skal bruge
- Bordsalt (natriumchlorid)
- Destilleret vand eller postevand
- Kogeplade eller varmeelement
- Klar glasbæger
- Rørestav af glas
Ved at følge disse trin kan du observere transformationen fra en klar, mættet væske til krystallinsk salt, hvilket illustrerer den grundlæggende videnskab bag fordampningsdamme og gammel saltproduktion.
 Varme artikler
Varme artikler
-
 Video:Hvordan bly (måske) forårsagede det gamle Roms undergangKredit:The American Chemical Society Det antikke Roms kejsere lavede nogle ret bizarre ting - brast ud i ukontrollable latteranfald, udnævne en hest til præst, klæder sig i dyreskind og angriber m
Video:Hvordan bly (måske) forårsagede det gamle Roms undergangKredit:The American Chemical Society Det antikke Roms kejsere lavede nogle ret bizarre ting - brast ud i ukontrollable latteranfald, udnævne en hest til præst, klæder sig i dyreskind og angriber m -
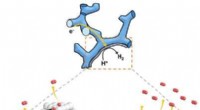 Wolframsuboxid forbedrer platinets effektivitet ved brintproduktionFigur. Skematisk fremstilling af hydrogen evolution reaktion (HER) af pseudo single-atom Pt understøttet af wolframsuboxid. Kredit:Korea Advanced Institute of Science and Technology Forskere præse
Wolframsuboxid forbedrer platinets effektivitet ved brintproduktionFigur. Skematisk fremstilling af hydrogen evolution reaktion (HER) af pseudo single-atom Pt understøttet af wolframsuboxid. Kredit:Korea Advanced Institute of Science and Technology Forskere præse -
 Hvordan tardigradens hemmeligheder kunne forbedre livreddende lægemidler som insulinSEM-billede af Milnesium tardigradum i aktiv tilstand. Kredit:PLoS ONE 7(9):e45682. doi:10.1371/journal.pone.0045682 UCLA-kemiker Heather Maynard måtte undre sig:Hvordan gør organismer som tardigra
Hvordan tardigradens hemmeligheder kunne forbedre livreddende lægemidler som insulinSEM-billede af Milnesium tardigradum i aktiv tilstand. Kredit:PLoS ONE 7(9):e45682. doi:10.1371/journal.pone.0045682 UCLA-kemiker Heather Maynard måtte undre sig:Hvordan gør organismer som tardigra -
 Mikrobølger afslører detaljeret struktur af molekylær motorSom en makroskopisk motor, det kunstige motormolekyle har en stator (nederst) og en rotor (øverst), forbundet med en aksel. Kredit:Sérgio Domingos / DESY Et team af forskere har brugt mikrobølger
Mikrobølger afslører detaljeret struktur af molekylær motorSom en makroskopisk motor, det kunstige motormolekyle har en stator (nederst) og en rotor (øverst), forbundet med en aksel. Kredit:Sérgio Domingos / DESY Et team af forskere har brugt mikrobølger
- Sådan fungerer din hjerne
- Første kig på nanoskala på, hvordan lithiumioner navigerer i en molekylær labyrint for at nå ba…
- Hvorfor er der ingen mekaniske bølger i OutSpace?
- Hvorfor er materie og energi vigtige?
- Kan den relative hastighed af to kroppe være større end absolut?
- Hvad er energien fra en foton med bølgelængde 827nm hvilken type radion det?


