Hvordan salt opløst i vand muliggør elektrisk ledningsevne
Af Isaiah David Opdateret 24. marts 2022
Visage/Stockbyte/Getty Images
Elektricitet og ledningsevne
For at forstå, hvorfor saltvand leder elektricitet, skal vi først definere elektricitet. Elektricitet er strømmen af ladede partikler - primært elektroner - gennem et medium. I metaller som kobber bevæger elektroner sig frit og fører strøm direkte. I elektrolytter som saltvand transporteres strøm af ioner.
Comstock Images/Comstock/Getty Images
Opløsning af salt i vand
Rent vand er en dårlig leder; kun en minimal mængde strøm kan passere gennem den. Når natriumchlorid (NaCl) opløses i vand, opløses molekylerne i natrium (Na⁺) og chlorid (Cl⁻) ioner. Na⁺-ionen, der har mistet en elektron, bærer en positiv ladning, mens Cl⁻-ionen, der har fået en elektron, bærer en negativ ladning.
Thinkstock/Comstock/Getty Images
Generering af en strøm i saltvand
Anvendelse af en elektrisk kilde skaber to terminaler:en negativ (katode) og en positiv (anode). Modsatte ladninger tiltrækker, så Na⁺-ioner trækkes mod katoden og Cl⁻-ioner mod anoden. Disse ioner flytter elektroner mellem terminalerne og danner en kontinuerlig ledende bane, der tillader en målbar strøm at flyde.
Digital Vision./Digital Vision/Getty Images
 Varme artikler
Varme artikler
-
 Sådan tilberedes en bromthymol blå pH-indikatoropløsningAf Kevin Krause, Opdateret 24. marts 2022 Bromthymolblåt er en meget brugt pH-indikator, der skifter fra gul i sure opløsninger til blå i basiske miljøer. Denne trin-for-trin guide viser, hvordan man
Sådan tilberedes en bromthymol blå pH-indikatoropløsningAf Kevin Krause, Opdateret 24. marts 2022 Bromthymolblåt er en meget brugt pH-indikator, der skifter fra gul i sure opløsninger til blå i basiske miljøer. Denne trin-for-trin guide viser, hvordan man -
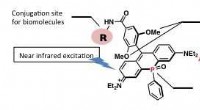 Et nær-infrarødt fluorescerende farvestof til langsigtet biobilleddannelseMolekylær struktur af det nye nær-infrarøde fluorescerende mærkningsmiddel PREX 710 med et koblingssted for et biomolekyle. Inkorporering af den elektrontiltrækkende phosphinoxid (P=O)-del i xanthenst
Et nær-infrarødt fluorescerende farvestof til langsigtet biobilleddannelseMolekylær struktur af det nye nær-infrarøde fluorescerende mærkningsmiddel PREX 710 med et koblingssted for et biomolekyle. Inkorporering af den elektrontiltrækkende phosphinoxid (P=O)-del i xanthenst -
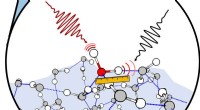 Kemikere ser nærmere på stedet, hvor vand møder luftSkematisk vandoverflade, hvor den spektrale signatur af et isotopisk mærket vandmolekyle er isoleret med to infrarøde lasere. Kredit:Nan Yang Vand, på trods af dens centrale plads i så mange proce
Kemikere ser nærmere på stedet, hvor vand møder luftSkematisk vandoverflade, hvor den spektrale signatur af et isotopisk mærket vandmolekyle er isoleret med to infrarøde lasere. Kredit:Nan Yang Vand, på trods af dens centrale plads i så mange proce -
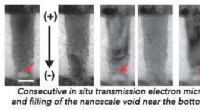 Forskere udvikler faseændringshukommelsesenheder til mere kraftfuld computingEt samarbejde mellem laboratoriet af Judy Cha, Carol og Douglas Melamed adjunkt i maskinteknik og materialevidenskab, og IBMs Watson Research Center kunne hjælpe med at gøre en potentielt revolutioner
Forskere udvikler faseændringshukommelsesenheder til mere kraftfuld computingEt samarbejde mellem laboratoriet af Judy Cha, Carol og Douglas Melamed adjunkt i maskinteknik og materialevidenskab, og IBMs Watson Research Center kunne hjælpe med at gøre en potentielt revolutioner
- Evolution og økologisk konkurrence mellem flercellede livscyklusser
- Forskere bruger maskinlæring til at hjælpe olieproduktionen
- Sådan beregnes procentdelen af ionisering Givet pH
- Lokalitetsdata som en identifikator af personlige data
- Hvordan sperm pakker fars genom, så det kan smelte sammen med mors
- Nanoskala saltkurve tæt på (med video)


