Arrhenius-syrer forklaret:deres dissociation i vand og kemisk betydning
alexkich/iStock/GettyImages
Forskeren Svante Arrhenius foreslog først, at syrer dissocierede i vand for at danne ioner. Ifølge ham var syrer materialer, der omfattede en brintion. Opløst i vand giver hydrogenionen, H+, opløsningen karakteristika af en syre. Arrhenius udviklede også en tilsvarende definition for en base. Når de er opløst i vand, producerer baser hydroxidioner, OH-, der giver opløsningen karakteristika af en base.
Arrhenius-definitionerne dækker mange af de mest almindelige syrer og baser og deres kemiske reaktioner, men der er andre materialer, der har karakteristika af syrer, men som ikke passer til Arrhenius-definitionen. Bredere definitioner af syrer kan omfatte nogle af disse materialer.
TL;DR (for lang; læste ikke)
En Arrhenius-syre er et materiale, der, når det opløses i vand, dissocieres til ioner, herunder hydrogenioner. Ifølge Arrhenius kan en syre defineres som et materiale, der øger koncentrationen af brintioner i vand. Den tilsvarende definition for baser er et materiale, der øger koncentrationen af hydroxidioner. Arrhenius-definitionerne er begrænset til materialer, der opløses i vand, mens bredere definitioner kan omfatte flere materialer blandt syrer og baser.
En Arrhenius-syres egenskaber
En Arrhenius-syres egenskaber
Historisk set blev syrer beskrevet som sure og ætsende, men man vidste kun lidt om grundlaget for disse egenskaber. I 1884 foreslog Svante Arrhenius, at forbindelser som NaCl eller bordsalt dannede ladede partikler kaldet ioner, når de blev opløst i vand. I 1887 havde Arrhenius udviklet en teori, der fik ham til at foreslå, at syrer ioniserede i vand for at producere brintioner. Hydrogenionerne gav syrer deres egenskaber.
Et vigtigt kendetegn ved syrer er, at de reagerer med metaller og danner et salt og brintgas. Ved at bruge Arrhenius definition af en syre er det klart, at syren opløses i vand til hydrogenioner og de andre negative ioner fra syren. Metallet kombineres med de negative ioner og efterlader hydrogenioner og ekstra elektroner for at danne brintgas.
Syrer reagerer også med baser og danner et salt og vand. Ifølge Arrhenius definition producerer baser hydroxidioner i opløsning. Som et resultat, i en syre-base reaktion, kombineres hydrogenionerne fra syren med hydroxidionerne fra basen for at danne vandmolekyler. De negative ioner fra syren kombineres med de positive ioner fra basen og danner et salt.
Eksempler på Arrhenius-syrereaktioner
Eksempler på Arrhenius-syrereaktioner
Når en typisk Arrhenius-syre som saltsyre reagerer med et metal eller en base, gør Arrhenius-definitionerne det nemt at følge reaktionerne. For eksempel reagerer saltsyre, HCl, med zink, Zn, og danner zinkchlorid og brintgas. De negative Cl-ioner kombineres med zinkatomerne for at danne ZnCl2-molekylerne og generere ekstra elektroner. Elektronerne kombineres med hydrogenionerne fra syren og bliver til brintgas. Den kemiske formel er Zn + 2HCl =ZnCl2 + H2.
Når saltsyre kombineres med en base såsom natriumhydroxid, NaOH, dissocieres basen til natrium- og hydroxidioner. Hydrogenionerne fra saltsyren kombineres med hydroxidionerne fra natriumhydroxidet og danner vand. Natriumionerne kombineres med klorionerne og danner NaCl eller bordsalt. Den kemiske formel er HCl + NaOH =NaCl + H2O.
Bredere definitioner af syrer
Bredere definitioner af syrer
Arrhenius definition af syrer er snæver i den forstand, at den kun gælder for stoffer, der opløses i vand, og kun for dem, der har brintioner. En bredere definition definerer syrer som stoffer, der øger koncentrationen af hydrogenioner, når de opløses i vand.
Endnu bredere definitioner, såsom Lewis- eller Bronsted-Lowry-definitionerne, beskriver syrer som elektronacceptorer eller som protondonorer. De omfatter stoffer, der udviser karakteristika for syrer, men som ikke passer til den traditionelle definition. For almindelige kemiske reaktioner udgør Arrhenius-definitionerne derimod et godt grundlag for at forklare, hvordan reaktionerne fungerer.
 Varme artikler
Varme artikler
-
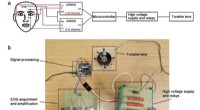 Øjestyret blød linse baner vej til bløde menneske-maskine-grænsefladerSkematisk og foto af det bløde linsesystem. Kredit:Cai lab/avancerede funktionelle materialer Et forskerhold ledet af University of California San Diego har udviklet en blød robotlinse, hvis bevæg
Øjestyret blød linse baner vej til bløde menneske-maskine-grænsefladerSkematisk og foto af det bløde linsesystem. Kredit:Cai lab/avancerede funktionelle materialer Et forskerhold ledet af University of California San Diego har udviklet en blød robotlinse, hvis bevæg -
 Hvordan spinder edderkoppen sin selvsamlede silke?Tilsætning af kaliumphosphat får de kunstige MaSp2 -proteiner til at kondensere til store dråber med høj densitet. Kredit:Kyoto University/Numata Lab Af alle de spændende emner inden for materiale
Hvordan spinder edderkoppen sin selvsamlede silke?Tilsætning af kaliumphosphat får de kunstige MaSp2 -proteiner til at kondensere til store dråber med høj densitet. Kredit:Kyoto University/Numata Lab Af alle de spændende emner inden for materiale -
 Foto-induceret ionforskydning i blandede halogenidperovskitter til et batteri, der kan oplades direk…PL-emissionskortlægning af MA0.17FA0.83Pb(I0.5Br0.5)3 ved detektionsbølgelængden på 670 nm og 790 nm efter lokal belysning i 1 time med en strålestørrelse på ~ 1 mm og tæthed på 1 sol på den bare film
Foto-induceret ionforskydning i blandede halogenidperovskitter til et batteri, der kan oplades direk…PL-emissionskortlægning af MA0.17FA0.83Pb(I0.5Br0.5)3 ved detektionsbølgelængden på 670 nm og 790 nm efter lokal belysning i 1 time med en strålestørrelse på ~ 1 mm og tæthed på 1 sol på den bare film -
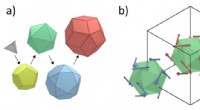 Kvasikrystalklar:Materiale afslører en unik forskydende overfladestruktur under mikroskopTsai-typen klynger sig inde i den anden af Au-Al-Tb tilnærmelsesvis videnskabsmændene valgte (a), og den tilsvarende spin -icosahedra (b). Kredit:Ryuji Tamura fra Tokyo University of Science Mel
Kvasikrystalklar:Materiale afslører en unik forskydende overfladestruktur under mikroskopTsai-typen klynger sig inde i den anden af Au-Al-Tb tilnærmelsesvis videnskabsmændene valgte (a), og den tilsvarende spin -icosahedra (b). Kredit:Ryuji Tamura fra Tokyo University of Science Mel
- Hvad betyder Seta i biologi?
- Celler falder i to brede kategorier afhængigt af om de har en cellevæg?
- Hvad flyder højere i vand et æble eller en peber?
- Hvilket mikroskop kan forstørre tusindvis af gange og give et 3 dimensions billede?
- Hvad hedder sukkermolekyle i RNA?
- Floridas kystlinje står over for årtier lange oversvømmelsestrusler – hvad de seneste kort over h…


