Sådan beregnes hastigheden af en kemisk reaktion:En praktisk vejledning
I en kemisk reaktion kolliderer partikler og overfører nok energi til at bryde eksisterende bindinger og danne nye. At forstå, hvor hurtigt denne proces sker, er afgørende for både kemikere, ingeniører og forskere.
Reaktionshastigheden
Overvej en simpel konvertering:A → B . Hastigheden kan beskrives ved, hvordan koncentrationen af A falder, eller hvordan B stiger over tid:
rate =-\dfrac{\Delta[A]}{\Delta t} =\dfrac{\Delta[B]}{\Delta t}
Det negative fortegn afspejler forbruget af A, mens ligningerne beregnes som gennemsnit over et valgt tidsinterval.
Bestemmelse af reaktionshastigheden
For at måle hastigheden eksperimentelt skal du overvåge koncentrationen af en reaktant eller et produkt som en funktion af tiden. Ved at registrere data på flere tidspunkter, plot koncentration versus tid og udregn hældningen for at opnå den øjeblikkelige hastighed.
Når du studerer en reaktion såsom A + B → C + D , er det almindeligt at holde en reaktant (f.eks. B) i stort overskud, således at dens koncentration forbliver i det væsentlige konstant. Dette isolerer virkningen af den anden reaktant (A) på hastigheden.
At plotte hastigheden mod varierende koncentrationer af A vil afsløre, om hastigheden er proportional med [A]. Et retlinet forhold indikerer en førsteordens afhængighed af A.
I så fald er hastighedskonstanten (k) defineret som:
k =\dfrac{rate}{[A]}
k er en sand konstant for en given reaktion ved en fast temperatur; den er uafhængig af koncentrationerne af reaktanterne. Dens enheder er typisk s -1 .
Støkiometri og reaktionshastigheder
Støkiometri relaterer molforholdet mellem reaktanter og produkter. For en afbalanceret ligning som 3A → B , et mol B forbruger tre mol A. Hastighedsudtrykket bliver:
rate =-\dfrac{1}{3}\dfrac{\Delta[A]}{\Delta t} =\dfrac{\Delta[B]}{\Delta t}
Mere generelt for aA + bB → cC + dD , satsen er:
rate =-\dfrac{1}{a}\dfrac{\Delta[A]}{\Delta t} =-\dfrac{1}{b}\dfrac{\Delta[B]}{\Delta t} =\dfrac{1}{c}\dfrac{\Delta[C]}{\Delta t} =\dfrac{1}{d}\dfrac{\Delta[D]}{\Delta t}
Satsloven
Hastighedsloven forbinder hastigheden med koncentrationerne af reaktanter, der er hævet til specifikke beføjelser:
rate =k[A]^x[B]^y
Her er k hastighedskonstanten, mens x og y er reaktionsrækkefølgerne i forhold til henholdsvis A og B. Disse eksponenter er ikke afledt af den kemiske ligning; de skal bestemmes eksperimentelt.
Beslutning af reaktionsrækkefølge:Et gennemarbejdet eksempel
Overvej reaktionen mellem hydrogen og salpetersyre:
2H2 + 2NO → N2 + 2H2 O
Takstloven har formen:
rate =k[H2 ]^x[NEJ]^y
Brug af starthastighedsdata:
| Eksperiment | [H2 ] | [NEJ] | Oprindelig sats (M/s) |
|---|---|---|---|
| 1 | 3,0×10 -3 | 1,0×10 -3 | 2,0×10 -4 |
| 2 | 3,0×10 -3 | 2,0×10 -3 | 8,0×10 -4 |
| 3 | 6,0×10 -3 | 2,0×10 -3 | 1,6×10 -3 |
Ved at sammenligne eksperimenter, hvor en reaktant holdes konstant, kan eksponenterne ekstraheres:
- Fordobling af [NEJ] (eksperiment 1→2) firdobler hastigheden, hvilket giver y =2.
- Fordobling af [H2 ] (eksperiment 2→3) fordobler hastigheden, hvilket giver x =1.
Takstloven er således:
rate =k[H2 ][NEJ] 2
Summering af ordrerne giver en overordnet tredjeordensreaktion.
Vigtige ting om reaktionsordrer
- Hastlove skal udledes eksperimentelt; de støkiometriske koefficienter giver ingen information om reaktionsrækkefølgen.
- En nulteordensreaktion har en hastighed lig med k, uafhængig af reaktantkoncentrationen.
- Reaktionsrækkefølgen afspejler, hvor følsomt hastigheden reagerer på ændringer i koncentrationen.
- Førsteordensreaktioner:fordobling af koncentrationen fordobler hastigheden.
- Andenordensreaktioner:hastigheden afhænger af én reaktant i anden eller to reaktanter hver i første potens.
Forståelse og anvendelse af disse principper muliggør nøjagtig kinetisk modellering, reaktordesign og optimering i industri- og laboratoriemiljøer.
 Varme artikler
Varme artikler
-
 Team får indsigt i oxidlaget af rustfrit stålFra venstre, Lin Zhu, beamline videnskabsmand; Alexei Zakharov, MAXPEEM beamline manager; Axel Knutsson, Materialespecialist hos Alfa Laval; Oskar Darselius Berg, Alfa Laval. Kredit:Lunds Universitet
Team får indsigt i oxidlaget af rustfrit stålFra venstre, Lin Zhu, beamline videnskabsmand; Alexei Zakharov, MAXPEEM beamline manager; Axel Knutsson, Materialespecialist hos Alfa Laval; Oskar Darselius Berg, Alfa Laval. Kredit:Lunds Universitet -
 Grønt brint:Fokus på katalysatoroverfladenGrønt brint er et håb for energiomstillingen. Vellykket brug, imidlertid, kræver detaljeret forståelse af dets produktionsprocesser. Kredit:Pascal Armbruster, KIT Brug af energi fra solcellemodule
Grønt brint:Fokus på katalysatoroverfladenGrønt brint er et håb for energiomstillingen. Vellykket brug, imidlertid, kræver detaljeret forståelse af dets produktionsprocesser. Kredit:Pascal Armbruster, KIT Brug af energi fra solcellemodule -
 Banebrydende forskning gør børnevacciner sikre ved alle temperaturerAsel Sartbaeva fra University of Bath har ledet arbejdet. Kredit:University of Bath Vacciner er notorisk svære at transportere til fjerntliggende eller farlige steder, da de ødelægges, når de ikke
Banebrydende forskning gør børnevacciner sikre ved alle temperaturerAsel Sartbaeva fra University of Bath har ledet arbejdet. Kredit:University of Bath Vacciner er notorisk svære at transportere til fjerntliggende eller farlige steder, da de ødelægges, når de ikke -
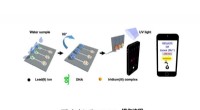 Ny enhed til hurtig og præcis detektering af blyDiagrammet viser detektionsprocessen. Kredit:HKBU Et forskerhold fra Institut for Kemi ved Hong Kong Baptist University (HKBU) har opfundet en bærbar enhed til one-stop-detektion af blykoncentrati
Ny enhed til hurtig og præcis detektering af blyDiagrammet viser detektionsprocessen. Kredit:HKBU Et forskerhold fra Institut for Kemi ved Hong Kong Baptist University (HKBU) har opfundet en bærbar enhed til one-stop-detektion af blykoncentrati
- Hvorfor er du i stand til at se månen, når den producerer sit eget lys?
- Kernen:DNA's beskyttende hjem i eukaryote celler
- Hvad er de vigtigste ting, der udgør universet?
- Ringede månen sandt i sit lysende skær i aften"?
- Hydrogel forbedrer leveringen af lægemiddel mod kræft
- Hvad indeholder enzymer, der bruges i nedbrydningen af glukose og generation ATP?


