Trin-for-trin guide til forberedelse af molære opløsninger
Af William Adkins Opdateret 24. marts 2022
En opløsning eller fortynding består af et fast stof opløst i et flydende opløsningsmiddel. Løsninger er integreret i medicin, industri og hverdagsapplikationer. Afhængigt af den påtænkte anvendelse kan en opløsnings koncentration udtrykkes som et masseforhold eller volumetrisk forhold mellem opløst stof og opløsningsmiddel. En molær opløsning indeholder specifikt et defineret antal mol opløst stof pr. liter opløsningsmiddel. De følgende trin beskriver, hvordan man fremstiller en molær opløsning.
Trin 1 – Forstå konceptet med muldvarp og molære opløsninger
En muldvarp er mængden af stof, der indeholder 6,02×10²³ elementære enheder, kendt som Avogadros tal. Denne værdi blev valgt, fordi massen i gram af et mol af en forbindelse nøje svarer til dens molære masse. For eksempel vejer et mol vand cirka 18 g, hvilket svarer til atomvægten af et vandmolekyle. En molær opløsning indeholder et bestemt antal mol opløst stof pr. liter opløsningsmiddel. Trinene nedenfor antager, at du forbereder en 1-liters opløsning.
Trin 2 – Evaluer potentielle kemiske reaktioner ved opløsning
Før du tilsætter opløsningsmidlet, skal du vurdere, om der kan forekomme eksoterme, endoterme eller farlige reaktioner. Brug altid rene kemikalier af analytisk kvalitet. Brug f.eks. destilleret vand i stedet for postevand; postevandets urenheder kan ændre opløsningens kemi.
Trin 3 – Bestem den nøjagtige masse af det opløste stof, der kræves
Beregn massen ved at gange den ønskede molaritet (mol pr. liter) med molmassen af det opløste stof. Vej den beregnede mængde på en kalibreret analytisk vægt.
Trin 4 – Opløs det målte opløste stof i en kalibreret 1-liters beholder
Anbring det vejede faststof i en ren 1-liters målekolbe eller krukke. Tilsæt opløsningsmiddel gradvist under omrøring, indtil det samlede volumen når nøjagtigt 1 l. Hvis det opløste stof er langsomt til at opløses, kan forsigtig opvarmning hjælpe, men undgå at overskride opløselighedsgrænsen.
Ting påkrævet
- Analytisk balance kalibreret i gram
- 1-liters målekolbe eller krukke
- Oprenset fast stof, der skal opløses
- Opløsningsmiddel (f.eks. destilleret vand)
TL;DR
Sørg for, at din opløsnings koncentration er under opløselighedsgrænsen. Præcise målinger og bevidsthed om potentielle reaktioner er afgørende for en pålidelig molær opløsning.
 Varme artikler
Varme artikler
-
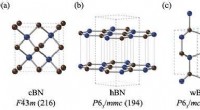 Forudsigelse af den mest stabile bornitridstruktur med kvantesimuleringerStrukturerne og rumgrupperne af (a) zink-blende bornitrid (cBN), (b) hexagonal bornitrid (hBN), (c) wurtzite bornitrid (wBN) og (d) romboedral bornitrid (rBN). Bor- og nitrogenatomer er afbildet i hen
Forudsigelse af den mest stabile bornitridstruktur med kvantesimuleringerStrukturerne og rumgrupperne af (a) zink-blende bornitrid (cBN), (b) hexagonal bornitrid (hBN), (c) wurtzite bornitrid (wBN) og (d) romboedral bornitrid (rBN). Bor- og nitrogenatomer er afbildet i hen -
 Hvorfor nogle stoffer holder dig varm:Videnskaben om termisk effusivitetAf Brett Smith Opdateret 24. marts 2022 David De Lossy/Photodisc/Getty Images Et stofs evne til at holde på varmen omtales som dets termiske effusivitet. To faktorer påvirker, hvor godt et stof k
Hvorfor nogle stoffer holder dig varm:Videnskaben om termisk effusivitetAf Brett Smith Opdateret 24. marts 2022 David De Lossy/Photodisc/Getty Images Et stofs evne til at holde på varmen omtales som dets termiske effusivitet. To faktorer påvirker, hvor godt et stof k -
 Forståelse af kovalente bindinger:Hvordan atomer deler elektronerWittayayut/iStock/GettyImages Hvad er en kovalent binding? En kovalent binding dannes, når to eller flere ikke-metalatomer deler et eller flere par valenselektroner, hvilket skaber en stabil, retning
Forståelse af kovalente bindinger:Hvordan atomer deler elektronerWittayayut/iStock/GettyImages Hvad er en kovalent binding? En kovalent binding dannes, når to eller flere ikke-metalatomer deler et eller flere par valenselektroner, hvilket skaber en stabil, retning -
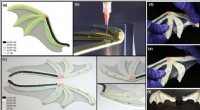 Forskere bryder ny vej inden for 3D-printet blød robotteknologi med det største udvalg af polymerh…(a) Illustration af det strukturelle design. (b) Direkte blæk-skrivning af hybridstrukturen. (c) Hærdet struktur (areal på ~90 cm 2 per vinge, membrantykkelse ~0,7 mm, total armtykkelse ~3,5 mm). (d
Forskere bryder ny vej inden for 3D-printet blød robotteknologi med det største udvalg af polymerh…(a) Illustration af det strukturelle design. (b) Direkte blæk-skrivning af hybridstrukturen. (c) Hærdet struktur (areal på ~90 cm 2 per vinge, membrantykkelse ~0,7 mm, total armtykkelse ~3,5 mm). (d
- Software registrerer bagdørsangreb på ansigtsgenkendelse
- Forskning baner vej for forbedret oprydning af forurenet grundvand
- Sammenlign en mol AG-108 og PT-195 ved hjælp af atomer protoner elektroner neutroner?
- Hvad de tre hovedmasser af vand, der omgiver Irland?
- Hvordan måneskin finjusterer dyrenes reproduktion
- Grafen-baserede terahertz-enheder:Fremtidens bølge


