Forståelse af kovalente bindinger:Hvordan atomer deler elektroner
Wittayayut/iStock/GettyImages
Hvad er en kovalent binding?
En kovalent binding dannes, når to eller flere ikke-metalatomer deler et eller flere par valenselektroner, hvilket skaber en stabil, retningsbestemt forbindelse. At bryde en sådan binding kræver betydelig energi - typisk mellem 50 og 200 kcal/mol - hvilket afspejler dets styrke og den stabilitet, det giver molekylet.
Nøgletræk ved kovalente bindinger
• Kun ikke-metaller (eller metalloider) med lignende elektronegativiteter danner kovalente forbindelser.
• Elektroner deles inden i de yderste skaller, hvilket giver atomerne en fast rumlig orientering.
• Polaritet afhænger af elektronegativitetsforskelle:lige deling giver en ikke-polær kovalent binding; ulige deling producerer en polær kovalent binding.
• På grund af den lave polaritet og den stærke retningsbestemte natur har molekyler med kovalente bindinger ofte lave smelte- og kogepunkter, resterende gasser eller væsker ved stuetemperatur.
Almindelige eksempler på kovalente molekyler
• Metan (CH4 ) – et ikke-polært molekyle, hvor kulstof deler fire ækvivalente elektronpar med brint.
• Saltsyre (HCl) – en polær kovalent binding; klors højere elektronegativitet trækker det delte par mod sig selv.
• Vand (H2 O) – et klassisk polært kovalent molekyle; oxygens stærkere træk skaber et dipolmoment, hvilket giver vandet dets unikke egenskaber.
• Ammoniak (NH3 ) – en polær kovalent forbindelse med en trigonal pyramideformet geometri.
Kontrast med ioniske bindinger
I en ionbinding donerer et metal en eller flere elektroner til et ikke-metal og producerer modsat ladede ioner, der tiltrækker hinanden. Daglige eksempler inkluderer bordsalt (NaCl), fluortandpasta (NaF), rust (Fe2 O3 ), og antacid calciumhydroxid (Ca(OH)2 ).
 Varme artikler
Varme artikler
-
 Låser op for effektiv lys-energikonvertering med stabile koordinationsnanoarkKredit:Hiroshi Nishihara fra Tokyo University of Science To-dimensionelle nanosheets lavet af bindinger mellem metalatomer og organiske molekyler er attraktive kandidater til fotoelektrisk omdanne
Låser op for effektiv lys-energikonvertering med stabile koordinationsnanoarkKredit:Hiroshi Nishihara fra Tokyo University of Science To-dimensionelle nanosheets lavet af bindinger mellem metalatomer og organiske molekyler er attraktive kandidater til fotoelektrisk omdanne -
 At knække sukkerkoden - hvorfor glykomet er den næste store ting inden for sundhed og medicinKredit:molekuul_be/shutterstock.com Når du tænker på sukker, du tænker sikkert på det søde, hvid, krystallinsk bordsukker, som du bruger til at lave småkager eller søde din kaffe. Men vidste du, a
At knække sukkerkoden - hvorfor glykomet er den næste store ting inden for sundhed og medicinKredit:molekuul_be/shutterstock.com Når du tænker på sukker, du tænker sikkert på det søde, hvid, krystallinsk bordsukker, som du bruger til at lave småkager eller søde din kaffe. Men vidste du, a -
 Innovativ forarbejdning og emballering for sikker, høj kvalitet, økologiske bærprodukterKredit:Stanislav Samoylik, Shutterstock I løbet af de sidste to årtier, der har været stigende bekymring for de negative virkninger af konventionelt dyrkede produkter på vores sundhed og miljøet.
Innovativ forarbejdning og emballering for sikker, høj kvalitet, økologiske bærprodukterKredit:Stanislav Samoylik, Shutterstock I løbet af de sidste to årtier, der har været stigende bekymring for de negative virkninger af konventionelt dyrkede produkter på vores sundhed og miljøet. -
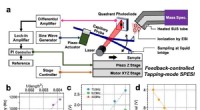 Vil du diagnosticere hjernesygdomme? En massespektrometri -billeddannelse kan en dag hjælpe digFigur 1:(a) Skematisk af målesystemet udviklet i denne undersøgelse. Ved at bruge denne teknologi, udvinding og ionisering af picolitervolumener kan udføres uden forstyrrelser forårsaget af overflader
Vil du diagnosticere hjernesygdomme? En massespektrometri -billeddannelse kan en dag hjælpe digFigur 1:(a) Skematisk af målesystemet udviklet i denne undersøgelse. Ved at bruge denne teknologi, udvinding og ionisering af picolitervolumener kan udføres uden forstyrrelser forårsaget af overflader
- Struktur og binding af brintsulfid?
- Hvordan fungerer en magnetisk sensor?
- Skillevægge:Hvordan immunceller kommer ind i væv
- Nye Grønlandskort viser flere gletsjere i fare
- Amazon -personalestadiet strejker i Tyskland på den store salgsdag
- Supermassiv sort hul-model forudsiger karakteristiske lyssignaler ved kollisionsspids


