Mastering Electron Dot (Lewis)-strukturer:En trin-for-trin guide
Af Kylene Arnold Opdateret 24. marts 2022
Elektronprikstrukturer, også kaldet Lewis-strukturer, er en grafisk repræsentation af den måde, elektroner er fordelt på i en forbindelse. Hvert grundstofs kemiske symbol er omgivet af linjer, der repræsenterer bindinger, og prikker, der repræsenterer ikke-bundne elektroner. Når du tegner en elektronstruktur, er dit mål at gøre hvert elements valens eller ydre elektronskal så fuld som muligt uden at gå over det maksimale antal elektroner for den skal.
Trin 1
Bestem hvert element i strukturen ved at se på dets kemiske formel. For eksempel er kuldioxids formel CO2. Derfor har den et carbonatom og to oxygenatomer.
Trin 2
Slå hvert element op i det periodiske system. Bemærk hver gruppe eller kolonnenummer. Dette afspejler, hvor mange valenselektroner grundstoffet har. For eksempel er carbon i gruppe 4A, og oxygen er i gruppe 6A; derfor har kulstof fire valenselektroner og oxygen har seks.
Trin 3
Tilføj valenselektronerne for alle grundstofferne. Dette er det samlede antal elektroner, der er tilgængelige for prikstrukturen. Da 4 + 6 + 6 =16, vil der være 16 elektroner i kuldioxids Lewis-struktur.
Trin 4
Bestem hvilket grundstof der er det mindst elektronegative eller har det svageste træk på elektronerne ved at se på et elektronegativitetsdiagram eller ved at undersøge grundstoffets position i forhold til de andre grundstoffer i det periodiske system. Elementer stiger generelt i elektronegativitet fra venstre mod højre og fra bund til top. Kulstof er det mindst elektronegative grundstof i forbindelsen med en værdi på 2,5.
Trin 5
Placer det mindst elektronegative element i midten af strukturen, og omgiv det derefter med de andre atomer. Brint har en tendens til at være en undtagelse fra denne regel og er sjældent et centralt atom. Kuldioxids struktur ville begynde sådan her:O C O.
Trin 6
Tegn en lige linje mellem hvert ydre atom og det centrale atom for at repræsentere en enkelt binding. For eksempel O – C – O.
Trin 7
Træk det samlede antal bindingselektroner fra antallet af tilgængelige elektroner. Husk, at hver enkelt binding involverer to elektroner. Da der er to bindinger, der hver indeholder to elektroner, er der 12 flere elektroner tilgængelige for kuldioxidstrukturen.
Trin 8
Placer prikker for at repræsentere de resterende elektroner omkring hvert afsidesliggende atom, indtil dets valensskal er fuld. Brint kræver to elektroner, og ikke-metaller kræver normalt otte.
Trin 9
Tilføj eventuelle resterende elektroner til det centrale atom. Hvis der ikke er nogen elektroner tilbage, men det centrale atom har færre elektroner, end det startede med, indikerer dette, at strukturen endnu ikke er færdig. For eksempel bidrog kulstof kun med en elektron til hvert bundet par. Der er to bundne par, så det tegner sig for to elektroner. Alligevel har kulstof fire valenselektroner. Diagrammet kræver yderligere arbejde.
Trin 10
Opret dobbelt- eller tredobbeltbindinger mellem de centrale og yderliggende atomer, hvis det centrale atoms valensskal ikke er fuld, og par af ikke-bundne elektroner er i nærheden.
Trin 11
Hvis elektronen er en ion, addér eller subtraher antallet af elektroner angivet ved ladningen fra et ikke-bundet par.
Trin 12
Skriv en ladning svarende til antallet af elektroner, du tilføjede eller fratrak ved siden af hvert berørt element.
Ting påkrævet
- Periodisk tabel over elementer
- Elektronegativitetsdiagram
TL;DR (for lang; læste ikke)
Tilføj altid ikke-bundne elektroner i par.
Sidste artikelSådan bestemmes massenummeret for et grundstof
Næste artikelFordele og ulemper ved syntetiske polymerer:En omfattende analyse
 Varme artikler
Varme artikler
-
 Hurtig test til diagnosticering af astmaDet holografiske mikroskop muliggør automatisk, tredimensionel sporing af immunceller i realtid. Kredit:Fraunhofer-Gesellschaft Astma er en af de mest almindelige luftvejssygdomme i verden, påvi
Hurtig test til diagnosticering af astmaDet holografiske mikroskop muliggør automatisk, tredimensionel sporing af immunceller i realtid. Kredit:Fraunhofer-Gesellschaft Astma er en af de mest almindelige luftvejssygdomme i verden, påvi -
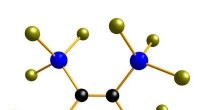 Skræddersyede silicium byggeklodserEn af siliciumbyggestenene, som tillader design af silicium til forskellige anvendelser. Kredit:Wagner-gruppen, Goethe-Universitetet Det brede spektrum af anvendelser for silikoner omfatter medici
Skræddersyede silicium byggeklodserEn af siliciumbyggestenene, som tillader design af silicium til forskellige anvendelser. Kredit:Wagner-gruppen, Goethe-Universitetet Det brede spektrum af anvendelser for silikoner omfatter medici -
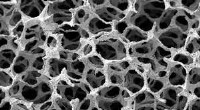 Metallisk skum kan opsuge lyd under højt tryk, miljøer med høje temperaturer såsom jetmotorerEt scanningselektronmikrofotografi af det nikkelbaserede superlegering med åbne celler. Kredit:Singapore Institute of Manufacturing Technology Superlegeringsskum kunne gøre skibs- og flymotorer me
Metallisk skum kan opsuge lyd under højt tryk, miljøer med høje temperaturer såsom jetmotorerEt scanningselektronmikrofotografi af det nikkelbaserede superlegering med åbne celler. Kredit:Singapore Institute of Manufacturing Technology Superlegeringsskum kunne gøre skibs- og flymotorer me -
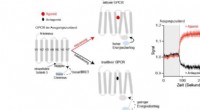 Et skridt foran inden for farmaceutisk forskningNye sensorer gør det muligt at måle aktivering eller deaktivering af GPCRer med high-throughput metoder. Kredit:Grafik:Hannes Schihada Hormoner og andre neurotransmittere, men også stoffer, virker
Et skridt foran inden for farmaceutisk forskningNye sensorer gør det muligt at måle aktivering eller deaktivering af GPCRer med high-throughput metoder. Kredit:Grafik:Hannes Schihada Hormoner og andre neurotransmittere, men også stoffer, virker
- Kaos Hvordan teori virker
- De første resultater af satellitovervågning over havniveau overgår forventningerne
- Er helium en solid væske eller gasrumtemp?
- Hvad er det lag af solens atmosfære, der også kaldes overflade?
- Hvilken type energi er en pindedynamit?
- Sådan bestemmes strømforbrugernes nuværende kapacitet


