Sådan bestemmes massenummeret for et grundstof
Af Chris Deziel | Opdateret 24. marts 2022
PollyW/iStock/GettyImages
TL;DR
Et grundstofs massenummer vises direkte under dets symbol i det periodiske system. Det er udtrykt i atommasseenheder (amu), som er lig med gram pr. mol.
Atomnummer vs. massetal
Hvert grundstof er defineret af dets atomnummer - antallet af positivt ladede protoner i dets kerne. Hydrogen har for eksempel én proton; ilt har otte. Det periodiske system arrangerer grundstoffer ved at øge atomnummeret.
Massetallet er dog det samlede antal protoner plus neutroner i kernen. Da neutroner har nogenlunde samme masse som protoner, men ingen ladning, skal de medtages, når grundstoffets masse beregnes. For eksempel har den mest almindelige isotop af oxygen otte protoner og otte neutroner, hvilket giver den et massetal på 16.
Find massetallet i det periodiske system
Se under symbolet for ethvert grundstof i et velrenommeret periodisk system - dette er massetallet. Du kan muligvis bemærke en decimal, som faktisk er den relative atommasse , det vægtede gennemsnit af alle naturligt forekommende isotoper. Fordi de fleste grundstoffer har flere isotoper, er gennemsnittet sjældent et heltal.
For eksempel angiver det periodiske system brints masse som 1,008, kulstof som 12,011 og oxygen som 15,99. Uran (atomnummer 92) har tre naturlige isotoper, hvilket giver det en relativ masse på 238,029. I rutineberegninger afrunder videnskabsmænd til nærmeste hele tal.
Enheder til masse:The Unified Atomic Mass Unit (amu)
Siden begyndelsen af det 20. århundrede er atommasseenheden (amu) har været standarden. Det er defineret som nøjagtigt en tolvtedel af massen af et isoleret kulstof-12-atom. Derfor er 1 amu lig med 1 gram pr. mol. Derfor vejer ét mol brint 1 gram, ét mol kulstof 12 gram og ét mol uran 238 gram.
Disse definitioner, vedtaget af IUPAC og brugt af NIST, sikrer sammenhæng på tværs af videnskabelig litteratur og kemiske beregninger.
Reference:IUPAC Technical Report, 2021; NIST Chemistry WebBook.
 Varme artikler
Varme artikler
-
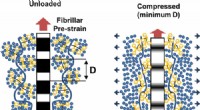 Kollagen i bruskvæv opfører sig som flydende krystaller på en smartphone-skærmKredit:ACS Brusk i vores led indeholder kollagen, som opfører sig lidt som de flydende krystaller på en smartphones skærm, ifølge forskere ved Queen Mary University of London (QMUL). Kollagenet æ
Kollagen i bruskvæv opfører sig som flydende krystaller på en smartphone-skærmKredit:ACS Brusk i vores led indeholder kollagen, som opfører sig lidt som de flydende krystaller på en smartphones skærm, ifølge forskere ved Queen Mary University of London (QMUL). Kollagenet æ -
 Forskere bygger chip til at analysere sundheden for hvide blodlegemerLab-on-a-chip af NTU-forskere, der kan sortere hvide blodlegemer ud og analysere dem for at finde ud af deres sundhedstilstand. Kredit:Nanyang Technological University Forskere fra Nanyang Technol
Forskere bygger chip til at analysere sundheden for hvide blodlegemerLab-on-a-chip af NTU-forskere, der kan sortere hvide blodlegemer ud og analysere dem for at finde ud af deres sundhedstilstand. Kredit:Nanyang Technological University Forskere fra Nanyang Technol -
 Udvikling af cellulær membran-FET (lipid-FET) til følsomhed af biosensorUdfordringer til potentiometriske måleordninger til molekylær detektion på en FET under ionisk miljø:dannelse af EDL, uspecifik binding, og tilfældigt orienterede receptorer. Kredit:Korea Institute of
Udvikling af cellulær membran-FET (lipid-FET) til følsomhed af biosensorUdfordringer til potentiometriske måleordninger til molekylær detektion på en FET under ionisk miljø:dannelse af EDL, uspecifik binding, og tilfældigt orienterede receptorer. Kredit:Korea Institute of -
 Video:Hvad er øjenskorper lavet af?Kredit:The American Chemical Society Stoffet, der ophobes i hjørnerne af dine øjne, mens du sover, har en række forskellige dagligdagse navne:øjenskorpe, søvn, øjestøv. Men hvorfor dukker det op
Video:Hvad er øjenskorper lavet af?Kredit:The American Chemical Society Stoffet, der ophobes i hjørnerne af dine øjne, mens du sover, har en række forskellige dagligdagse navne:øjenskorpe, søvn, øjestøv. Men hvorfor dukker det op
- Hvad er kurveren for jorden?
- Sådan beregner du en halv procent på en Calculator
- Hvilke forbindelser laver planter, når de vokser?
- Hvad er vigtigheden af mesophyllvæv?
- Arbejdsproteiner gør god brug af frustration
- Holdet studerer, hvordan egoistiske gener forårsager mandlig sterilitet i blomstrende planter


