Forståelse af ioniske forbindelser:Dannelse, struktur og egenskaber
alexkich/iStock/GettyImages
TL;DR
Ioniske forbindelser er bygget af ioner, ikke molekyler. Elektroner overføres fra et atom til et andet, hvilket skaber positivt og negativt ladede ioner, der tiltrækker hinanden gennem elektrostatiske kræfter. Denne elektronoverførsel giver stabile, ladede partikler, der danner gitteret af en ionisk forbindelse.
Hvordan ioniske forbindelser dannes
Atomer, der besidder løst fastholdte ydre elektroner - såsom hydrogen, natrium og kalium - kan donere disse elektroner til atomer, der har brug for dem for at færdiggøre deres ydre skaller. Typiske elektronacceptorer omfatter halogener (klor, brom) med syv elektroner i deres yderste skal og oxygen eller svovl, der hver har brug for to elektroner for at opnå en stabil konfiguration.
For eksempel reagerer et natriumatom (Na) med en valenselektron med et kloratom (Cl), der kræver en elektron mere. Natrium donerer sin elektron og bliver til en positivt ladet Na⁺-ion, mens klor vinder elektronen og bliver til en negativt ladet Cl⁻-ion. Den resulterende elektrostatiske tiltrækning mellem Na⁺ og Cl⁻ danner ionbindingen, der udgør natriumchlorid (NaCl).
Tilsvarende kan to kaliumatomer donere i alt to elektroner til et svovlatom, hvilket giver kaliumsulfid (K2S). I hvert tilfælde sikrer overførslen af elektroner, at begge arter opnår fulde ydre skaller og derved stabilisere forbindelsen.
Polyatomiske ioner
Nogle molekyler bliver selv ladede ioner - kendt som polyatomiske ioner - og kan deltage i ionbinding. Et almindeligt eksempel er ammoniumionen (NH4⁺), som dannes, når nitrogen binder kovalent til fire hydrogenatomer, men har en ekstra positiv ladning. Når NH4⁺ støder på sulfidionen (S²⁻), kombineres de og danner ammoniumsulfid ((NH4)₂S). Bindingen mellem NH4⁺ og S²⁻ er ionisk, mens bindingerne i NH4⁺-enheden forbliver kovalente.
Ioniske forbindelsers egenskaber
Ioniske forbindelser udviser karakteristiske træk på grund af deres ladede bestanddele:
- De opløses i vand og opløses i deres bestanddele, hvilket giver dem mulighed for let at deltage i yderligere kemiske reaktioner.
- Fordi ionerne bærer ladning, leder vandige opløsninger af ioniske forbindelser elektricitet.
- Stærke elektrostatiske tiltrækninger resulterer i høje smelte- og kogepunkter.
- Mange ioniske faste stoffer krystalliserer til regelmæssige gitter, som ofte ser hårde og sprøde ud.
At forstå disse egenskaber hjælper kemikere med at forudsige reaktivitet, opløselighed og fysisk opførsel af ioniske materialer.
Sidste artikelSådan vælger du de bedste handsker til sikker brug af acetone
Næste artikelBor:Metalloiden med den mindste atomradius
 Varme artikler
Varme artikler
-
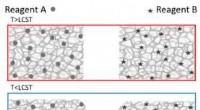 Undersøgelse igangsætter kemiske reaktioner ved at afkøle materialer i stedet for at opvarme demKredit:Vanderbilt University En ny undersøgelse foretaget af Vanderbilt-forskere viser evnen til at igangsætte kemiske reaktioner ved at køle materialer i stedet for at opvarme dem - en kontraintui
Undersøgelse igangsætter kemiske reaktioner ved at afkøle materialer i stedet for at opvarme demKredit:Vanderbilt University En ny undersøgelse foretaget af Vanderbilt-forskere viser evnen til at igangsætte kemiske reaktioner ved at køle materialer i stedet for at opvarme dem - en kontraintui -
 Nyt kunstigt enzym nedbryder sejt, træagtigt lignin:Undersøgelse viser løfte om at udvikle en ny …Woody lignin, set her i renset form, har et betydeligt løfte som et vedvarende biobrændstof, hvis det effektivt kan nedbrydes til nyttig form. Kredit:Andrea Starr | Pacific Northwest National Laborato
Nyt kunstigt enzym nedbryder sejt, træagtigt lignin:Undersøgelse viser løfte om at udvikle en ny …Woody lignin, set her i renset form, har et betydeligt løfte som et vedvarende biobrændstof, hvis det effektivt kan nedbrydes til nyttig form. Kredit:Andrea Starr | Pacific Northwest National Laborato -
 Hvorfor flydende iltspild på asfalt udgør eksplosive farerAf Jack Ori Opdateret 24. marts 2022 Ilt er den livsbærende gas i luften, men når den destilleres og afkøles til kryogene temperaturer, bliver den til en væske. Flydende oxygen (LOX) bruges i raketm
Hvorfor flydende iltspild på asfalt udgør eksplosive farerAf Jack Ori Opdateret 24. marts 2022 Ilt er den livsbærende gas i luften, men når den destilleres og afkøles til kryogene temperaturer, bliver den til en væske. Flydende oxygen (LOX) bruges i raketm -
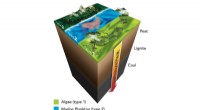 Forskere bruger røntgenstråler til at knække skiferens hemmeligheder, en hjørnesten i en af na…Som vist i denne illustration, som kulstof som det der findes i alger, marine plankton og kystnære landplanter bevæger sig tættere på Jordens kerne, det udsættes for højere temperaturer og tryk, der æ
Forskere bruger røntgenstråler til at knække skiferens hemmeligheder, en hjørnesten i en af na…Som vist i denne illustration, som kulstof som det der findes i alger, marine plankton og kystnære landplanter bevæger sig tættere på Jordens kerne, det udsættes for højere temperaturer og tryk, der æ
- Hvad betyder Bionomy Nomclature?
- Hvad er smeltepunktet og kogepunktet for magnesium?
- Hvordan adskiller stamceller sig fra andre celler?
- Når kræfter, der handler på et bevægende objekt, er det, der vil rejse med konstant hastighed?
- Forklar, hvorfor det er vanskeligt at nøjagtigt repræsentere ammoniak to dimensionelt?
- Anvendelse af ny teknologi til at løse miljømæssige udfordringer


