Sådan tilberedes en natriumkarbonatopløsning:En trin-for-trin guide
Af bidragende skribent — Opdateret 24. marts 2022
Helmut Feil/iStock/GettyImages
Natriumcarbonat (Na₂CO₃), almindeligvis kendt som vaskesodavand, er et uorganisk salt værdsat for dets alsidighed inden for glasfremstilling, elektrokemi, tandpastaformulering og husholdningsrengøring. For at bruge det effektivt skal du forberede opløsninger med en defineret koncentration, enten som en masseprocent eller i molaritet.
Forberedelse af natriumkarbonat derhjemme
Den mest bekvemme måde at fremstille natriumcarbonat på er ved termisk nedbrydning af bagepulver (natriumbicarbonat). Opvarmning af pulveret til temperaturer over 80°C driver reaktionen:
2NaHCO3 → Na2CO3 + CO2 + H2O
Hver 2 mol bagepulver giver 1 mol natriumcarbonat og frigiver kuldioxid og vanddamp. Brug rent glas eller en aluminiumspande, og lad materialet køle af før håndtering.
Oprettelse af en løsning med en ønsket masseprocent
1. Beregn den nødvendige masse af natriumkarbonat
Brug formlen:
Masse (g) =(Volume(L) × %masse) ÷ (100–%masse)
For eksempel at lave en 12 % opløsning i 350 ml vand:
Masse =350×12 ÷ (100–12) =47,73 g
2. Vej natriumcarbonatet
Mål den beregnede mængde på en kalibreret skala.
3. Opløses i vand
Hæld vandet i et bægerglas, tilsæt natriumcarbonatet og rør, indtil det er helt opløst.
Oprettelse af en løsning med en ønsket molaritet
1. Beregn massen af natriumkarbonat
Multiplicer den ønskede molaritet med volumenet i liter og molmassen (106gmol⁻¹):
Masse (g) =Molaritet × Volumen (L) × 106
For en 0,2M opløsning i 300mL:
Masse =0,2 × 0,3 × 106 =6,36 g
2. Vej natriumcarbonatet
Brug en præcis skala til at få den beregnede masse.
3. Tilføj til vand
Begynd med 20-30 ml mindre end det endelige volumen, og tilsæt derefter saltet.
4. Rør til det er opløst
Brug en ske eller forsigtig hvirvling for at sikre fuldstændig opløsning.
5. Juster den endelige lydstyrke
Overfør opløsningen til en målecylinder og fyld op med destilleret vand for at nå målvolumen.
Nødvendige materialer
- Natriumcarbonat (eller bagepulver til produktion)
- Nøjagtig skala
- Bægerglas eller varmebestandig beholder
- Røseske eller magnetomrører
- Destilleret vand
- Klassificeret cylinder
Sikkerhedstip
Selvom natriumcarbonat generelt er sikkert, skal du undgå at indånde støv og bære handsker og øjenbeskyttelse ved håndtering af pulveret eller under termisk nedbrydning.
For detaljerede sikkerhedsdata, se Chemical Safety Database .
 Varme artikler
Varme artikler
-
 Skin et lys:Ny forskning viser, hvordan lavenergilys kan bøje plastikForskere afslørede en måde at bruge lavenergilys til at manipulere fotopolymerer eller plastfilm. Kredit:Florida State University Et hold af Florida State University-forskere har afsløret en måde a
Skin et lys:Ny forskning viser, hvordan lavenergilys kan bøje plastikForskere afslørede en måde at bruge lavenergilys til at manipulere fotopolymerer eller plastfilm. Kredit:Florida State University Et hold af Florida State University-forskere har afsløret en måde a -
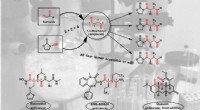 Når svovl forsvinder sporløstNy selektiv syntese af alle 1, 4-dicarbonylisomerer fra sulfoxider og udvalgte vigtige bioaktive forbindelser med 1, 4-dicarbonylmotiv. Kredit:© Maulide Group Mange naturprodukter og lægemidler ha
Når svovl forsvinder sporløstNy selektiv syntese af alle 1, 4-dicarbonylisomerer fra sulfoxider og udvalgte vigtige bioaktive forbindelser med 1, 4-dicarbonylmotiv. Kredit:© Maulide Group Mange naturprodukter og lægemidler ha -
 Naturlige regnbuefarver fremstilles mikrobieltSystemets metaboliske teknik blev anvendt til at konstruere og optimere de metaboliske veje, og membranteknik blev anvendt til at øge produktionen af målfarvestofferne, succesfuldt at producere de s
Naturlige regnbuefarver fremstilles mikrobieltSystemets metaboliske teknik blev anvendt til at konstruere og optimere de metaboliske veje, og membranteknik blev anvendt til at øge produktionen af målfarvestofferne, succesfuldt at producere de s -
 Nyt onlineværktøj til at forbedre cirkulært økodesignKredit:CIRC-PACK Et nyt værktøj er netop blevet lanceret, som giver producenter af emballage (plast og pap) mulighed for at vurdere dens genanvendelighed og cirkulære økonomi-relaterede indikatore
Nyt onlineværktøj til at forbedre cirkulært økodesignKredit:CIRC-PACK Et nyt værktøj er netop blevet lanceret, som giver producenter af emballage (plast og pap) mulighed for at vurdere dens genanvendelighed og cirkulære økonomi-relaterede indikatore
- Ukraines forskere navigerer lockdown for at nå Antarktis
- Hvad er et hastighedsnummer?
- Hvad er kilden til energi i kredsløb?
- Kvantenøglefordeling baseret på kvantesammenfiltring af høj kvalitet
- Håndtering af tumorer med jernoxid
- Hvorfor er radioaktivitet af et element, der ikke påvirkes af de sædvanlige faktorer, der påvirke…


