Hvordan pH-buffere stabiliserer surhed og alkalinitet
Af Carrie Perles
Opdateret 24. marts 2022
Introduktion
En pH-buffer er en omhyggeligt afbalanceret opløsning, der modstår ændringer i surhedsgrad eller basicitet, når små mængder af en syre eller base indføres. Ved at neutralisere overskydende hydrogen- eller hydroxidioner holder det en opløsnings pH-værdi stabil, hvilket gør syrer mindre sure og baser mindre basiske.
Reaktion med en syre
Når en syre kommer ind i en bufferopløsning, fanger buffermolekyler frie hydrogenioner (H⁺). Fordi H⁺-ioner er det, der giver en opløsning dens sure karakter, reduceres den samlede surhedsgrad ved at fjerne dem.
Reaktion med en base
Omvendt, når en base tilsættes, binder buffermolekyler de overskydende hydroxidioner (OH⁻). Eliminering af OH⁻-ioner formindsker opløsningens basicitet og opretholder den ønskede pH.
Betydning for kroppen
Motion accelererer stofskiftet og genererer CO₂ og hydrogenioner, der akkumuleres som mælkesyre i muskelvæv. Disse ændringer kan sænke blodets pH. Normal blod pH er stramt reguleret omkring 7,4; et fald under 6,8 kan være fatalt. Endogene pH-buffere neutraliserer mælkesyre, bevarer en sund blod-pH og sikrer korrekt fysiologisk funktion.
 Varme artikler
Varme artikler
-
 Elastisk polymer, der er både stiv og hård, løser mangeårige problemerEn stærkt sammenfiltret hydrogel (venstre) og en almindelig hydrogel (højre). Kredit:Suo Lab/Harvard SEAS Polymer science har muliggjort gummidæk, Teflon og Kevlar, vandflasker i plast, nylonjakke
Elastisk polymer, der er både stiv og hård, løser mangeårige problemerEn stærkt sammenfiltret hydrogel (venstre) og en almindelig hydrogel (højre). Kredit:Suo Lab/Harvard SEAS Polymer science har muliggjort gummidæk, Teflon og Kevlar, vandflasker i plast, nylonjakke -
 Forskere finder en miljøvenlig måde at farve blå jeans påProcessen med at farve jeans er en af de største kilder til forurening inden for modeindustrien. Ny forskning fandt et mere miljøvenligt alternativ. Kredit:Andrew Davis Tucker/UGA Blusset eller
Forskere finder en miljøvenlig måde at farve blå jeans påProcessen med at farve jeans er en af de største kilder til forurening inden for modeindustrien. Ny forskning fandt et mere miljøvenligt alternativ. Kredit:Andrew Davis Tucker/UGA Blusset eller -
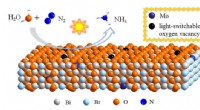 Forbedret omgivende ammoniakfotosyntese ved hjælp af nanosheets med lysomskiftelige iltpladserForskere har præsenteret en strategi ved samtidig at introducere lysomskiftelig ilt-ledighed og dopingmo i Bi 5 O 7 Br nanosheets til effektivt fotokatalytisk N 2 fiksering. Den modificerede fot
Forbedret omgivende ammoniakfotosyntese ved hjælp af nanosheets med lysomskiftelige iltpladserForskere har præsenteret en strategi ved samtidig at introducere lysomskiftelig ilt-ledighed og dopingmo i Bi 5 O 7 Br nanosheets til effektivt fotokatalytisk N 2 fiksering. Den modificerede fot -
 Hurtigere, grønnere måde at producere kulstofkugler påKulissfærer - mikroskopbilleder Hurtig, grøn og et-trins metode til fremstilling af porøse kulstofkugler, som er en vital komponent for kulstoffangstteknologi og for nye måder at lagre vedvarende ener
Hurtigere, grønnere måde at producere kulstofkugler påKulissfærer - mikroskopbilleder Hurtig, grøn og et-trins metode til fremstilling af porøse kulstofkugler, som er en vital komponent for kulstoffangstteknologi og for nye måder at lagre vedvarende ener


