Mastering Buffer Solutions:Trin-for-trin guide til stabile pH-miljøer
Af Carla Boulianne Opdateret 24. marts 2022
Bufferopløsninger modstår ændringer i pH, fordi de indeholder svage syre-base-konjugater, der neutraliserer H+ og OH-ioner. Bufferopløsninger består af svage syrer eller baser og saltet af denne syre eller base. Valg af et passende buffersystem afhænger af pH-området for buffering. De fleste biologiske reaktioner forekommer ved et pH-område på 6 til 8. Fosfatbuffere buffer over pH-området på 6,5 til 7,5. Carboxylsyrebuffere er anvendelige fra pH 3 til 6. Boratbuffere fungerer fra pH 8,5 til 10. Aminosyrebuffere, såsom glycin og histidin, fungerer over en mangfoldighed af pH-områder. Tris buffer er et af de mest brugte buffersystemer i biologiske laboratorier. Beregninger for en Tris bufferopløsning vil blive brugt i det følgende eksempel, men metoden gælder for enhver bufferopløsning.
Trin 1
Brug produktet af den endelige opløsnings molaritet og volumen til at bestemme det nødvendige antal mol base. For eksempel, hvis 2 liter af en 0,1 M opløsning af Tris-buffer er nødvendig, så er antallet af påkrævede mol Tris:
0,1 mol/liter x 2 liter =0,2 mol Tris-base
Trin 2
Beregn den nødvendige buffermasse ved at gange antallet af nødvendige mol med basens molekylvægt. For eksempel er massen af 0,2 mol Tris-base lig med:
0,2 mol Tris x 121,1 g/mol Tris =24,22 g Tris
Trin 3
Mål den passende basemasse på en skala.
Trin 4
Opløs basen i destilleret vand ved hjælp af en magnetisk omrørerstang og omrørende varmeplade. Opløs det i en mængde vand, der kun er lidt mindre end den endelige opløsningsvolumen (950 til 975 ml for hver liter endelig opløsning). Tris-bufferens pH ændres med koncentrationen og skal justeres, hvis der anvendes et for lille initialvolumen. Det er også bedst at forberede bufferen ved den samme temperatur, som den vil blive brugt under analysen eller eksperimentet, da Tris har store temperaturafhængige ændringer i pH.
Trin 5
Titrer den vandige Tris-opløsning med 1 M saltsyre ved hjælp af et pH-meter.
Trin 6
Bring opløsningen til det endelige volumen med destilleret vand i en målekolbe.
Ting påkrævet
- Destilleret vand
- Basispulver eller krystal
- Saltsyre (HCl)
- Klassificeret cylinder
- Volumetrisk kolbe
- Magnetisk rørestang
- Rørende varmeplade
- pH-måler med sonde
- Skala
- Lommeregner
TL;DR (for lang; læste ikke)
For at spare tid, når du forbereder en bufferopløsning, kan du bruge præfabrikerede bufferkoncentrater ved den nødvendige pH og fortyndes til ønsket molaritet og volumen.
Forbered bufferopløsning ved den samme temperatur, som den vil blive brugt for at undgå væsentlige pH-ændringer.
Undgå tidskrævende pH-justeringer, titrér kun efter fortynding til den ønskede koncentration. Opløsning i for lille volumen vil føre til gentagne titreringer.
Advarsel
Udvis forsigtighed ved håndtering af syrer og baser.
Bær beskyttelsesbriller.
 Varme artikler
Varme artikler
-
 Skift dit digitale termometer til Fahrenheit:En trin-for-trin guideAf Heather Laurent | Opdateret 24. marts 2022 Foremniakowski/iStock/GettyImages Uanset om du er kok, læge eller blot hjemmebruger i USA, kan aflæsning af temperaturer i Fahrenheit være mere intuitiv
Skift dit digitale termometer til Fahrenheit:En trin-for-trin guideAf Heather Laurent | Opdateret 24. marts 2022 Foremniakowski/iStock/GettyImages Uanset om du er kok, læge eller blot hjemmebruger i USA, kan aflæsning af temperaturer i Fahrenheit være mere intuitiv -
 Jernbaserede katalysatorer opdaget ved lysdreven kuldioxidhydrogeneringFig. 1. FeOx/Fe til reduktion af CO2 til værditilvækst kulbrinter. Kredit:ZHANG et al. Kinesiske forskere forberedte for nylig en række Fe-holdige katalysatorer fra MgFeAl Layered Double Hydroxide
Jernbaserede katalysatorer opdaget ved lysdreven kuldioxidhydrogeneringFig. 1. FeOx/Fe til reduktion af CO2 til værditilvækst kulbrinter. Kredit:ZHANG et al. Kinesiske forskere forberedte for nylig en række Fe-holdige katalysatorer fra MgFeAl Layered Double Hydroxide -
 Samarbejde giver lovende innovation inden for pletbestandighedPrøver af klud både ubehandlet, venstre, og behandlet med en fluor-fri oleofob belægning udviklet i laboratorier af Emmanuel Giannelis, professor i materialevidenskab og teknik, og Jintu Fan, professo
Samarbejde giver lovende innovation inden for pletbestandighedPrøver af klud både ubehandlet, venstre, og behandlet med en fluor-fri oleofob belægning udviklet i laboratorier af Emmanuel Giannelis, professor i materialevidenskab og teknik, og Jintu Fan, professo -
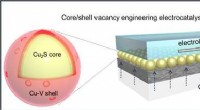 Ny katalysator opgraderer kuldioxid til fundne brændstofferCore/shell-vacancy engineering (CSVE) katalysator muliggør effektiv elektrokemisk reduktion af CO 2 til multi-carbon alkoholer. Kredit:ZHUANG Taotao Flydende multi-carbon alkoholer såsom ethanol
Ny katalysator opgraderer kuldioxid til fundne brændstofferCore/shell-vacancy engineering (CSVE) katalysator muliggør effektiv elektrokemisk reduktion af CO 2 til multi-carbon alkoholer. Kredit:ZHUANG Taotao Flydende multi-carbon alkoholer såsom ethanol
- Hvorfor er ærlighed et spørgsmål om selvtillid til videnskabsmand?
- Behovet for sociale færdigheder hjalp med at forme det moderne menneskelige ansigt
- Hvordan overlever blinde hulefisk deres miljø med lavt iltindhold?
- Når pladetektonik får revner til at dannes?
- Ny drejeskivelignende katalytisk reaktor lover mere bæredygtig kemisk fremstilling
- Hvad er specielle egenskaber ved feltspat?


