Forholdet mellem atmosfærisk tryk og kogepunkt forklaret
smileitsmccheeze/iStock/GettyImages
Når det omgivende lufttryk falder, falder den temperatur, der kræves for, at en væske kan koge. Det er grunden til, at madlavning i høje højder tager længere tid – vand koger ved en lavere temperatur og holder derfor mindre varme, hvilket kræver længere tilberedningstid for at opnå samme grad af færdighed.
TL;DR
Kogepunktet stiger med atmosfærisk tryk. Efterhånden som trykket falder, falder den nødvendige temperatur til kogning, hvilket gør fordampning lettere og kræver mindre varme for at nå kogetilstanden.
Damptryk
Et stofs damptryk er det tryk, som dets damp udøver i ligevægt med dets flydende (eller faste) fase ved en given temperatur. For eksempel, i en forseglet beholder med en halv liter vand ved stuetemperatur, fordamper vandet ind i vakuumet og etablerer et damptryk på omkring 0,03 atm (0,441 psi). At hæve temperaturen øger molekylernes kinetiske energi, og følgelig stiger damptrykket.
Molekylære vibrationer og energifordeling
Alle molekyler vibrerer i tilfældige retninger over det absolutte nulpunkt. Når temperaturen stiger, bliver disse vibrationer hurtigere. Fordelingen af hastigheder er ikke ensartet - nogle molekyler bevæger sig langsomt, mens andre accelererer hurtigt. De hurtigste, når de når overfladen, har nok kinetisk energi til at overvinde intermolekylære kræfter og undslippe ind i gasfasen. Denne selektive flugt er det, der driver fordampningen og hæver damptrykket.
Interaktion mellem damp og atmosfærisk tryk
I et vakuum møder fordampede molekyler ingen modstand og danner frit en damp. I nærvær af luft skal damptrykket imidlertid overstige det omgivende atmosfæriske tryk for at fordampningen kan fortsætte. Hvis damptrykket er lavere end det omgivende tryk, bliver de molekyler, der forlader væskeoverfladen, bombarderet af luftmolekyler og tvunget tilbage i væsken, hvilket undertrykker fordampning.
Kogning under reduceret tryk
En væske begynder at koge, når dens damptryk er lig med det ydre tryk, hvilket tillader dampbobler at dannes og vokse. Ved høje atmosfæriske tryk kan en væske blive ekstrem varm uden at koge, fordi det omgivende tryk forhindrer dampboblerne i at udvide sig. Når det omgivende tryk falder, forhindrer færre kollisioner fra luftmolekyler at undslippe damp. Følgelig når væsken kogende tilstand ved en lavere temperatur, hvilket gør kogningen nemmere og ofte hurtigere under reduceret tryk.
 Varme artikler
Varme artikler
-
 Selvemitterede overfladebølger i dynamisk brud af siliciumenkeltkrystalDynamisk revnefrontadfærd i steady-state (110) spaltning af de enkeltkrystallinske siliciumprøver under ren bøjning. (A) Morfologier af (110) spaltningsplanet (xy-planet) af de as-sawne prøver ved for
Selvemitterede overfladebølger i dynamisk brud af siliciumenkeltkrystalDynamisk revnefrontadfærd i steady-state (110) spaltning af de enkeltkrystallinske siliciumprøver under ren bøjning. (A) Morfologier af (110) spaltningsplanet (xy-planet) af de as-sawne prøver ved for -
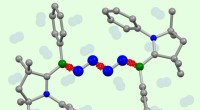 Inert nitrogen tvunget til at reagere med sig selvFor første gang, to molekyler af atmosfærisk nitrogen (blå, midten) er koblet direkte til hinanden i forskning af kemikere fra Würzburg og Frankfurt. Kredit:Dr. Rian Dewhurst / Dr. Marc-André Légaré
Inert nitrogen tvunget til at reagere med sig selvFor første gang, to molekyler af atmosfærisk nitrogen (blå, midten) er koblet direkte til hinanden i forskning af kemikere fra Würzburg og Frankfurt. Kredit:Dr. Rian Dewhurst / Dr. Marc-André Légaré -
 Vedvarende fotokonduktivitet bruges til at stimulere neurotypiske cellerEksponering af GaN for UV-lys forårsager en ophobning af elektroner ved den biologiske grænseflade, selv efter at lyset er fjernet. Dette fænomen, kendt som persistent fotokonduktivitet (PPC), kan bru
Vedvarende fotokonduktivitet bruges til at stimulere neurotypiske cellerEksponering af GaN for UV-lys forårsager en ophobning af elektroner ved den biologiske grænseflade, selv efter at lyset er fjernet. Dette fænomen, kendt som persistent fotokonduktivitet (PPC), kan bru -
 Mestring af vindafkøling:Sådan beregnes den opfattede temperatur nøjagtigtAf Rosann Kozlowski Opdateret 24. marts 2022 Pixfly/iStock/Getty Images Under en vejrmelding midt i en blæsende vinter vil en meteorolog ofte nævne vindafkølingsfaktor sammen med dagens høje og lav
Mestring af vindafkøling:Sådan beregnes den opfattede temperatur nøjagtigtAf Rosann Kozlowski Opdateret 24. marts 2022 Pixfly/iStock/Getty Images Under en vejrmelding midt i en blæsende vinter vil en meteorolog ofte nævne vindafkølingsfaktor sammen med dagens høje og lav
- Hvorfor er det fordelagtigt for organismer som svampe og alger at danne gensidigt forhold?
- Amerikanerne er enige om, at misinformation er et problem, viser meningsmåling
- Strategier til at konstruere metalorganiske rammer til effektiv fotokatalyse
- Hvor findes lavt jordskælv?
- Hvad er 2 anvendelser til metalliske mineraler?
- Blå kulstof:Kan en løsning på klimaudfordringen begraves i fjorddybet?


