Faseovergange:Endotermiske vs. eksoterme energiændringer
Af Riti Gupta, Opdateret 24. marts 2022
Uanset om du koger pasta eller ser frost dannes på et vintervindue, sker der hele tiden faseændringer. Disse overgange – fast, flydende og gas – er ledsaget af absorption eller frigivelse af varme, hvilket gør dem til endoterme eller eksoterme processer.
Energiflow i faseovergange
Hver faseændring involverer et skift i partikelbevægelse og intermolekylær tiltrækning. I et fast stof vibrerer molekyler omkring faste positioner. Når varme tilføres, får de kinetisk energi, bryder gitteret og bevæger sig ind i en væske. Yderligere opvarmning øger molekylær bevægelse, indtil stoffet fordamper.
Vand, med dets stærke hydrogenbindinger, eksemplificerer denne adfærd. Den energi, der kræves for at afbryde disse bindinger under smeltning eller kogning, er grunden til, at vi mærker varmen fra damp eller varmen fra kogende vand.
Endoterme vs. eksoterme processer
Generelt kræver bevægelse fra en mere ordnet til en mindre ordnet tilstand - fast til flydende til gas - varmetilførsel, hvilket gør processen endoterm. Det omvendte, fra gas til flydende til fast, frigiver varme og er eksotermisk.
Oversigt over faseændringer
- Frysning (Væske → Fast):Eksotermisk – varmeafgivet.
- Smeltning (Fast → Flydende):Endotermisk – varmeabsorberet.
- Kondens (Gas → Væske):Eksotermisk – varmeafgivet.
- Fordampning (Væske → Gas):Endotermisk – varmeabsorberet.
- Sublimering (Faststof → Gas):Endotermisk – varmeabsorberet.
- Deponering (Gas → Fast stof):Eksotermisk – varmeafgivet.
Husk:modsatte faseændringer involverer modsatte energistrømme. At kende den ene retning fortæller dig straks den anden.
TL;DR
Mere ordnet til mindre ordnet:eksotermisk. Mindre ordnet til mere ordnet:endotermisk.
 Varme artikler
Varme artikler
-
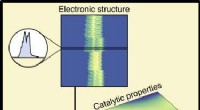 Maskinlæring forbinder materialesammensætning og ydeevne i katalysatorerKredit:University of Michigan I et fund, der kunne være med til at bane vejen mod renere brændstoffer og en mere bæredygtig kemisk industri, forskere ved University of Michigan har brugt maskinlær
Maskinlæring forbinder materialesammensætning og ydeevne i katalysatorerKredit:University of Michigan I et fund, der kunne være med til at bane vejen mod renere brændstoffer og en mere bæredygtig kemisk industri, forskere ved University of Michigan har brugt maskinlær -
 Hvad sker der, når oliedepoter brænder i dagevis efter luftangrebI begyndelsen af marts indikerede rapporter, at amerikansk-israelske luftangreb på iranske mål satte flere olielagre i nærheden af Teheran i brand. Mindst fire depoter blev ramt, hvilket skabte en sto
Hvad sker der, når oliedepoter brænder i dagevis efter luftangrebI begyndelsen af marts indikerede rapporter, at amerikansk-israelske luftangreb på iranske mål satte flere olielagre i nærheden af Teheran i brand. Mindst fire depoter blev ramt, hvilket skabte en sto -
 Materialeforskere skaber stærkere kobolt til brændselscellerKredit:Pacific Northwest National Laboratory Et multiinstitutionelt forskerteam ledet af materialeforskere fra Pacific Northwest National Laboratory (PNNL) har designet en yderst aktiv og holdbar
Materialeforskere skaber stærkere kobolt til brændselscellerKredit:Pacific Northwest National Laboratory Et multiinstitutionelt forskerteam ledet af materialeforskere fra Pacific Northwest National Laboratory (PNNL) har designet en yderst aktiv og holdbar -
 Power dressing:El-producerende, strækbar, selvreparerende materialer til wearablesDen mekaniske og termoelektriske selvhelbredende proces af kompositfilmen. Gengivet med tilladelse fra reference en. Kredit:WILEY-VCH Verlag GmbH Bærbar elektronik kan altid drives af stretchy, se
Power dressing:El-producerende, strækbar, selvreparerende materialer til wearablesDen mekaniske og termoelektriske selvhelbredende proces af kompositfilmen. Gengivet med tilladelse fra reference en. Kredit:WILEY-VCH Verlag GmbH Bærbar elektronik kan altid drives af stretchy, se
- Hvornår løber den elektriske strøm?
- Hvordan reagerer jern med damp, når den opvarmes?
- Har du en drone? Lær lovene, før du tager flyvning
- Hvad er de specielle træk ved ægceller?
- Koalaen:Når det er smart at være langsom
- Seismiske stresskortprofiler inducerede jordskælvsrisiko for West Texas, Ny mexico


