Sådan beregnes molarvarme af fordampning
Fordampningsvarmen er den energi, der er nødvendig for at fordampe en mol væske. Enhederne er som regel kilojoules pr. Mol eller kJ /mol. To mulige ligninger kan hjælpe dig med at bestemme molarvarmen for fordampning. For at beregne molarvarme af fordampning, skriv ned dine givne oplysninger, vælg en ligning, der passer til omstændighederne, og løse ligningen ved hjælp af de givne tryk- og temperaturdata.
Skriv ned dine givne oplysninger. For at beregne dampens molarvarme skal du skrive ned de oplysninger, som problemet giver. Problemet vil enten tilvejebringe to tryk og to temperaturværdier eller den molære varme af sublimering og den molære varme af fusion. Den molære varme af sublimering er den energi, der er nødvendig for at sublimere en mol af et faststof, og den molære varme af fusion er den energi, der er nødvendig for at smelte en mol faststof.
Bestem hvilken ligning der skal bruges. Ved beregning af molarvarme af fordampning skal du bestemme, hvilken ligning du vil anvende ud fra de givne oplysninger. Hvis problemet giver de to tryk og to temperaturværdier, skal du bruge ligningen ln (P1 /P2) = (Hvap /R) (T1-T2 /T1xT2), hvor P1 og P2 er trykværdierne; Hvap er molarvarmen af fordampning; R er gaskonstanten; og T1 og T2 er temperaturværdierne. Hvis problemet giver den molære varme af sublimering og den fusionsmolekylære varme, skal du bruge ligningen Hsub = Hfus + Hvap, hvor Hsub er den molære varme af sublimering og Hfus er den fusionsvarme.
Løs ligning. Hvis du bruger ligningen ln (P1 /P2) = (Hvap /R) (T1-T2 /T1xT2); værdien af gaskonstanten, R, er 8.314 J /Kxmol. For eksempel, hvis P1 = 402mmHg, P2 = 600mmHg, T1 = 200K og T2 = 314K, så er Hvap lig med 1834 J /mol. Derefter deler du dit svar med 1.000, fordi der er 1.000 joules i 1 kilojoule. Svaret bliver så 1,834 kJ /mol. Hvis du bruger ligningen, Hsub = Hfus + Hvap, trækker du Hfus fra Hsub. For eksempel, hvis Hsub = 20 kJ /mol og Hfus = 13 kJ /mol, hvorefter Hvap = 7 kJ /mol.
Sidste artikelSådan beregnes en quintile
Næste artikelDaglig brug af polynomier
 Varme artikler
Varme artikler
-
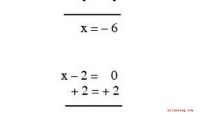 Sådan faktoriseres ligningerFaktoriserende ligninger er et af grundene til algebra. Du kan finde svaret på en kompleks ligning meget nemmere ved at bryde ligningen ned i to simple ligninger. Selv om processen kan virke udfordren
Sådan faktoriseres ligningerFaktoriserende ligninger er et af grundene til algebra. Du kan finde svaret på en kompleks ligning meget nemmere ved at bryde ligningen ned i to simple ligninger. Selv om processen kan virke udfordren -
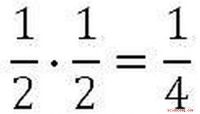 Sådan løser du grundlæggende sandsynlighedsproblemer, der involverer en mønt FlipDette er artikel 1 i en række selvstændige artikler om grundlæggende sandsynlighed. Et fælles emne i indledende sandsynlighed er at løse problemer med møntflip. Denne artikel viser trinene til løsning
Sådan løser du grundlæggende sandsynlighedsproblemer, der involverer en mønt FlipDette er artikel 1 i en række selvstændige artikler om grundlæggende sandsynlighed. Et fælles emne i indledende sandsynlighed er at løse problemer med møntflip. Denne artikel viser trinene til løsning -
 Sådan lærer du matematik med Cuisenaire RodsCuisenaire stænger er et simpelt, men genialt værktøj til undervisning af matematiske relationer til små børn. Oftere anvendt i Europa end USA, blev de først udviklet af belgiske lærer Georges Cuisena
Sådan lærer du matematik med Cuisenaire RodsCuisenaire stænger er et simpelt, men genialt værktøj til undervisning af matematiske relationer til små børn. Oftere anvendt i Europa end USA, blev de først udviklet af belgiske lærer Georges Cuisena -
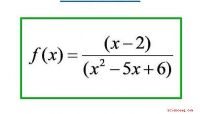 Hvordan man kender forskellen mellem en lodret asymptote og et hul i grafen for en rationel funktion…Der er en vigtig stor forskel mellem at finde den lodrette asymptote (r) af grafen for en rationel funktion og finde et hul i grafen for den funktion. Selv med de moderne grafikregnemaskiner, som vi h
Hvordan man kender forskellen mellem en lodret asymptote og et hul i grafen for en rationel funktion…Der er en vigtig stor forskel mellem at finde den lodrette asymptote (r) af grafen for en rationel funktion og finde et hul i grafen for den funktion. Selv med de moderne grafikregnemaskiner, som vi h


