Opfindelse kan forbedre levering af kræftmedicin, reducere skadelige virkninger af kemoterapi

Xenia Kachur, en kandidatstuderende i det biomedicinske ingeniørvidenskabelige tværfaglige program ved UA, arbejder på et projekt for at levere kemoterapeutiske lægemidler til kræftvæv uden at skade raske kropsceller. (Foto af Beatriz Verdugo)
(PhysOrg.com) - En opfindelse fra University of Arizona forskere kan give en måde at levere kemoterapeutiske lægemidler til kræftvæv i kontrollerede doser uden at skade raske kropsceller.
Forskere fra University of Arizona har muligvis fundet en måde at levere kemoterapeutiske lægemidler til kræftvæv i kontrollerede doser uden at skade raske kropsceller.
Hvis det lykkes, opfindelsen af guldovertrukne liposomer kunne gøre kemoterapi mere effektiv til at ødelægge kræftceller og lindre de skadelige bivirkninger, der kan skyldes behandlingen.
Opfindelsen af Marek Romanowski, en lektor i afdelingen for biomedicinsk ingeniørvidenskab ved Engineering College ved UA, og hans laboratoriehold har ikke en sølvbeklædning. Bedre:Den har en foring af guld. Hemmeligheden ved ikke-invasivt at kontrollere frigivelsen af kemoterapeutiske lægemidler ligger i nanoskala kapsler fremstillet af lipider og belagt med et fint lag guld.
Kemoterapeutiske lægemidler er undertiden indkapslet i små kapsler kaldet liposomer, som er lavet af organiske lipider, der allerede findes i humane celler. Lipidindkapslingen forhindrer kroppens immunsystem i at angribe det fremmede molekyle, før det kan levere stoffet.
Efter frigivelse i blodbanen, lægemiddelbærende liposomer akkumuleres omkring en kræftsvulst på grund af en egenskab kendt som utæt vaskulatur:Tumorceller har ekstra åbninger til blodkar for at optage næringsstoffer transporteret i blodbanen, normalt fordi de forsøger at vokse hurtigere end normale celler. Den ekstra blodgennemstrømning betyder, at flere næringsstoffer, og også flere liposomer, sandsynligvis akkumuleres i tumorcellerne, hvor de til sidst nedbrydes og frigiver lægemidlet til cellerne, fører til celledød.
De meget giftige lægemidler, der bruges til kemoterapi ødelægger kræftceller, men uden mulighed for at skelne mellem celletyper, de kan også skade raske celler. Denne skade på kroppens normale, raske celler fører til de bivirkninger, der normalt er forbundet med kemoterapibehandlinger:anæmi, hårtab, opkastning - da celler, der udgør maveslimhinden, ødelægges - og kvalme, blandt andre.
Nøgler i en lås
For bedre at målrette kræftceller, UA -teamet knyttet liposomer til signalmolekyler kaldet ligander, som interagerer med bestemte celleceptorer som nøgler i en lås.
"Det hele afhænger af den sygdom, vi er målrettet mod, men i tilfælde af tumorceller, de over-udtrykker visse receptorer af flere årsager. Den ene er, at tumorceller formerer sig meget hurtigt, og så overudtrykker de mange næringsstofreceptorer, fordi de vil dele sig hurtigere, "sagde Xenia Kachur, en tredjeårs kandidatstuderende i Biomedical Engineering Graduate Interdisciplinary Program, eller GIDP. De ekstra receptorer gør liposomerne mere tilbøjelige til at låse sig fast og komme ind i tumorceller end normale celler.
Når de nedbrydes, liposomer frigiver medicin bit for bit på en ukontrolleret måde, som muligvis ikke effektivt ødelægger tumorceller. Sagde Sarah Leung, en fjerdeårs kandidatstuderende i biomedicinsk teknik GIDP, der også er i Romanowski-laboratoriet:"Der er en særlig koncentration, hvor du har optimale resultater, så nedenunder, at du ikke har nok af stoffet til at få et godt svar, og over det kan det være endnu mere giftigt. "
Den nye opfindelse kunne give læger mulighed for at kontrollere mængden af medicin frigivet ad gangen, og kun at frigive lægemidlet i tumorområdet, derved beskytte sunde celler mod skader forårsaget af lægemidlet. Det er her guldforingen kommer ind.
Lægemidler belagt med guld
"En egenskab ved guld er, at det kan omdanne nær infrarødt lys til varme, "sagde Kachur." Ved at lægge guld på overfladen af disse liposomer, vi kan derefter sætte en stimulus ind, såsom nær-infrarødt lys. Guldet omdanner lyset til varme, varmen får liposomet til at blive utæt, og så kan det, der virkelig er koncentreret indeni, diffundere ud gennem det utætte liposom. "
"Infrarødt lys trænger det dybeste gennem kroppen, fordi det interagerer mindst med de fleste væv, og det forhindrer også meget af den opvarmning, som din krop [ellers] kan opleve, "sagde Kachur.
Teorien går på, at mængden af infrarødt lys kan varieres for at kontrollere mængden af lægemiddel, der frigives fra de guldbelagte liposomer.
"Ved at bruge mere eller mindre lys, du kan frigive mere eller mindre af stoffet og også sætte tid på svarene, så når du udløser lys, noget stof lækker, du kan udløse det igen og få mere stoflækage, eller du kan vente lidt, lad stoffet sprede sig, gøre sit, derefter aktivere det igen. Det giver mulighed for meget mere frihed med frigivelsesprocessen, "sagde Leung." Ved at have dette meget udløste svar kan du ramme det terapeutiske vindue. "
På trods af øget blodgennemstrømning til tumorceller og ligandernes key-in-lock-virkning, nogle liposomer kan stadig ende inde i raske celler. I det tilfælde, guldbelægningen kan potentielt virke for at forhindre frigivelse af det giftige stof til de raske celler.
Ved selektivt at skinne det infrarøde lys kun i tumorområdet, læger kunne sikre sig, at kun liposomer i tumorområdet er i stand til at frigive stoffet.
"Når du ved, hvor tumorer er, du kan gå videre og pege din lyskilde mod disse områder. Uanset hvad der er tilbage, vil det forlade kroppen eller kan langsomt frigives, men ikke så højt eller så giftigt for niveauer, som det ville være, hvis du bare injicerede stoffet systemisk, "sagde Leung.
Opfindelsen har en anden bonus:"Det guldbelagte liposom er biologisk nedbrydeligt, som er en af de bedste dele af vores system, "sagde Leung. I øjeblikket er der ingen godkendte kemoterapeutiske behandlinger, der gør det muligt at eliminere guldnanostrukturer fra kroppen ved hjælp af kroppens egne mekanismer, sagde Leung.
Nyrer, de organer, der normalt filtrerer affaldsmolekyler ud af blodet, har en grænse for størrelsen af molekyle, de kan filtrere. "På grund af den størrelse det nedbrydes til, vores system skal kunne adskilles via nyrerne, hvilket er virkelig unikt, "sagde Leung.
Der er stadig mange trin, der skal tages for at teste opfindelsen, før den kan bruges til kræftbehandling. Men hvis det lykkes, guldovertrukne liposomer kunne tilvejebringe en metode til at målrette kemoterapeutiske lægemidler mod kræftceller, udløser ikke-invasivt lægemidlets frigivelse ved hjælp af infrarødt lys og giver en naturlig måde for kroppen at filtrere stoffet fra blodbanen.
En dag, kræftpatienter kan potentielt modtage kemoterapibehandlinger med tillid til, at stofferne effektivt vil ødelægge kræftceller, og uden frygt for at lide nogen skadelige bivirkninger.
 Varme artikler
Varme artikler
-
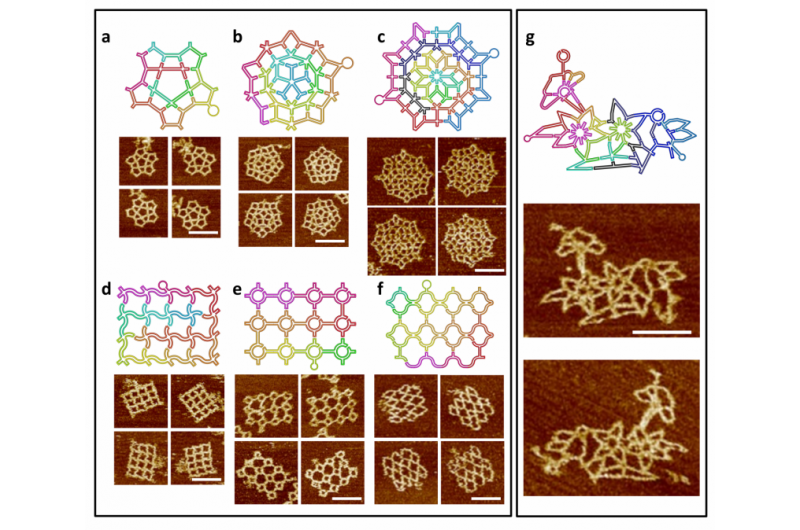 Sjælden form:Nye strukturer bygget af DNA dukker opBillederne viser stilladsfoldningsbanerne for A) stjerneform B) 2-D Penrose flisebelægning C) 8-fold kvasikrystallinsk 2-D mønster D) bølgegitter. E) cirkel array. F) fiskenetmønster G) blomster- og f
Sjælden form:Nye strukturer bygget af DNA dukker opBillederne viser stilladsfoldningsbanerne for A) stjerneform B) 2-D Penrose flisebelægning C) 8-fold kvasikrystallinsk 2-D mønster D) bølgegitter. E) cirkel array. F) fiskenetmønster G) blomster- og f -
 Nanopartikler med en skalstruktur forbedrer ydeevnen af zinkoxidfotodetektorerZinkoxid-nanopartikler med en omhyggeligt styret multi-skal struktur kan fange lys og dermed forbedre ydeevnen af fotodetektorer. Kredit:KAUST Forbedring af lyssensorers følsomhed eller solcelle
Nanopartikler med en skalstruktur forbedrer ydeevnen af zinkoxidfotodetektorerZinkoxid-nanopartikler med en omhyggeligt styret multi-skal struktur kan fange lys og dermed forbedre ydeevnen af fotodetektorer. Kredit:KAUST Forbedring af lyssensorers følsomhed eller solcelle -
 Verdens mindste spiraler kunne beskytte mod identitetstyveriScanning elektronmikroskop billede af en individuel nano-spiral. Kredit:Haglund Lab / Vanderbilt Tag guldspiraler på størrelse med en skilling ... og krymp dem omkring seks millioner gange. Result
Verdens mindste spiraler kunne beskytte mod identitetstyveriScanning elektronmikroskop billede af en individuel nano-spiral. Kredit:Haglund Lab / Vanderbilt Tag guldspiraler på størrelse med en skilling ... og krymp dem omkring seks millioner gange. Result -
 Silicium kan fås til at smelte omvendtEn lille siliciumchip - den glødende orange firkant i midten af denne særlige varmeenhed - opvarmes til en temperatur langt under siliciums smeltepunkt, og derefter meget langsomt afkølet. Chippen i
Silicium kan fås til at smelte omvendtEn lille siliciumchip - den glødende orange firkant i midten af denne særlige varmeenhed - opvarmes til en temperatur langt under siliciums smeltepunkt, og derefter meget langsomt afkølet. Chippen i


