Hvordan guld nanopartikler kan hjælpe med at bekæmpe kræft i æggestokkene
Positivt ladede guldnanopartikler er normalt giftige for celler, men kræftceller formår på en eller anden måde at undgå nanopartikeltoksicitet. Mayo Clinic-forskere fandt ud af hvorfor og fastlagt, hvordan man gør nanopartiklerne effektive mod kræftceller i æggestokkene. Opdagelsen er detaljeret beskrevet i den aktuelle online-udgave af Journal of Biological Chemistry .
"Denne undersøgelse identificerer en ny mekanisme, der beskytter æggestokkræftceller ved at forhindre celledød eller apoptose, som skulle opstå, når de støder på positivt ladede nanopartikler, " siger seniorforfatterne til denne undersøgelse, Priyabrata Mukherjee, Ph.D., en Mayo Clinic molekylærbiolog, og Y.S. Prakash, M.D., Ph.D., en Mayo Clinic anæstesiolog og fysiolog.
Hvorfor kræftceller overlevede
Guld nanopartikler kan have mange medicinske anvendelser, fra billeddiagnostik og hjælp til diagnoser til levering af terapier. I dette tilfælde, ved at bruge et specielt præparat til at sætte positive ionladninger på overfladen, nanopartiklerne er beregnet til at fungere som en målrettet destruktor af tumorceller, mens den efterlader sunde celler alene. Nanopartiklerne formodes at dræbe celler ved at få cellulære calciumionniveauer til at stige. Men forskere opdagede, at et regulatorisk protein i mitokondrierne i det væsentlige bufferer det stigende calcium ved at transportere det ind i mitokondrierne, dermed undergrave celledød. Kræftceller har en overflod af denne transporter og kan således være beskyttet mod nanopartikeltoksicitet.
Forskerholdet opdagede, at hvis de hæmmer calciumoptagelsen i mitokondrierne, tilstrækkelig cellulær stress opbygges, gør guldnanopartiklerne mere effektive til at ødelægge kræftceller.
Forskerne siger, at forståelsen af, hvordan mitokondrielle transportmekanismer fungerer, vil hjælpe med udformningen af målrettede behandlinger mod kræft. De opfordrede nanopartikeludviklere til at integrere denne nye mekanistiske viden i deres processer til at designe nanopartikelegenskaber, der skal bruges i terapi.
 Varme artikler
Varme artikler
-
 Gentest i lægekontoretDenne engangspatron kan detektere genetiske variationer fra blodprøver. DNA isoleres fra hvide blodlegemer og fanges på et objektglas i patronen. Kredit:Nanosphere, Inc. (PhysOrg.com) -- Et bærbar
Gentest i lægekontoretDenne engangspatron kan detektere genetiske variationer fra blodprøver. DNA isoleres fra hvide blodlegemer og fanges på et objektglas i patronen. Kredit:Nanosphere, Inc. (PhysOrg.com) -- Et bærbar -
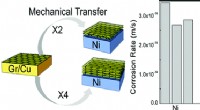 Graphen er den tyndeste kendte antikorrosionsbelægningNy forskning har etableret mirakelmaterialet kaldet grafen som verdens tyndeste kendte belægning til beskyttelse af metaller mod korrosion. Deres undersøgelse af denne potentielle nye brug af grafen v
Graphen er den tyndeste kendte antikorrosionsbelægningNy forskning har etableret mirakelmaterialet kaldet grafen som verdens tyndeste kendte belægning til beskyttelse af metaller mod korrosion. Deres undersøgelse af denne potentielle nye brug af grafen v -
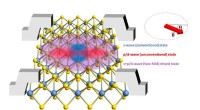 Forskere observerer to gange symmetrisk superledning i 2D niobiumdiselenidForskere har opdaget, gennem elektrontransport og tunnelmålinger (grå kontakter), en blandet konventionel/ukonventionel superledende tilstand i ark af NbSe2 nogle få atomer tykke (blå og gule cirkler)
Forskere observerer to gange symmetrisk superledning i 2D niobiumdiselenidForskere har opdaget, gennem elektrontransport og tunnelmålinger (grå kontakter), en blandet konventionel/ukonventionel superledende tilstand i ark af NbSe2 nogle få atomer tykke (blå og gule cirkler) -
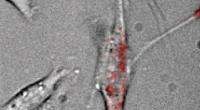 Nanotermometre viser forskelle i første temperaturrespons i levende cellerForskere bruger kvanteprikker (vist med rødt) til at måle temperaturen på levende celler. Kredit:Haw Yang, Ph.D. Ved at bruge en moderne version af åben-vid-og-hold-det-under-din-tungen, forskere
Nanotermometre viser forskelle i første temperaturrespons i levende cellerForskere bruger kvanteprikker (vist med rødt) til at måle temperaturen på levende celler. Kredit:Haw Yang, Ph.D. Ved at bruge en moderne version af åben-vid-og-hold-det-under-din-tungen, forskere
- Brug af maskinlæring til tidlig opdagelse af anomalier hjælper med at undgå skader
- Ingen sukkerbelægning, men sød ikke desto mindre
- Sådan konverteres kubiske fødder til Therms
- Tyskland skyder livestreamet trods indsats fra tech firmaer (opdatering)
- Boeing-kapsel vender tilbage til Jorden efter afbrudt rummission (opdatering)
- Fjernmåling anvendt til at estimere søens klarhed i Kina


