Nanorobot til transport af stoffer i kroppen
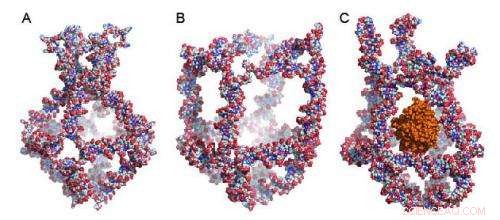
Figuren viser en nanocage, hvor otte unikke DNA-molekyler er blandet sammen. Nanocagen har fire funktionelle elementer, der transformerer sig selv som reaktion på ændringer i den omgivende temperatur. Disse transformationer enten lukker (1A) eller åbner (1B) nanocage. Ved at udnytte temperaturændringerne i omgivelserne, forskerne fangede et aktivt enzym kaldet peberrodsperoxidase (HRP) i nanocage (1C). Kredit:Sissel Juul
En nanorobot er en populær betegnelse for molekyler med en unik egenskab, der gør det muligt at programmere dem til at udføre en bestemt opgave. I samarbejde med kolleger i Italien og USA, forskere ved Aarhus Universitet har nu taget et stort skridt i retning af at bygge den første nanorobot af DNA-molekyler, der kan indkapsle og frigive aktive biomolekyler.
I tide, nanorobotten (også kaldet en DNA nanocage) vil uden tvivl blive brugt til at transportere medicin rundt i kroppen og derved have en målrettet effekt på syge celler.
Design ved hjælp af kroppens naturlige molekyler
Ved hjælp af DNA-selvsamling, forskerne designet otte unikke DNA-molekyler fra kroppens egne naturlige molekyler. Når disse molekyler blandes sammen, de aggregerer spontant i en brugbar form - nanocagen (se figur).
Nanocagen har fire funktionelle elementer, der transformerer sig selv som reaktion på ændringer i den omgivende temperatur. Disse transformationer enten lukker (figur 1A) eller åbner (figur 1B) nanocage. Ved at udnytte temperaturændringerne i omgivelserne, forskerne fangede et aktivt enzym kaldet peberrodsperoxidase (HRP) i nanocage (figur 1C). De brugte HRP som model, fordi dets aktivitet er let at spore.
Dette er muligt, fordi nanocagens ydre gitter har åbninger med en mindre diameter end det centrale sfæriske hulrum. Denne struktur gør det muligt at indkapsle enzymer eller andre molekyler, der er større end åbningerne i gitteret, men mindre end det centrale hulrum.
Forskerne har netop offentliggjort disse resultater i det anerkendte tidsskrift ACS Nano . Her viser forskerne, hvordan de kan udnytte temperaturændringer til at åbne nanocage og tillade HRP at blive indkapslet, før den lukker igen.
De viser også, at HRP bevarer sin enzymaktivitet inde i nanocage og omdanner substratmolekyler, der er små nok til at trænge ind i nanocage til produkter indeni.
Indkapslingen af HRP i nanocage er reversibel, på en sådan måde, at nanocagen er i stand til at frigive HRP igen som reaktion på temperaturændringer. Forskerne viser også, at DNA-nanocagen – med sin enzymbelastning – kan optages af celler i kultur.
Ser på fremtiden, konceptet bag denne nanocage forventes at blive brugt til medicinlevering, som et transportmiddel for medicin, der kan målrette syge celler i kroppen for at opnå en hurtigere og mere gavnlig effekt.
 Varme artikler
Varme artikler
-
 Grafen maler en korrosionsfri fremtidKredit:AlexanderAlUS/Wikipedia/CC BY-SA 3.0 Overfladen af grafen, et etatom tykt ark kulstof, kan tilfældigt dekoreres med ilt for at skabe grafenoxid; en form for grafen, der kan have en betyde
Grafen maler en korrosionsfri fremtidKredit:AlexanderAlUS/Wikipedia/CC BY-SA 3.0 Overfladen af grafen, et etatom tykt ark kulstof, kan tilfældigt dekoreres med ilt for at skabe grafenoxid; en form for grafen, der kan have en betyde -
 Nanopartikelgel forener olie og vand i en fremstillingsvenlig tilgangI modsætning til andre gel-fremgangsmåder, hvor nanopartikler forbliver ved grænsefladen mellem gelens to opløsningsmidler (øverst til venstre), den nye tilgang koncentrerer nanopartikler i det indre
Nanopartikelgel forener olie og vand i en fremstillingsvenlig tilgangI modsætning til andre gel-fremgangsmåder, hvor nanopartikler forbliver ved grænsefladen mellem gelens to opløsningsmidler (øverst til venstre), den nye tilgang koncentrerer nanopartikler i det indre -
 Forskere opdager nyt materiale til køling af elektroniske enhederDette er en skematisk oversigt over termisk styring i elektronik:Lokale temperaturstigninger opstår som følge af strømmen i aktive områder af enheder og kan føre til forringelse af enhedens ydeevne. M
Forskere opdager nyt materiale til køling af elektroniske enhederDette er en skematisk oversigt over termisk styring i elektronik:Lokale temperaturstigninger opstår som følge af strømmen i aktive områder af enheder og kan føre til forringelse af enhedens ydeevne. M -
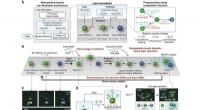 Nanopartikel-baseret computerarkitektur til nanopartikel neurale netværkDen nanopartikel-baserede von Neumann-arkitektur (NVNA) på en lipid nanotablet (LNT) chip. (A) Skematisk af NVNA-LNT. LNTet drives med software sammensat af instruktions-DNAer i opløsning og hardware
Nanopartikel-baseret computerarkitektur til nanopartikel neurale netværkDen nanopartikel-baserede von Neumann-arkitektur (NVNA) på en lipid nanotablet (LNT) chip. (A) Skematisk af NVNA-LNT. LNTet drives med software sammensat af instruktions-DNAer i opløsning og hardware
- Hvordan man opbygger en armillær sphere
- Sådan finder du Southern Cross Constellation
- Tetrapod nanokrystaller lyser vejen til stærkere polymerer
- Landaftaler, der skal forbedre fødevaresikkerheden, kan have skadet
- Sådan evalueres triggefunktioner uden en lommeregner
- Klimaændringer er større trussel end COVID:Røde Kors


