Bevæbning af nanopartikler til kræftdiagnose og behandling
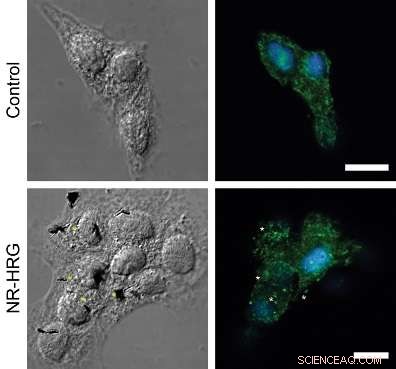
Figur:ErbB2 receptor klynge ved HRG -nanorod binding til MCF7 celler. Konfokale mikrografer, der viser et dorsalt afsnit af målrettede (bundpanel) og ikke-målrettede (øverste panel) MCF7-celler. ErbB2 -receptorer (grøn) blev immunfarvet uden at permeabilisere plasmamembranen. Kerner blev farvet med Hoechst 33342 (blå). Stjerner angiver eksempler på ErbB2 -receptorklynger, der er i nærheden af nanoroder.
UCD -forskere har med succes manipuleret nanopartikler til at målrette mod to humane brystkræftcellelinjer som et værktøj til kræftdiagnose og behandling.
Belægning af nanopartikler med forskellige stoffer gør det muligt at indstille deres interaktion med celler på en bestemt måde. For eksempel, brug af en optisk aktiv partikel som guld (Au) vil give fremragende kontrast i nær infrarød (NIR) billeddannelse og, hvis opvarmet, faktisk kan ødelægge det omgivende væv. Dette kaldes fototermisk ablationsterapi. Magnetisk aktive partikler som jern (Fe) kan muliggøre fysioterapier ved at generere varme, når de udsættes for skiftevis magnetiske felter, der forårsager celledød (magnetisk hypertermi).
UCD -teamet ledet af Conway Fellows, Professor Gil Lee på School of Chemistry and Chemical Biology og professor Walter Kolch i systembiologi Irland, syntetiserede nanoroder med et langt jernsegment belagt med polyethylenglycol og en kort guldspids belagt med et enkelt lag af proteinet, heregulin (HRG).
HRG er en vækstfaktor, der binder til og aktiverer ErbB -familien af proteinreceptorer. ErbB2 er overudtrykt i visse brystkræftformer og forbundet med dårlig prognose. Imidlertid, ErbB2 -overekspression fører til øget følsomhed over for visse lægemidler. Teamet mener, at Fe-Au funktionaliserede nanoroder, der bruges sammen med disse lægemidler, kan være nyttige i kræftbehandling.
Efter karakterisering og tuning af nanorodernes interaktion med cellerne, forskergruppen vurderede, hvordan cellerne reagerer på mekanisk stimulering. At gøre dette, de integrerede en elektromagnetisk pincet med et optisk mikroskop og brugte en ny mikrofluid -chip til at overvåge interaktionen mellem individuelle nanoroder med to humane brystkræftcellelinjer, der udtrykker ErbB -familien af receptorer med forskellige hastigheder. Når HRG-nanoroderne binder sig til kræftceller, der udtrykker ErbB, de starter en kaskade af signalhændelser, der fører til celledød.
"Brug af magnetisk pincet til at strække celler, vi var i stand til yderligere at aktivere cellesignaleringsveje for at udløse celledød. Dette var endnu mere effektivt til at forårsage kræftcelledød end magnetisk hypertermi, den anden terapeutiske tilgang, vi vurderede ", forklarede Dr. Devrim Kilinc, første forfatter og forsker i Lee -gruppen.
"Resultaterne er en positiv indikation for nanoskala -målretning og lokaliseret manipulation af kræftceller med en specifik receptorprofil."
 Varme artikler
Varme artikler
-
 Slukker verdens vand- og energikriser, en lille dråbe ad gangenEn bille i Namib-ørkenen i Afrika bruger sin teksturerede ryg til at samle drikkevand fra den tågefyldte morgenvind. Hvis forskere kan udføre noget billebiomimik, det ville betyde en ny kilde til vand
Slukker verdens vand- og energikriser, en lille dråbe ad gangenEn bille i Namib-ørkenen i Afrika bruger sin teksturerede ryg til at samle drikkevand fra den tågefyldte morgenvind. Hvis forskere kan udføre noget billebiomimik, det ville betyde en ny kilde til vand -
 Verdens mindste vielsesringeVerdens mindste vielsesringe er bygget op af to sammenkoblede DNA-tråde. Kredit:Alexander Heckel Oprettelse af kunstige strukturer fra DNA er målet med DNA -nanoteknologi. Denne nye disciplin, som
Verdens mindste vielsesringeVerdens mindste vielsesringe er bygget op af to sammenkoblede DNA-tråde. Kredit:Alexander Heckel Oprettelse af kunstige strukturer fra DNA er målet med DNA -nanoteknologi. Denne nye disciplin, som -
 Sweet spot i sødt materiale til brintlagringTusinder af timers beregninger på Rice Universitys to hurtigste supercomputere fandt ud af, at den optimale arkitektur til at pakke brint ind i hvid grafen involverer at lave skyskraberlignende rammer
Sweet spot i sødt materiale til brintlagringTusinder af timers beregninger på Rice Universitys to hurtigste supercomputere fandt ud af, at den optimale arkitektur til at pakke brint ind i hvid grafen involverer at lave skyskraberlignende rammer -
 En teknik til at skabe sub-10-nm grafen nanobånd fra knuste kulstof nanorørFigur, der illustrerer den strukturelle ændring i CNTer før og efter højtryks- og termisk behandling, hvor de uberørte CNTer klemmes til GNRer efter tryk/termisk behandling. Skematisk diagram af squas
En teknik til at skabe sub-10-nm grafen nanobånd fra knuste kulstof nanorørFigur, der illustrerer den strukturelle ændring i CNTer før og efter højtryks- og termisk behandling, hvor de uberørte CNTer klemmes til GNRer efter tryk/termisk behandling. Skematisk diagram af squas
- Edmunds samler de seneste pickupper i fuld størrelse
- Forskere lister 50 udtryk, som du måske forvirrer
- Ultratynde designermaterialer låser op for kvantefænomener
- Ødelægger havstigninger husværdier ved kysten? Svaret:Måske
- EU-forbrugerchef utålmodig med Facebook over data
- En undersøgelse viser væksttendenser for kvindelige mordofre i Spanien, der strækker sig over et …


