Kronetere flader i grafen for stærk, specifik binding

Dette ark med grafen indeholder en række kronethere, der stærkt kan binde udvalgte gæstioner eller molekyler. Kredit:Oak Ridge National Laboratory
Ethers - simple organiske molekyler, hvor et oxygenatom bygger bro mellem to carbonatomer - er de kemiske byggesten i almindelige produkter, herunder mange opløsningsmidler, drivmidler, kosmetik og lægemidler. Forbind dem sammen i store molekylringe, og de bliver til videnskabelig royalty - kroneethermolekyler, hvis udvikling i høj grad førte til Nobelprisen i kemi i 1987. Disse kroneformede ringe er vigtige som den oprindelige prototype i vært-gæstkemi, et felt, hvor "gæst" -ioner og -molekyler kan fanges i hulrummet af et "vært" -molekyle. Denne evne giver kemikere mulighed for at organisere en samling af separat svage bindingsinteraktioner, såsom den elektrostatiske binding mellem et ether oxygenatom og en metalion, at opnå stærk, selektiv binding. Denne nyttige ejendom, kaldet "molekylær genkendelse, "er ansat til adskillelser, sensing og katalyse.
Nu har et team ledet af Department of Energy's Oak Ridge National Laboratory fundet en måde at dramatisk øge kroneternes selektivitet og bindingsstyrke. Forskerne har inkorporeret dem inden for en stiv ramme af grafen-ultra stærkt og let et-atom-tykt carbon, der er en stor ting i sig selv (det var emnet for Nobelprisen i fysik i 2010).
"Vi er de første til at se kronetere i grafen, "sagde Matthew Chisholm, som leder Scanning Transmission Electron Microscopy Group i ORNL's Materials Science and Technology Division og fokuserer på karakterisering af materialer. "Vores beregninger baseret på disse observationer indikerer hidtil uset selektivitet og bindingsstyrke."
Indarbejde kroneetere i grafen, som er et stift ark på grund af bikagearrangementet af dets carbonatomer, tvinger etherringene til at ligge fladt. Resultatet er stive huller, der optimerer selektiviteten for atomer af størrelser, der bedst passer til ringhulrum. I øvrigt, at begrænse kronerne i to dimensioner tvinger alle deres iltdipoler til at pege indad, mod hullerne, optimering af det elektrostatiske potentiale for bindingsatomer. For eksempel, styrken, hvormed en kroneether binder et kaliumatom, er tre gange større i sit begrænsede, stiv tilstand på grafen end i en ubegrænset struktur.
Resultaterne, offentliggjort i 13. november -udgaven af Naturkommunikation , kan indvarsle en ny regeringstid for kroneethere i forskellige anvendelser. Deres stærke, specifik elektrostatisk binding kan fremskynde sensorer, kemiske separationer, oprydning af atomaffald, ekstraktion af metaller fra malme rensning og genbrug af sjældne jordarter vandrensning, bioteknologi, energiproduktion i holdbare lithium-ion-batterier, katalyse, medicin og datalagring.
Molekylær genkendelse
Størrelsen og formen af hulrummet, der dannes i et kroneethermolekyle, giver selektivitet for komplementære ioner og små molekyler, der passer til det, som en lås og nøgle. Kronetere findes i forskellige størrelser, så de kan rumme ioner med forskellige diametre. I en kroneeter, de elektriske dipolmomenter for C – O – C ethergrupperne, når de er organiseret omkring en fanget gæstmetalion, giver et stort elektrostatisk potentiale for binding af ion i ringhulen. Værten kan derefter transportere gæsten til steder, den normalt ikke kunne gå, såsom gennem cellemembraner. Den kendsgerning, at kun gæstionen kan transporteres på den måde, gør kroneethere særligt nyttige inden for videnskab og teknologi.
Forskere har undersøgt den samordnede elektrostatiske binding af kroneetherværter til deres ioniske gæster i 50 år. Fordi kronethers molekylære genkendelsesegenskaber efterligner de selektive molekylære transportegenskaber af biologiske proteiner, en ny forståelse af farmaceutisk funktion er blevet mulig med spændende medicinske anvendelser. Inden for industriel teknologi, vært -gæst -kemi kan bruges i lille skala til analyse af sporioner i vandige vandløb og i stor skala til at fjerne forurenende stoffer (f.eks. radioaktivt cæsium) fra affald. Fordi kronetere er selektive, de bruges nu til metalseparationer og har allerede hjulpet med at rydde op i millioner af gallon af gammelt atomaffald.
Men et problem har forhindret kronetere i at realisere deres fulde potentiale i denne og andre applikationer:Traditionelle kronetere er ekstremt fleksible. De snor sig og vrides konstant - millioner af gange hvert sekund i løsning. På grund af fleksibiliteten, a crown ether molecule can adjust the size and shape of its cavity to accommodate a range of sizes and shapes of guests, limiting the crown ether's selectivity. Despite their flexibility, crown ethers surprisingly cannot adopt an optimal shape to bind guest ions, limiting the strength of their binding. Their oxygen atoms point in a three-dimensional zigzag pattern in which the C–O–C dipoles do not point directly at the guest, resulting in far weaker binding than is often desired.
The graphene crown ethers' new flattened, rigid state means they have no flexibility. "Their perfect rigidity is something we almost never see in molecular systems, especially among the traditional crown ethers, "sagde Bruce Moyer, leader of ORNL's Chemical Separations Group. "The oxygens are held in place. There is no way graphene is going to twist. Traditional crown ethers have dipoles that do not point directly at the metal, but the dipoles of the crown ethers in graphene point directly at the guest ion. Graphene thus gives you both enhanced selectivity and enhanced binding for metal ions that fit the crown ether cavity."
Added Moyer, "Such selectively enhanced binding allows you to do much more challenging separations in principle." One example might be mining lithium, an element important in batteries for electric vehicles, from sea water, where it is present in low concentrations.
Such industrial applications would require scaling up production of the graphene crown ethers. Initial research would require moles, an amount of crown ethers equivalent to the number of atoms in 12 grams of carbon-12 (i.e., Avogadro's number, or 6.023 x 10 23 ).
"If we have a mole of holes, that's enough to do bulk chemistry, " Moyer said. "Now we've got to figure out how to make a mole of holes."
Building a better atom trap
ORNL researchers used a chemical approach to produce graphene. Cristian Contescu and Nidia Gallego started with graphite, oxidized it to form graphene oxide and then reduced that to form graphene. Because reduction never gets rid of all the oxygen, the oxygen that remains must be very strongly bonded to carbon atoms. When oxygens and carbons alternate around the rim of a hole in the graphene, crown ethers form in the rigid material.
Chisholm and Junjie Guo, a former postdoctoral researcher at ORNL, used scanning transmission electron microscopy and electron energy loss spectroscopy to reveal the atomic positions, local composition and local electronic properties in the oxidized graphene. Moyer, who shared expertise on crown ethers, said he "can hardly wait till we can demonstrate the unprecedented selectivity of the graphene crown ethers in extracting metal ions from solution."
ORNL's Jaekwang Lee, at Vanderbilt University during the study, and Sokrates Pantelides, who holds joint appointments at Vanderbilt and ORNL, used the VASP program on a supercomputer at the National Energy Research Scientific Computing Center (a DOE Office of Science User Facility at Lawrence Berkeley National Laboratory) to perform density-functional theory calculations of graphene sheets functionalized by crown ethers. The calculations revealed the binding properties of planar crown ethers.
The team will continue to explore the behavior of rigid crown ethers. "We're starting from ground zero, " Chisholm said. "We have seen these crown ether structures in graphene oxide, and now we have to show that they can be made and used."
Future challenges include reproducibly making holes of uniform size (Chisholm has done this with an electron beam, but the approach is too time-consuming to work at large scale) and isolating and specifically placing single atoms in structures.
DOE's Office of Science sponsored the research, which used resources at the Center for Nanophase Materials Sciences, a DOE Office of Science User Facility at ORNL.
UT-Battelle manages ORNL for DOE's Office of Science. The single largest supporter of basic research in the physical sciences in the United States, the Office of Science is working to address some of the most pressing challenges of our time.
 Varme artikler
Varme artikler
-
 Fremstilling af komplekse 3D metalliske strukturer i nanoskala muliggjortFremstilling af mange objekter, maskiner, og enheder omkring os er afhængige af den kontrollerede deformation af metaller ved industrielle processer såsom bøjning, klipning, og stempling. Kan denne te
Fremstilling af komplekse 3D metalliske strukturer i nanoskala muliggjortFremstilling af mange objekter, maskiner, og enheder omkring os er afhængige af den kontrollerede deformation af metaller ved industrielle processer såsom bøjning, klipning, og stempling. Kan denne te -
 Nanodecoy-terapi binder og neutraliserer SARS-CoV-2-virusTransmissionselektronmikrografi af SARS-CoV-2-viruspartikler, isoleret fra en patient. Billede taget og farveforbedret på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Kredit:NIAI
Nanodecoy-terapi binder og neutraliserer SARS-CoV-2-virusTransmissionselektronmikrografi af SARS-CoV-2-viruspartikler, isoleret fra en patient. Billede taget og farveforbedret på NIAID Integrated Research Facility (IRF) i Fort Detrick, Maryland. Kredit:NIAI -
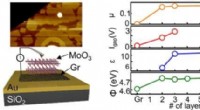 Epitaksialt dyrket molybdænoxid udvikler sig som et bulk-lignende 2-D dielektrisk lagKredit:Seoul National University 3 eV har været påkrævet for UV-relaterede optoelektroniske enheder, kraftelektronik, og dielektriske lag. En af de lovende kandidater er overgangsmetaloxider (TMO
Epitaksialt dyrket molybdænoxid udvikler sig som et bulk-lignende 2-D dielektrisk lagKredit:Seoul National University 3 eV har været påkrævet for UV-relaterede optoelektroniske enheder, kraftelektronik, og dielektriske lag. En af de lovende kandidater er overgangsmetaloxider (TMO -
 Opbygning af nanomaterialer til næste generation af computereNanoforskere ved Northwestern University har udviklet en plan til at fremstille nye heterostrukturer fra forskellige typer 2-D materialer. Forskerne beskriver deres plan i Journal of Applied Physics
Opbygning af nanomaterialer til næste generation af computereNanoforskere ved Northwestern University har udviklet en plan til at fremstille nye heterostrukturer fra forskellige typer 2-D materialer. Forskerne beskriver deres plan i Journal of Applied Physics
- Spildevand har ikke signifikant ændret seismisk stressretning i det sydlige Kansas
- Seks skyer bør du vide om - og hvad de kan afsløre om vejret
- Brasiliens Petrobras nægter at tanke iranske skibe på grund af amerikanske sanktioner
- Rapport:Klimaændringer betyder mindre sne for Yellowstone
- Forskere rapporterer haptisk interface til mobil teknologi
- NASA ser orkanen Jose mellem Bahamas og Bermuda


