Hurtig indfangning af kræftmarkører hjælper med at diagnosticere og behandle
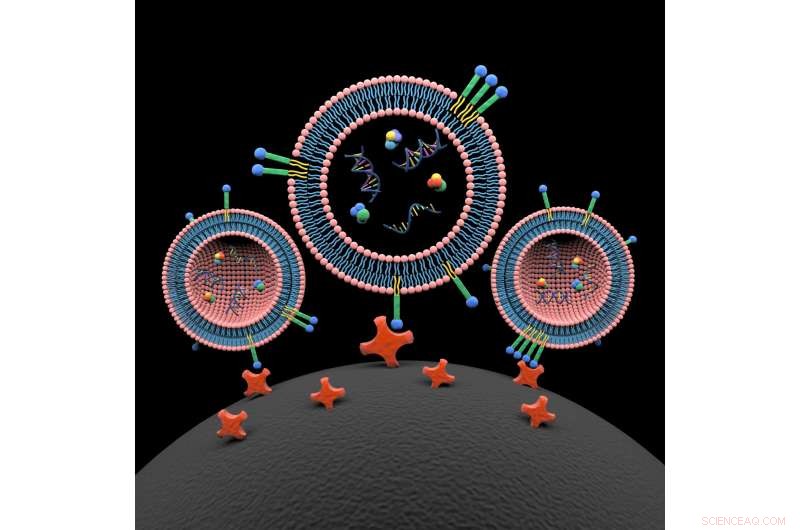
Lipid nanoprober (blå, grøn og gul farvet) indsættes spontant i lipiddobbeltlag af tre ekstracellulære vesikler. Lastindholdet i ekstracellulære vesikler omfatter proteiner, DNA og RNA. De lipid nanoprobe-mærkede ekstracellulære vesikler fanges på overfladen af en magnetisk perle (sort, bund) gennem interaktion med konjugerede avidinmolekyler (rød). Eksosomisolering og dens lastanalyse giver nye muligheder for en bred vifte af molekylære analyser, herunder mutationspåvisning fra blodplasma fra cancerpatienter. Kredit:Xin Zou/Penn State
Et nanoskalaprodukt af menneskelige celler, der engang blev betragtet som junk, er nu kendt for at spille en vigtig rolle i intercellulær kommunikation og i mange sygdomsprocesser, herunder kræftmetastaser. Forskere ved Penn State har udviklet nanoprober til hurtigt at isolere disse sjældne markører, kaldet ekstracellulære vesikler (EV'er), til potentiel udvikling af præcise kræftdiagnoser og personlige kræftbehandlinger.
"De fleste celler genererer og udskiller ekstracellulære vesikler, " siger Siyang Zheng, lektor i biomedicinsk teknik og elektroteknik. "Men de er svære for os at studere. De er sub-mikrometer partikler, så vi har virkelig brug for et elektronmikroskop for at se dem. Der er mange tekniske udfordringer i isoleringen af elbiler i nanoskala, som vi forsøger at overvinde til point-of-care cancerdiagnostik."
På én gang, forskere mente, at elbiler var lidt mere end affaldssække, der blev smidt ud af celler. For nylig, de er kommet til at forstå, at disse små fedtindkapslede sække – lipider – indeholder dobbeltstrenget DNA, RNA og proteiner, der er ansvarlige for at kommunikere mellem celler og kan bære markører for deres oprindelsesceller, inklusive tumorceller. I tilfælde af kræft, mindst én funktion for elbiler er at forberede fjernt væv til metastaser.
Holdets første udfordring var at udvikle en metode til at isolere og rense elbiler i blodprøver, der indeholder flere andre komponenter. Brug af flydende biopsi, eller blodprøver, for kræftdiagnose er en nylig udvikling, der giver fordele i forhold til traditionel biopsi, hvilket kræver at man fjerner en tumor eller stikker en nål ind i en tumor for at udvinde kræftceller. Til lungekræft eller hjernekræft, sådanne invasive teknikker er vanskelige, dyrt og kan være smertefuldt.
"Ikke-invasive teknikker såsom flydende biopsi er at foretrække til ikke kun påvisning og opdagelse, men også til overvågning af behandlingen, " siger Chandra Belani, professor i medicin og vicedirektør for Kræftinstituttet, Penn State College of Medicine, og klinisk samarbejdspartner på undersøgelsen.
"Vi opfandt et system af to mikro/nano materialer, " siger Zheng. "Den ene er en mærkningsprobe med to lipidhaler, der spontant indsættes i lipidoverfladen af den ekstracellulære vesikel. I den anden ende af sonden har vi et biotinmolekyle, der vil blive genkendt af et avidinmolekyle, vi har knyttet til en magnetisk perle. "
De overflademodificerede magnetiske perler er 400 til 500 nanometer i diameter, og mærkningsproberne er i størrelsesordenen 10 nanometer. Når systemet er optimeret, forskerne kan isolere elbilerne fra blodplasmaprøver på cirka 15 minutter. Elbilerne og deres indhold kan derefter analyseres i et laboratorium eller sendes til et kommercielt diagnostisk laboratorium for at karakterisere DNA'et, RNA og proteiner.
I et papir, der blev offentliggjort online i dag, 10. april, og som forsideartikel for april i Natur Biomedicinsk teknik , hovedforfatter Yuan Wan, en postdoktor i Zhengs laboratorium, beskriver brugen af nanoproberne til at fange elbiler fra blodplasmaet fra 19 patienter med ikke-småcellet lungekræft.
"Hjælpet med denne nye tilgang, Vi har med succes isoleret elbiler fra 19 patienter med fremskreden lungekræft og identificeret DNA-mutationer, der kan vejlede præcisionsterapi i stedet for rutinemæssig kemoterapi, " siger Wan. "Fra at indsamle blod til at få EV-afledt DNA, hele proceduren kan afsluttes inden for en time. Det kræver kun en magnet og en fælles bordcentrifuge. Sammenlignet med gængse metoder, nanoprobe -systemet ville i høj grad lette klinisk laboratorieundersøgelse. "
Fordi teknologien kun kræver materialer og en ekstern magnet, det er relativt billigt og hurtigt sammenlignet med den nuværende guldstandard for adskillelse, kaldet ultracentrifugering, som kræver dyrt udstyr og tager timer at gennemføre.
Når først valideret i en større undersøgelse, Zheng og Belani mener, at denne teknik ikke kun kan anvendes på lungekræft, men også på de fleste, hvis ikke alle solide tumorer, som er ansvarlige for 80-90 procent af kræftdødsfaldene.
"Sekvensering af DNA isoleret fra elbiler vil tjene som et lovende værktøj til at spore kræftudvikling og overvåge tumordynamik med det ultimative mål at forbedre kræftoverlevelse, " slutter Belani.
 Varme artikler
Varme artikler
-
 Grafen baner vejen for et nyt produkt, der gør det muligt for industrielle brugereKredit:National Physical Laboratory NPL, Chalmers Tekniske og Grafiske Universitet, har demonstreret den langsigtede stabilitet af epigrafen kvante Hall-chippen, som repræsenterer et vigtigt skrid
Grafen baner vejen for et nyt produkt, der gør det muligt for industrielle brugereKredit:National Physical Laboratory NPL, Chalmers Tekniske og Grafiske Universitet, har demonstreret den langsigtede stabilitet af epigrafen kvante Hall-chippen, som repræsenterer et vigtigt skrid -
 Nyt system ændrer formen på ting, der kommer i biomolekylær leveringfugleperspektiv af guldpyramiderne set gennem et nærfeltsscanningsoptisk mikroskop. Dette billede bekræftede, hvad simuleringen forudsagde:når laseren exciterede overfladeplasmonerne, nærfeltsforstærk
Nyt system ændrer formen på ting, der kommer i biomolekylær leveringfugleperspektiv af guldpyramiderne set gennem et nærfeltsscanningsoptisk mikroskop. Dette billede bekræftede, hvad simuleringen forudsagde:når laseren exciterede overfladeplasmonerne, nærfeltsforstærk -
 Forskere diskuterer den fremtidige virkning af nutidens nanoteknologiske forskningTeri Odom og Chad Mirkin fra International Institute for Nanotechnology. Kredit:Northwestern University Verdenskendte nanovidenskabsmænd og kemikere Chad Mirkin, direktøren for International Insti
Forskere diskuterer den fremtidige virkning af nutidens nanoteknologiske forskningTeri Odom og Chad Mirkin fra International Institute for Nanotechnology. Kredit:Northwestern University Verdenskendte nanovidenskabsmænd og kemikere Chad Mirkin, direktøren for International Insti -
 Ultratynde sølvfilm og litografisk mønstrede strukturer for at forbedre plasmonisk ydeevneUdjævningseffekten af en gasklynge -ionstråle (lilla) på en ru overflade (grå). Kredit:A*STAR Institute of Materials Research and Engineering Plasmoniske enheder - såsom superlinser, hyperlinser
Ultratynde sølvfilm og litografisk mønstrede strukturer for at forbedre plasmonisk ydeevneUdjævningseffekten af en gasklynge -ionstråle (lilla) på en ru overflade (grå). Kredit:A*STAR Institute of Materials Research and Engineering Plasmoniske enheder - såsom superlinser, hyperlinser
- Nye materialer gennemgår fast-flydende faseovergange ved stuetemperatur
- Ny model finder, at lande bør arbejde sammen om at kontrollere coronavirus, skadelige arter
- Afsløring af fejl i metrics for brugerloginsystemer
- Benzinkrise kræver gensidig tillid mellem politiske beslutningstagere, forbrugere og leverandører
- Registrer afstand for alternativ superstrøm
- Hvilke skyer er forbundet med en forkølelse?


