At gøre fartøjer utætte efter behov kan hjælpe med medicinafgivelse

Fluorescerende jernoxid-nanopartikler lyser i endotelceller i et eksperiment på Rice University. Til venstre, nanopartiklerne er jævnt fordelt blandt mikrotubulierne, der er med til at give cellerne deres form. Til højre, efter at et magnetfelt er påført, nanopartiklerne trækkes mod den ene ende af cellerne og ændrer deres form. Forskerne mener, at dette tilbyder en måde at gøre endotelbarrieren "utæt" nok til at tillade lægemiddelmolekyler at passere igennem for at nå væv. Kredit:Laboratory of Biomolecular Engineering and Nanomedicine/Rice University
Endotelcellerne, der beklæder blodkarrene, er tæt pakket for at holde blodet inde og flyde, men forskere ved Rice University og deres kolleger har opdaget, at det kan være muligt selektivt at åbne huller i disse barrierer lige nok til at lukke store molekyler igennem - og derefter lukke dem igen.
Ris bioingeniør Gang Bao og samarbejdspartnere ved Emory University og Georgia Institute of Technology rapporterede, at de brugte magneter til at hjælpe jernoxidnanopartikler med at invadere endotelceller både i laboratoriet og in vivo. Så bruger de de samme magneter til at gøre kar midlertidigt "utætte".
Denne permeabilitet ville tillade lægemidler med store molekyler at nå målvæv, sagde Bao. Stærke magneter kan muligvis selv føre nanopartikelinfunderede stamceller eller lægemiddelfyldte nanopartikler til målrettede områder, selv i dybe væv som organer, som nuværende terapier ikke kan nå, han sagde.
Undersøgelsen vises i dag i Naturkommunikation .
"For mange sygdomme, systemisk levering gennem blodbanen er den eneste måde at levere molekyler til stedet, " sagde Bao. "Små molekyler kan trænge ind i blodkarret og komme ind i de syge celler, men store molekyler som proteiner eller lægemiddelfyldte nanopartikler kan ikke passere endotelet effektivt, medmindre det er utæt."
Blodkar i kræftsvulster har typisk huller i endotelbarrieren, men de lukker ikke efter behov, som Bao og hans team håber på at få dem til at gøre.
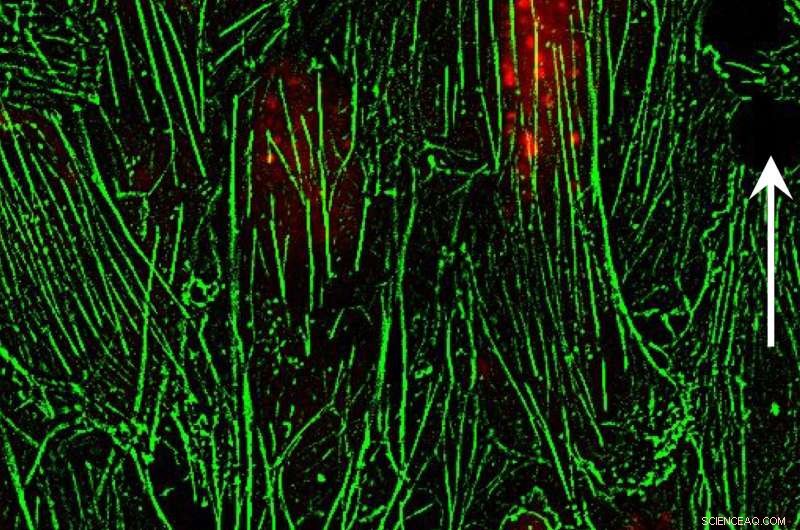
Under påvirkning af en magnet, nanopartikler justerer actinfilamenter i endotelceller. Rice University-forskere har mistanke om, at en sådan omlægning kan forstyrre samlingerne mellem endotelceller og øge vaskulær permeabilitet. Kredit:Laboratory of Biomolecular Engineering and Nanomedicine/Rice University
Sammen med lægemiddelmolekyler, Bao ønsker at bruge magneter til at levere nanopartikel-infunderede stamceller til skadet væv. "Medmindre du kan lave direkte indsprøjtning af stamceller, lad os sige ind i hjertet, du skal lave systemisk levering, og du har ingen kontrol over, hvor de går hen.
"Vores oprindelige idé var at levere magnetiske nanopartikler ind i stamceller og derefter bruge en magnet til at tiltrække stamcellerne til et bestemt sted, sagde han. Ved at gøre det, vi opdagede også, at ved at anvende et magnetfelt, vi kunne generere ændringer i cellens skeletstruktur med hensyn til actinfilamentstrukturerne."
Disse strukturelle elementer giver celler deres form og hjælper med at holde naboceller tæt komprimeret. "Vi tænkte, om vi kunne ændre celle-celle-forbindelsen ved at bruge magnetisk kraft, der var en mulighed for, at vi kunne konstruere fartøjets utæthed, " sagde Bao.
Laboratoriet skabte et mikrofluidisk flowkammer, der efterlignede det vaskulære system og forede dets rør med rigtige endotelceller. Eksperimenter beviste deres hypotese:Når et magnetfelt blev påført de nanopartikel-infunderede celler, hullerne åbnede sig. Aflastning af kraften gjorde det muligt for de fleste huller at lukke efter 12 timer.
Mikroskopiske billeder viste, at fluorescerende mærkede nanopartikler var jævnt fordelt inde i endotelkanalen, når et magnetfelt ikke blev påført. Da det var, partiklerne omfordelt, og den kraft, de påførte, forvrængede cytoskelettet.

Rice University-forskere forbereder et parti jernoxid-nanopartikler til eksperimenter. De har opdaget partiklerne, sammen med stærke magneter, kan bruges til at åbne mellemrum for lægemiddellevering mellem endotelcellerne, der beklæder blodkarrene. Fra venstre, Gang Bao, Sheng Tong og Linlin Zhang. Kredit:Jeff Fitlow/Rice University
På nogle billeder, aktinfilamenter, der hjælper med at give en celle dens form, blev observeret på linje med kraften. "Det er en ret dramatisk ændring, " sagde Bao. "Når du først anvender kraften, givet nok tid, cellernes struktur ændres. Det fører til åbningen af celle-celle-forbindelsen."
Bao sagde, at den magnetiske kraft også genererer et biologisk signal, der ændrer cytoskeletstrukturen. "Det bidrager også til utætheden, " sagde han. "Vi forsøger stadig at forstå, hvilken slags signal vi giver til celler, og hvordan de individuelle celler reagerer."
Mens der er metoder til at lette to typer transport over endotelbarrieren - paracellulær (mellem celler) og transcellulær (gennem celler) - har ingen af dem evnen til at målrette specifikke områder af kroppen. Bao sagde, at hans teams tilgang tilbyder en løsning.
Han sagde, at hans gruppe er en del af et igangværende samarbejdsprojekt om knæreparation med Dr. Johnny Huards laboratorium, en professor i ortopædisk kirurgi ved University of Texas Health Science Center i Houston. "Problemet er, hvordan man akkumulerer terapeutiske stamceller omkring knæet og holder dem der, " sagde Bao. "Efter at have injiceret de nanopartikel-infunderede celler, vi ønsker at sætte en række magneter rundt om knæet for at tiltrække dem.
"Men hvis du vil behandle hjertet eller leveren, du skal bruge en ret stor enhed for at have det nødvendige magnetfelt, " sagde han. "Det har vi ikke endnu. At drive dette til et klinisk miljø vil være en udfordring."
 Varme artikler
Varme artikler
-
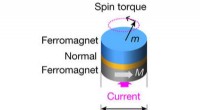 Magnetisk enhed i nanoskala efterligner neuronernes adfærd og kan genkende menneskelige lydsignalerSkematisk af en spin-drejningsmoment nano-oscillator, bestående af et ikke-magnetisk afstandsstykke (guld) mellem to ferromagnetiske lag, med magnetisering m for det frie lag (blå) og M for det faste
Magnetisk enhed i nanoskala efterligner neuronernes adfærd og kan genkende menneskelige lydsignalerSkematisk af en spin-drejningsmoment nano-oscillator, bestående af et ikke-magnetisk afstandsstykke (guld) mellem to ferromagnetiske lag, med magnetisering m for det frie lag (blå) og M for det faste -
 Computing med molekyler:Et stort skridt inden for molekylær spintronikHvert molekyle kan adresseres separat med et scanningstunnelmikroskop og skiftes mellem tilstande ved at anvende en positiv eller negativ spænding. Kredit:Jan-Simon von Glasenapp og Rainer Herges
Computing med molekyler:Et stort skridt inden for molekylær spintronikHvert molekyle kan adresseres separat med et scanningstunnelmikroskop og skiftes mellem tilstande ved at anvende en positiv eller negativ spænding. Kredit:Jan-Simon von Glasenapp og Rainer Herges -
 Prototypeværktøjer til masseproduktion af nanostrukturer lanceres i SingaporeEn af de firkantede plastikfilm, der bærer mønstre i nanometerstørrelse, rulles ud af prototypen roll-to-roll UV nanoimprinter - Roll-to-roll-behandling vil gøre det muligt at fremstille sådan unik pl
Prototypeværktøjer til masseproduktion af nanostrukturer lanceres i SingaporeEn af de firkantede plastikfilm, der bærer mønstre i nanometerstørrelse, rulles ud af prototypen roll-to-roll UV nanoimprinter - Roll-to-roll-behandling vil gøre det muligt at fremstille sådan unik pl -
 Babytrin til gennemsigtig elektronikScanning elektronmikroskop (SEM) billedet viser, at Ag nanotrådene er fuldstændig forbundet efter laserbehandling. Kredit:Li et al Et submikrometertyndt net af sølv nanotråde - der er gennemsigtig
Babytrin til gennemsigtig elektronikScanning elektronmikroskop (SEM) billedet viser, at Ag nanotrådene er fuldstændig forbundet efter laserbehandling. Kredit:Li et al Et submikrometertyndt net af sølv nanotråde - der er gennemsigtig


