Nanolock registrerer kræftmutation; kan føre til tidlige diagnoser, personlige terapier
Øjeblikket, hvor raske celler bliver til kræftceller, er et kritisk punkt. Og hvis fanget tidligt nok, mange kræftformer kan stoppes i deres spor. En gruppe melder sig ind ACS sensorer at de har udviklet en præcis og følsom metode, der kan genkende en bestemt mutation i den genetiske kode, der har været impliceret i sygdommen. Det kunne hjælpe læger med at diagnosticere kræftformer tidligere og behandle dem med individualiserede terapier.
Kræftdrivermutationer hjælper med initiering og progression af kræft. En sådan mutation i BRAF genet har været forbundet med adskillige kræftformer, herunder kræft i skjoldbruskkirtlen. Den nuværende metode til påvisning af drivermutationer er real-time PCR, hvor mutante DNA-sekvenser selektivt amplificeres og kopieres, men det er ikke nøjagtigt nok til at opdage disse genetiske ændringer pålideligt. Forskere har udviklet metoder til at læse den genetiske sekvens ved at flytte den gennem en nanopore, men igen, metoden er ikke nær præcis nok i sig selv. Så, Li-Qun Gu og kolleger søgte en måde at bedre lokalisere disse mutationer, og med enkeltmolekyle opløsning, bygger på deres tidligere arbejde med at udvikle en "nanolock-nanopore" sensor.
En nanolock er en speciel struktur, der kan stabilisere basepar af DNA'et på mutationsstedet, når det går gennem en nanopore. Holdet har nu fundet ud af, at mutant-DNA, der bærer en nanolock, gennemgår en unik form for udlåsning, når det bevæger sig gennem poren. Opdagelse af denne aktivitet resulterede i et meget nøjagtigt og følsomt nanoporefingeraftryk for BRAF mutation i vævsprøver fra patienter med skjoldbruskkirtelkræft. Forskerne siger, at de forventer tilgangen, en gang integreret med en miniature, højkapacitetsenhed, kunne muliggøre nøjagtig og PCR-fri påvisning af forskellige sygdomsfremkaldende mutationer til diagnose og prognose.
 Varme artikler
Varme artikler
-
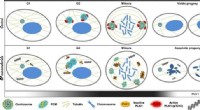 Forskere afslører anticanceregenskaber af nanomaterialer med mitose-målretningsmekanismeEn model til at illustrere den molekylære anticanceraktivitet af BP-nanomaterialer gennem blokering af mitotisk progression. Kredit:SIAT En forskergruppe ledet af prof. Li Hongchang fra Shenzhen I
Forskere afslører anticanceregenskaber af nanomaterialer med mitose-målretningsmekanismeEn model til at illustrere den molekylære anticanceraktivitet af BP-nanomaterialer gennem blokering af mitotisk progression. Kredit:SIAT En forskergruppe ledet af prof. Li Hongchang fra Shenzhen I -
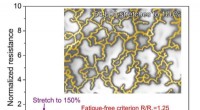 Forskere skaber træthedsfri, strækbar lederTræthedsfri fleksibel transparent elektrode til strækbar og bøjelig elektronik. Kredit:University of Houston Forskere har opdaget en ny strækbar, gennemsigtig leder, der kan foldes eller strækkes
Forskere skaber træthedsfri, strækbar lederTræthedsfri fleksibel transparent elektrode til strækbar og bøjelig elektronik. Kredit:University of Houston Forskere har opdaget en ny strækbar, gennemsigtig leder, der kan foldes eller strækkes -
 Underlagsfejl er nøglen til vækst af 2-D materialerGrafik, der viser en bornitridoverflade med wolframatomer, der forankrer trekantede domæner, der illustrerer defektkontrol af orienteringen. Kredit:Xiaotian Zhang/Penn State At skabe to-dimensione
Underlagsfejl er nøglen til vækst af 2-D materialerGrafik, der viser en bornitridoverflade med wolframatomer, der forankrer trekantede domæner, der illustrerer defektkontrol af orienteringen. Kredit:Xiaotian Zhang/Penn State At skabe to-dimensione -
 Sulfid og jern arbejder sammen for at afsløre en ny vej til radionuklidsekvesteringSigtning af radionuklider med svovl:Technetium -bindingsveje under sulfidogene forhold stimuleret af nZVI tilbyder en muligvis mere bæredygtig, miljøvenlig tilgang til bioremediering. Som en vedva
Sulfid og jern arbejder sammen for at afsløre en ny vej til radionuklidsekvesteringSigtning af radionuklider med svovl:Technetium -bindingsveje under sulfidogene forhold stimuleret af nZVI tilbyder en muligvis mere bæredygtig, miljøvenlig tilgang til bioremediering. Som en vedva
- Kuglehobe 4 milliarder år yngre end tidligere antaget
- Attraktive forretningskvinder betragtes som mindre troværdige femmes fatales
- Neutroner afslører den vilde Weyl-verden af halvmetaller
- Hvad er forskellen mellem svejsning og lodning?
- Aneurismenummer kan hjælpe kirurger med at træffe behandlingsbeslutninger
- At finde mørkt stof i mørket


