Nanopartikler tager en bid af infektioner

En hurtig test under UV-lys afslører, om dental billeddannende plader er forurenet med bakterier, takket være polymerer indlejret med multifunktionelle nanopartikler. Kredit:Gengivet med tilladelse fra ref 1. © 2016 Wiley-VCH
Antibiotika-resistente bakterier, der koloniserer overflader og medicinsk udstyr, forårsager alarmerende årlige stigninger i antallet af patienter, der bliver smittet på hospitaler og klinikker. Et KAUST-team arbejder på at reducere disse tal med en smart polymer, der ændrer farve og aktiverer naturlige antimikrobielle enzymer, når bakteriel kontaminering opdages.
Konstant eksponering for spytbakterier gør tandværktøjer, såsom genanvendelige røntgenbilledplader, ideelle miljøer for virulente biofilm. En løsning på dette problem er at belægge enheder med polymerer indlejret med nanoskala krystaller, der langsomt frigiver sølvioner, et bredspektret biocidmiddel. Imidlertid, udfordringer med nanopartikeludvaskning, har forpurret udviklingen af denne teknologi.
Lektor Niveen Khashab, hendes ph.d. studerende Shahad Alsaiari og kolleger fra universitetets center for avancerede membraner og porøse materialer indså, at skift til guldnanopartikler kunne give antimikrobielle belægninger detektionsevner - disse små krystaller har følsomme optiske egenskaber, der kan indstilles til at spotte specifikke biomolekylære interaktioner. Men at inkorporere dem sikkert i polymerer krævede nye typer nanofillers.
"Nanofillers er små kemiske midler fordelt i matrixen af en polymerkomposit, " forklarede Khashab. "De er dopanter, så de forbedrer det almindelige materiale og introducerer nye egenskaber - i vores tilfælde, gør belægningen antibakteriel."
Holdets tilgang bruger guld nanoclusters behandlet med lysozymenzymer, der har medfødt forsvar mod patogener, såsom Escherichia coli, almindeligvis kendt som E. coli. De fastgjorde disse kolloider til overfladen af lidt større, porøse silica nanopartikler fyldt med antibiotiske lægemiddelmolekyler.
Normalt, dette guld-silica kompleks udsender glødende, rødt fluorescerende lys. Men når lysozymenhederne støder på bakterier, en stærk tiltrækning af cellevægge river guld-nanoklyngerne fra deres silicapartnere - en handling, der samtidig slukker for fluorescens og frigiver antibiotikalasten.
Blandingseksperimenter afslørede de guldbaserede nanofyldstoffer integreret grundigt i polymerkompositter og udviste minimal udvaskning under forsøg med E. coli. Khashab tilskriver disse gunstige polymerinteraktioner de skarpe, blotlagte kanter af guldklynger på silicakuglerne
Forskerne testede deres koncept ved at sammenligne røntgentandplader med og uden den smarte polymerbelægning. Begge prøver gav de samme højopløselige billeder af tænder og knoglestruktur. Imidlertid, kun den belagte plade muliggjorde hurtig visuel vurdering af bakteriel kontaminering, blot ved at oplyse enheden med en UV-lampe og se efter farveændring. Vellykket frigivelse af det antibakterielle middel reducerede også drastisk biofilmopbygning.
"Belægningsprocessen er nem, " bemærkede Khashab. "Vi kigger på at forbedre denne teknologi til at omfatte andet medicinsk udstyr i forskellige størrelser og former."
 Varme artikler
Varme artikler
-
 Robust ny proces danner 3D-former fra flade ark af grafenDenne undersøgelse viser grafenintegration til en række forskellige mikrostrukturerede geometrier, herunder pyramider, søjler, kupler, og omvendte pyramider. Kredit:Nam Research Group, University of I
Robust ny proces danner 3D-former fra flade ark af grafenDenne undersøgelse viser grafenintegration til en række forskellige mikrostrukturerede geometrier, herunder pyramider, søjler, kupler, og omvendte pyramider. Kredit:Nam Research Group, University of I -
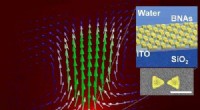 Forskere modellerer makroskala plasmonisk konvektion for at kontrollere væske og partikelbevægelseDette er en skildring af væskekonvektionen (pile) overlejret på baggrundstemperaturfordelingen produceret af BNAerne og ITO. Indsatsen viser BNA -geometrien med et (falsk farve) scanningselektronmikro
Forskere modellerer makroskala plasmonisk konvektion for at kontrollere væske og partikelbevægelseDette er en skildring af væskekonvektionen (pile) overlejret på baggrundstemperaturfordelingen produceret af BNAerne og ITO. Indsatsen viser BNA -geometrien med et (falsk farve) scanningselektronmikro -
 Små 3D-strukturer forbedrer solcelleeffektivitetenDenne skematiske repræsentation viser den nye struktur:nikkeloxidstriber løber vinkelret på det faktiske materiale, fungerer som en bane for elektronerne. Kredit:Lutz Mühlenbein En ny metode til a
Små 3D-strukturer forbedrer solcelleeffektivitetenDenne skematiske repræsentation viser den nye struktur:nikkeloxidstriber løber vinkelret på det faktiske materiale, fungerer som en bane for elektronerne. Kredit:Lutz Mühlenbein En ny metode til a -
 Forskere udvikler en omkostningseffektiv måde at forbedre optiske gassensorer fra en fælles forbin…Kredit:Concordia University For mange, zinkoxid fremmaner billeder af lyse striber ned ad livreddernes næser. Men for forskere på Concordias fakultet for kunst og naturvidenskab, ZnO er en spænden
Forskere udvikler en omkostningseffektiv måde at forbedre optiske gassensorer fra en fælles forbin…Kredit:Concordia University For mange, zinkoxid fremmaner billeder af lyse striber ned ad livreddernes næser. Men for forskere på Concordias fakultet for kunst og naturvidenskab, ZnO er en spænden
- Ultrahurtige grafenbaserede fotodetektorer med datahastigheder på op til 50 GBit/s
- Test for halogen
- Hvordan er Rock Salt dannet?
- Læsning mellem diamanterne:Forskere udvider den dybe kulstofhistorie
- De ublu omkostninger ved klimaudsættelse
- Ny PPPL-opfindelse kunne forbedre effektiviteten af bil- og lastbilmotorer og samtidig reducere fo…


