Færre forsøgsdyr takket være sekundære nanokroppe

Alpakaerne holdt på Max Planck Institute for Biophysical Chemistry vandrer frit over store enge. Efter meget milde vaccinationer af to alpakaer, Göttingen-forskerne hentede byggeplaner for de sekundære nanokroppe fra en lille blodprøve. Ved hjælp af disse planer, bakterier kan programmeres til at producere dem i stor skala uden yderligere dyrs involvering. Kredit:© MPI for Biophysical Chemistry/ I. Böttcher-Gajewski
Antistoffer er uundværlige i biologisk forskning og medicinsk diagnostik. Imidlertid, deres produktion er tidskrævende, dyrt, og kræver brug af mange dyr. Forskere ved Max Planck Instituttet for Biofysisk Kemi i Göttingen, Tyskland, har nu udviklet såkaldte sekundære nanostoffer, der kan erstatte de mest anvendte antistoffer og drastisk kan reducere antallet af dyr i antistofproduktion. Dette er muligt, fordi de sekundære nanostoffer kan produceres i stor skala af bakterier. I øvrigt, de sekundære nanobodies udkonkurrerer deres traditionelle antistof-modstykker i centrale cellebiologiske applikationer.
Som en central del af vores immunsystem, antistoffer beskytter os mennesker og andre hvirveldyr mod patogener. De er, imidlertid, også væsentlige værktøjer inden for medicinsk diagnostik, terapi, og grundforskning - fx i fluorescensmikroskopi. Når forskere vil studere et bestemt protein i en celle, de kan markere det selektivt med antistoffer rettet mod dette protein. Når først disse såkaldte primære antistoffer har bundet deres mål, sekundære antistoffer påføres. Disse binder de primære antistoffer, bære fluorescerende farvestoffer, der lyser under mikroskopet, og dermed synliggøre proteinet af interesse.
Det store udvalg af primære antistoffer produceres traditionelt i små pattedyr som kaniner og mus:For det første, dyrene immuniseres med det rensede protein - det kan sammenlignes med at vaccinere mennesker. Som resultat, dyrenes immunsystem danner antistoffer mod proteinet. Antistofferne opsamles endelig fra dyrenes blod, og bearbejdet. Da antistoffer bruges af tusindvis af laboratorier verden over, og fordi de fleste af deres anvendelser er afhængige af sekundære antistoffer, sidstnævnte er i enorm efterspørgsel. Derfor, produktionen af sekundære antistoffer nødvendiggør ikke kun mange, men også store dyr som æsler, geder, eller får. Dette udgør et etisk problem.
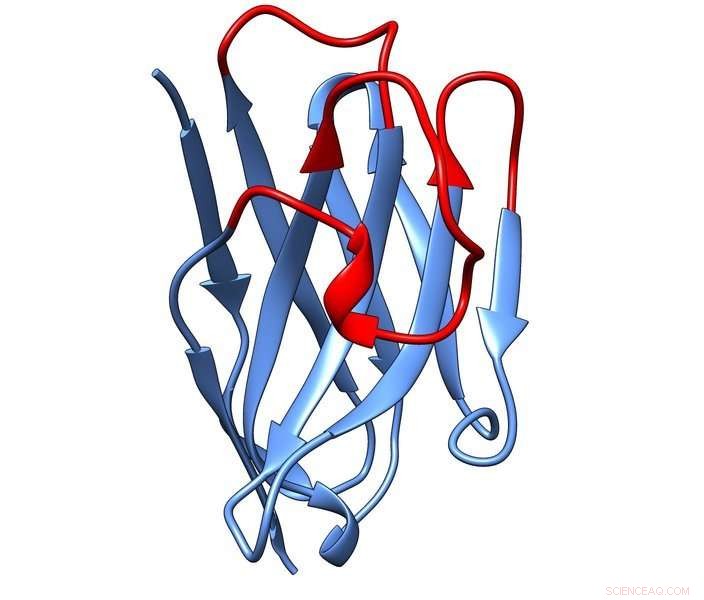
Tredimensionel struktur af en nanobody. Kredit:© MPI for Biofysisk Kemi/ T. Pleiner og S. Trakhanov
Sekundære nanostoffer kan produceres i bakterier
Forskere ved Max Planck Institute for Biophysical Chemistry præsenterer nu et bæredygtigt alternativ, der kan erstatte sekundære antistoffer rettet mod primære fra mus eller kaniner. Den er afhængig af såkaldte nanobodies og kan drastisk reducere antallet af dyr, der bruges til antistofproduktion. Nanobodies er fragmenter af specielle antistoffer fra kameler og beslægtede arter såsom alpakaer. "Vi har udviklet sekundære nanobodies, der ikke kun yder meget godt, men også, de kan fremstilles mikrobiologisk i enhver skala - ligesom øl i en gærer, " forklarer Dirk Görlich, Direktør ved Max Planck Instituttet i Göttingen og leder af projektet.
"Sekundære antistoffer skal opfylde ekstremt strenge kvalitetskrav og må kun påvise primære antistoffer af en enkelt art og ingen strukturer i de analyserede celler eller medicinske prøver. problemet var at få byggeplaner for virkelig perfekte sekundære nanobodies. Vi startede med et stort antal varianter, som vi udtog fra en lille mængde blod fra to immuniserede alpacaer. Ved såkaldt fag-visning, så fiskede vi de bedste varianter frem og brugte dem til sidst til at programmere bakterier til nanobody-produktion, " forklarer Tino Pleiner, første forfatter til værket.
Nanobodies blev første gang beskrevet i 1993 af en belgisk banebrydende gruppe af videnskabsmænd. Siden da, forskere forsøger at udnytte dem til deres arbejde i laboratoriet. Imidlertid, at erstatte sekundære antistoffer med nanobodies viste sig slet ikke at være trivielt. En grund er nanobodernes størrelse:De er ti gange mindre end normale antistoffer. Derfor, de giver meget mindre plads til at koble fluorescerende molekyler og fremstår derfor langt mere svagt i mikroskopet end konventionelle antistoffer.

Sekundære nanobistoffer koblet til fluorescerende farvestoffer kan erstatte respektive sekundære antistoffer i mikroskopi. Billedet viser kræftceller farvet med primære antistoffer mod lamin A/C (markeret med grønt) og celleproliferationsmarkøren Ki-67 (rød), der blev påvist med specifikke sekundære nanobistoffer. [mindre] Kredit:© MPI for Biophysical Chemistry/ T. Pleiner
"Ja, vores første eksperimenter med sekundære nanobodies var temmelig skuffende og producerede kun mørke og støjende billeder. Imidlertid, vi gav ikke op, og immuniserede de to alpakkaer igen for at stimulere deres immunsystem til at forbedre de indledende nanostoffer. Yderligere udvikling i reagensglasset, en speciel koblingsstrategi for de fluorescerende farvestoffer, og at kombinere to eller flere kompatible nanobodies klarede resten, Görlich fortæller om indledende vanskeligheder. nanobodies matcher i det mindste konventionelle antistoffer med hensyn til signalstyrke.
Forbedret opløsning i lysmikroskopi
Nanobodies har klare fordele i forhold til sekundære antistoffer. "Super-opløsning fluorescensmikroskopi, for eksempel, kan optisk løse cellulære strukturer i intervallet nogle få nanometer. Imidlertid, sådanne billeder bliver slørede, når der bruges primære og sekundære antistoffer, der hver allerede måler 15 nanometer. Brug af nanobodies med en størrelse på kun tre nanometer forbedrer faktisk opløsningen, " siger Pleiner.
"Vi har testet de sekundære nanobodies i andre applikationer udover mikroskopi, og resultaterne er meget lovende, " understreger Görlich. Især den nye produktionsvej i bakterier letter deres modifikation og fusion til andre reporterproteiner, for eksempel enzymer. "Vi forventer, at vores nanobodies i mange applikationer vil erstatte konventionelle sekundære antistoffer fra æsler, geder, eller får."
Sidste artikelNy indsigt i grafen
Næste artikelFluorescerende nanomedicin kan guide tumorfjernelse, dræbe de resterende kræftceller
 Varme artikler
Varme artikler
-
 Enkelt molekylært lag og tynd siliciumstråle muliggør nanolaserdrift ved stuetemperaturKredit:Arizona State University For første gang, forskere har bygget en nanolaser, der kun bruger et enkelt molekylært lag, placeret på en tynd siliciumstråle, som fungerer ved stuetemperatur. Den
Enkelt molekylært lag og tynd siliciumstråle muliggør nanolaserdrift ved stuetemperaturKredit:Arizona State University For første gang, forskere har bygget en nanolaser, der kun bruger et enkelt molekylært lag, placeret på en tynd siliciumstråle, som fungerer ved stuetemperatur. Den -
 Lysstyret gearkasse til nanomaskinerKunstnerisk gengivelse af en nanomaskine, der kombinerer motor (rød og blå) og kobling (grøn og lilla) underenheder forbundet med transmissionsunderenheder (polymerkæder repræsenteret som strenge). Di
Lysstyret gearkasse til nanomaskinerKunstnerisk gengivelse af en nanomaskine, der kombinerer motor (rød og blå) og kobling (grøn og lilla) underenheder forbundet med transmissionsunderenheder (polymerkæder repræsenteret som strenge). Di -
 Taranteller inspirerer til nye strukturelle farver med den største betragtningsvinkelUdviklingen af ikke-iriserende strukturelt farvet materiale inspireret af tarantelhår. Kredit:University of Akron Inspireret af håret på blå taranteller, forskere fra University of Akron leder e
Taranteller inspirerer til nye strukturelle farver med den største betragtningsvinkelUdviklingen af ikke-iriserende strukturelt farvet materiale inspireret af tarantelhår. Kredit:University of Akron Inspireret af håret på blå taranteller, forskere fra University of Akron leder e -
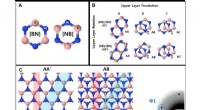 En ultimativ endimensionel elektronisk kanal i sekskantet bornitridEt lag af sekskantet bornitrid har form som en hønsenet, og dannes ved vekslen af bor (B, pink) og nitrogen (N, blå). Afhængigt af hvordan lagene er stablet sammen, materialet antager forskellige ar
En ultimativ endimensionel elektronisk kanal i sekskantet bornitridEt lag af sekskantet bornitrid har form som en hønsenet, og dannes ved vekslen af bor (B, pink) og nitrogen (N, blå). Afhængigt af hvordan lagene er stablet sammen, materialet antager forskellige ar
- Fulleren-kugler kan bruges til at glide i nanoverdenen
- Hvordan reproducerer nåletræer?
- Et nærmere kig på potentialet for vandopdeling af solbrændstof
- Hurtige klimaændringer på tværs af den nordlige halvkugle i den tidligste Mellem-Pleistocæn
- Højindkomster har et stærkere sikkerhedsnet efter jobtab
- Radiohalo detekteret i en galaksehob med lav masse


